
【题目】Y是合成香料、医药、农药及染料的重要中间体,可由X在酸性条件下反应得到:
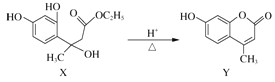
下列说法正确的是( )
A.X分子中所有碳原子可能共平面
B.X、Y分别与足量H2加成后的分子中均含有手性碳原子
C.Y可以发生显色、氧化和还原反应,还可以与甲醛发生缩聚反应
D.1mol的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为4∶3
【答案】BC
【解析】
A.X含有饱和碳原子,具有甲烷的结构特征;
B.苯环、碳碳双键都可与氢气发生加成反应,手性碳原子应连接4个不同的原子或原子团;
C.Y含有酚羟基和碳碳双键,具有酚、烯烃的性质;
D.X中酚羟基、酯基可与氢氧化钠溶液反应,Y中酚羟基、酯基可与氢氧化钠反应,且酯基可水解生成酚羟基和羧基。
A.X分子中含有饱和碳原子,具有甲烷的结构特征,因此所有的碳原子不可能在同一个平面上,A错误;
B.苯环、碳碳双键都可与氢气发生加成反应,反应后连接甲基的碳原子为手性碳原子,连接4个不同的原子或原子团,B正确;
C.Y含有酚羟基和碳碳双键,酚羟基可发生显色反应,碳碳双键可发生氧化、还原反应,酚可与甲醛发生缩聚反应,C正确;
D.X中酚羟基、酯基可与氢氧化钠溶液反应,1mol可与3molNaOH反应,Y中酚羟基、酯基可与氢氧化钠反应,且酯基可水解生成酚羟基和羧基,则1molY可与3molNaOH反应,最多消耗NaOH的物质的量之比为1:1,D错误;
故合理选项是BC。


科目:高中化学 来源: 题型:
【题目】某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
(1)现有以下仪器和用品:橡胶管、秒表、温度计、amol/L稀硝酸、bmol/L稀硝酸及下图中仪器.
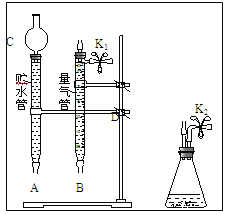
①写出本实验的化学方程式,并标出电子转方向和数目:__________________________.
②设计实验方案:在_________________下,测定________________________________.
③在答卷的图中将A、B、C、D、几处用橡胶管以正确方式连接起来,以测定反应所产生气体的体积(三个容器中的液体和水都已画出)_______________.
④测定前,为避免NO被氧化为NO2,要用CO2排出锥形瓶和橡胶管中的空气:在锥形瓶中加入铜片后松开K2弹簧夹,从K2处的橡胶管向装置中通入CO2,此时K1处应进行的操作是____________,则空气已排尽.
(2)注入稀硝酸后,在给定条件下设计实验探究浓度和温度对化学反应速率的影响:温度25℃、50℃;时间t1、t2、t3;收集气体体积V1、V2.请完成下表:____________
实验 | 稀硝酸的浓度/(mol/L) | 稀硝酸的体积/mL | 温度 | 时间 | 收集气体 |
① | a | V | 25 | t1 | V1 |
② | V | ||||
③ | V |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g)![]() CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是

A. 该反应的△H<0,且p1<p2
B. 反应速率:ν逆(状态A)>ν逆(状态B)
C. 在C点时,CO转化率为75%
D. 在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿挥发油是青蒿的活性成分(几乎不溶于水,可溶于乙醚,熔点156-157℃,对热不稳定,乙醚的沸点34.6℃),有抗菌、解热、止咳等作用。实验室从青蒿中提取青蒿挥发油的流程如图所示。
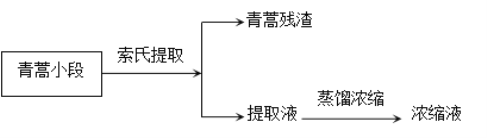
索氏提取装置如图所示,实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与青蒿小段接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿小段的连续萃取。回答下列问题:
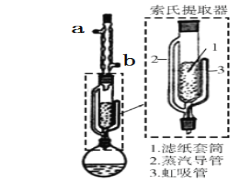
(1)实验时需将青蒿剪成1-2cm小段,放入滤纸套筒1中,剪成小段的目的是___,圆底烧瓶中加入乙醚为溶剂时,应不超过烧瓶容积的___。
(2)索氏提取器中滤纸套筒的高度(x)、套管内青蒿小段的高度(y)及虹吸管的高度(z)由大到小的顺序是___(用x、y、z回答),与常规的萃取相比,采用索氏提取器的优点是___。
(3)提取时球形冷凝管中冷水应从__(填“a”或“b”)管导入,提取液需经___(“常压”或“减压”)蒸馏法除去大部分溶剂,下列仪器在该蒸馏中需要用到的有___(填字母标号)。
A.直形冷凝管 B.球形冷凝管 C.锥形瓶 D.烧杯 E.温度计
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用![]() 可消除
可消除![]() 的污染,反应原理为:
的污染,反应原理为:![]() ,在10L密闭容器中分别加入
,在10L密闭容器中分别加入![]() 和
和![]() ,测得不同温度下
,测得不同温度下![]() 随时间变化的有关实验数据如表所示:
随时间变化的有关实验数据如表所示:
组别 | 温度 | 时间 物质的量 | 0 | 10 | 20 | 40 | 50 |
|
|
|
|
|
|
|
|
|
|
|
|
|
| M |
|
下列说法正确的是
A.组别![]() 中
中![]() 内,
内,![]() 降解速率为
降解速率为![]()
B.由实验数据可知温度![]()
C.![]() 时,表格中M对应的数据为
时,表格中M对应的数据为![]()
D.该反应只有在高温下才能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A.标准状况下,22.4 L CH2Cl2中含有碳原子数为NA
B.在溶有1molFe(OH)3的胶体中含有的胶粒数小于NA
C.常温下0.2 mol铝与足量浓硫酸反应,生成气体的分子数为0.3 NA
D.常温下向密闭容器内充入46 g NO2,容器中气体的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g) +2H2(g) ![]() CH3OH(g) △H =-90.8 kJ·mol-1
CH3OH(g) △H =-90.8 kJ·mol-1
300℃时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 | |
反应物投入量 | 1 molCO、2 mol H2 | 1mol CH3OH | 2mol CH3OH | |
平衡 时 数据 | CH3OH的浓度(mol·L-1) | c1 | c2 | c3 |
反应的能量变化 | a kJ | bkJ | ckJ | |
体系压强(Pa) | p1 | p2 | p3 | |
反应物转化率 | a1 | a2 | a3 | |
下列说法正确的是
A. 2c1>c3 B. ∣a∣+∣b∣=90.8
C. 2p2<p3 D. a1+ a3<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
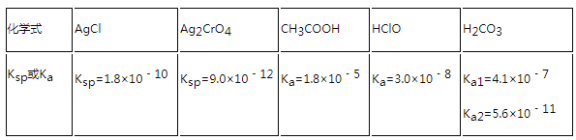
A.相同浓度CH3COONa和NaClO的混合溶液中,各种离子浓度的大小关系是:c(Na+)>c(ClO﹣)>c(CH3COO﹣)>c(OH﹣)>c(H+)
B.次氯酸钠溶液中通入少量CO2的离子方程式为:2ClO﹣+CO2+H2O=CO32﹣+2HClO
C.向0.1 molL﹣1CH3COOH溶液中滴加NaOH溶液中至c(CH3COOH):c(CH3COO﹣)=5:9,此时溶液的pH=5
D.向浓度均为1.0×10﹣3molL﹣1的KCl和K2CrO4混合溶液中滴加1.0×10﹣3molL﹣1的AgNO3溶液,CrO42﹣先形成沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com