
【题目】氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素![]() 的碱性溶液制氢气的装置示意图
的碱性溶液制氢气的装置示意图![]() 电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极
电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极![]() 。
。
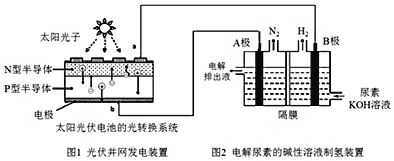
(1)图1中N型半导体为______![]() 填“正极”或“负极”
填“正极”或“负极”![]()
(2)该系统工作时,A极的电极反应式为______
(3)若A极产生![]()
![]() ,则此时B极产生______L
,则此时B极产生______L![]() 标况下
标况下![]() 。
。
【答案】负极 ![]()
![]()
【解析】
(1)电解池中,氮元素化合价升高产生氮气,则A极作阳极,氢元素化合价降低产生氢气,则B作阴极,阴极与电源的负极相连;
(2)![]() 为阳极,尿素在碱性条件失电子产生碳酸根、氮气、水;
为阳极,尿素在碱性条件失电子产生碳酸根、氮气、水;
(3)根据电路中转移电子数相等计算。
(1)电解尿素中,氮元素化合价由![]() 价变为0价,H元素化合价由
价变为0价,H元素化合价由![]() 价变为0价,则氮元素被氧化,氢元素被还原,所以生成氮气的电极A是阳极,生成氢气的电极B是阴极,与电源负极相连的是阴极,则图1中N型半导体为负极,P型半导体为正极,故答案为:负极;
价变为0价,则氮元素被氧化,氢元素被还原,所以生成氮气的电极A是阳极,生成氢气的电极B是阴极,与电源负极相连的是阴极,则图1中N型半导体为负极,P型半导体为正极,故答案为:负极;
(2)![]() 为阳极,发生氧化反应,电极反应式为:
为阳极,发生氧化反应,电极反应式为:![]() ,故答案为:
,故答案为:![]() ;
;
(3)若A极产生![]()
![]() ,氮气的物质的量为:
,氮气的物质的量为:![]() ,转移电子的物质的量为:
,转移电子的物质的量为:![]() ,所以生成氢气的物质的量为:
,所以生成氢气的物质的量为:![]() ,则体积为:
,则体积为:![]() ,故答案为:
,故答案为:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】分别向等体积的不含O2、含有O2的0.1mol·L1BaCl2溶液中通入SO2,探究体系中物质间的相互作用,实验记录如下。(已知:pH越小,溶液酸性越强)
pH变化 |
|
溶液中是否产生沉淀 | 不含O2的BaCl2溶液中没有白色沉淀,含有O2的BaCl2溶液中产生白色沉淀。 |
下列说法不正确的是
A.a所示溶液的pH降低的原因:SO2与H2O反应生成H2SO3,溶液的c(H+)增大
B.b所示溶液中发生反应:2Ba2++O2+2SO2+2H2O=2BaSO4↓+4H+
C.b比a所示溶液的pH小的原因:Ba2++SO2+H2O=BaSO3↓+2H+
D.SO2通入不含O2的BaCl2溶液后,再通入NH3,产生BaSO3沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列电解质溶液的说法中,正确的是
A.常温下,![]() 与
与![]() 两溶液混合后
两溶液混合后![]() ,则一定有
,则一定有![]()
B.常温下,![]() 溶液与
溶液与![]() 溶液混合后所得
溶液混合后所得![]() 的溶液中:
的溶液中:![]()
C.![]() 溶液中离子总数为x,
溶液中离子总数为x,![]() 溶液中离子总数为y,则
溶液中离子总数为y,则![]()
D.已知:![]() 的
的![]() 为
为![]() ,若将浓度均为
,若将浓度均为![]() 的
的![]() 溶液和KOH溶液等体积混合,则会有
溶液和KOH溶液等体积混合,则会有![]() 沉淀产生
沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,石灰乳达到平衡:Ca(OH)2 (s)![]() Ca2+(aq)+2OH-(aq),下列叙述正确的是( )
Ca2+(aq)+2OH-(aq),下列叙述正确的是( )
A.加水,Ca(OH)2 溶解平衡向右移动,pH 增大
B.加入少量盐酸,Ca(OH)2 溶解平衡向右移动,ksp﹝Ca(OH)2﹞增大
C.加入少量氢氧化钠固体,Ca(OH)2 溶解平衡向左移动,溶液中 c(H+)减小
D.升高温度,Ca(OH)2 溶解平衡向右移动,ksp﹝Ca(OH)2﹞增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如图:

(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的离子方程式是_________________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
ⅰ:2Fe2++PbO2+4H++SO![]() ===2Fe3++PbSO4+2H2O
===2Fe3++PbSO4+2H2O
ⅱ:……
①写出ⅱ的离子方程式:_______________________________________。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b._________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸 H2Y 溶液中滴加 NaOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如图所示,下列有关说法错 误的是( )
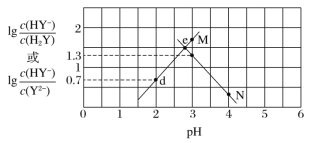
A.曲线 M 表示 pH 与 lgc(HY-)/c(H2Y)的变化关系
B.Ka2(H2Y)=10-4.3
C.d 点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(Na+)
D.交点 e 的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
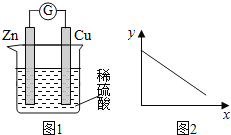
A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当下列物理量不再随时间变化时,表明反A(s)+2B(g)![]() C(g)+D(g)一定达到平衡状态的是
C(g)+D(g)一定达到平衡状态的是
A.混合气体的压强B.混合气体的密度
C.混合气体的物质的量D.混合气体中C和D的物质的量之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6mol,C的物质的量为0.8 mol。
2C(g)+2D(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)反应前A的物质的量浓度是________ mol·L-1 。
(3)10 s末,生成物D的物质的量浓度为____ mol·L-1。
(4)A与B的平衡转化率之比为________。
(5)反应过程中容器内气体的平均相对分子质量变化是________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com