
| 1 |
| 2 |
| 1 |
| 2 |
| A、-285.8kJ/mol |
| B、285.8kJ/mol |
| C、-241.8kJ/mol |
| D、241.8kJ/mol |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
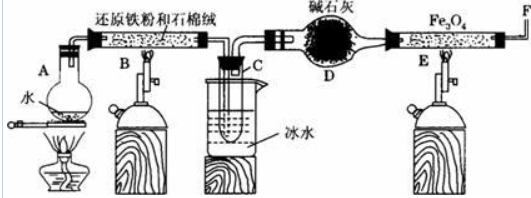
查看答案和解析>>
科目:高中化学 来源: 题型:
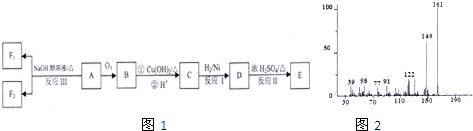

查看答案和解析>>
科目:高中化学 来源: 题型:
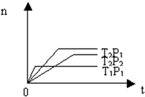 反应2X(g)+Y(g)?2Z(g);△H<0(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示.则下列判断正确的是( )
反应2X(g)+Y(g)?2Z(g);△H<0(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示.则下列判断正确的是( )| A、T1<T2,P1<P2 |
| B、T1<T2,P1>P2 |
| C、T1>T2,P1>P2 |
| D、T1>T2,P1<P2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤焦油中含有苯、二甲苯、苯酚等化工原料 |
| B、石油裂解的主要目的是为了获得短链不饱和烃 |
| C、烟、雾属于胶体,能产生丁达尔效应 |
| D、可用热的饱和碳酸钠溶液除去金属表面的矿物油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+,Al3+,Ag+,Ba2+,Fe3+ |
| 阴离子 | Cl-,CO32-,SO42-,NO3-,OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
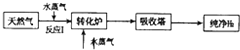
| 温度 | 400℃ | 500℃ | 800℃ | 1000℃ |
| 平衡常数 | 10 | 9 | 1 | 0.5 |
| 4 |
| 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com