
【题目】将标准状况下的a L氯化氢气体溶于100mL水中,得到的盐酸的密度为b g/mL,则该盐酸的物质的量的浓度是( ) mol/L
A. 10 a /22.4 B. 10 a /22.4(a +0.1)
C. ab/(22400+36.5a) D. 1000ab/(2240+36.5a)
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.苯和乙烷都能发生取代反应
B.石油的分馏和煤的干馏都是化学变化
C.工业上可通过石油分馏直接得到甲烷、乙烯和苯
D.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA代表阿伏加德罗常数,下列说法正确的是( )
A. 46gNO2和N2O4的混合液中总原子数为3NA
B. 4℃时9mL水和11.2L氮气含有相同的分子数
C. 同温同压下,NA个CO2与NA个N2和O2的混合气体的体积不相等
D. 1.01×105Pa时,11.2 L氧气所含的原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有NH3,另一个盛有N2、H2的混合气体,在同温同压下,两容器内的气体一定具有相同的
A. 原子数 B. 分子数 C. 质量 D. 密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是
A. n(H2CO3)和n(HCO3-)之和为1mol的NaHCO3溶液中,含有Na+数目为NA
B. 17gH2O2所含非极性键数目为0.5NA
C. 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA
D. 56g铁与足量氯气反应,氯气共得到3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因是___________________________(用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)____(填“>”“<”或“=”)0.1 mol·L-1的NaOH溶液中由水电离出的c(H+)。
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):c(Na+)-c(A-)= __________mol·L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断室温下(NH4)2CO3溶液的pH____(填“>”“<”或“=”)7。
(5)将相同温度下相同浓度的以下四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列_____________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H(结构简式为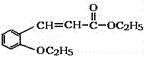 )是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,其合成路线如下:
)是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,其合成路线如下:
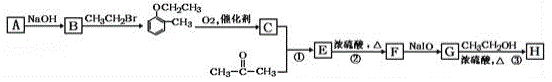
已知:①![]()
②
请回答下列问题:
(1)A的化学名称为_______________,G中所含官能团的名称是________________________;①和②的反应类型分别是______________、__________________。
(2)检验有机物A 中官能团的方法为__________________________________。
(3)高分子化合物M 的结构简式为__________________。
(4)反应③的化学反应方程式为__________________________________。
(5)有机物C 有多种同分异构体,其中属于芳香羧酸类的同分异构体有___________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水中的电离方程式:
①Ba(OH)2:________________________________________________;
②KAl(SO4)2:____________________________________________。
(2)写出下列物质发生水解的离子方程式:
①NaClO:________________________________________________________;
②FeCl3:_______________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com