
【题目】有机物H(结构简式为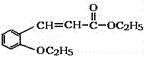 )是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,其合成路线如下:
)是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,其合成路线如下:
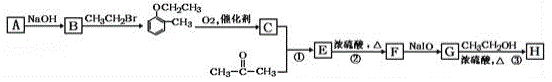
已知:①![]()
②
请回答下列问题:
(1)A的化学名称为_______________,G中所含官能团的名称是________________________;①和②的反应类型分别是______________、__________________。
(2)检验有机物A 中官能团的方法为__________________________________。
(3)高分子化合物M 的结构简式为__________________。
(4)反应③的化学反应方程式为__________________________________。
(5)有机物C 有多种同分异构体,其中属于芳香羧酸类的同分异构体有___________种。
【答案】 2﹣甲基苯酚或邻甲基苯酚 碳碳双键、羧基、醚键 加成反应 消去反应 取有机物A少许于试管中,滴加氯化铁溶液,溶液显紫色 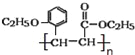
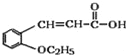 +CH3CH2OH
+CH3CH2OH![]()
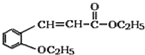 +H2O 14
+H2O 14
【解析】有机物A分子式为C7H8O,所以,A为邻甲基苯酚,与溴乙烷发生取代反应生成醚,根据信息可知,该有机物CH3CH2O-C6H5-CH3 中甲基被氧气氧化为醛基,变为有机物C:CH3CH2O-C6H5-CHO,然后该物质与丙酮发生加成反应变为羟基酮E,E在浓硫酸作用下,加热发生消去反应生成烯醛F,最后烯醛F被NaIO氧化为含有羧酸的有机物G,最后有机物G与乙醇发生酯化反应生成酯(H)。
(1)通过以上分析可知:A为含有羟基和甲基的芳香化合物,化学名称为邻甲基苯酚,通过有机物G的结构可知所含官能团的名称是碳碳双键、羧基、醚键;醛和酮发生加成反应生成含有羟基、酮羰基的有机物E,然后E在浓硫酸、加热条件下发生消去反应,正确答案:2﹣甲基苯酚或邻甲基苯酚;碳碳双键、羧基、醚键; 加成反应;消去反应。
(2)检验有机物A 中含有羟基,检验方法可用氯化铁溶液,溶液显紫色;或浓溴水,产生白色沉淀;正确答案:取有机物A少许于试管中,滴加氯化铁溶液,溶液显紫色。
(3)有机物H(结构简式为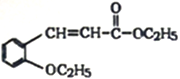 )是合成高分子化合物M的单体,所以有机物H通过加聚反应可以生成M,其结构简式为
)是合成高分子化合物M的单体,所以有机物H通过加聚反应可以生成M,其结构简式为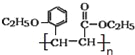 ;正确答案:
;正确答案: 。
。
(4)含有羧酸的有机物G,与乙醇在浓硫酸加热条件下发生酯化反应生成酯(H),方程式如下: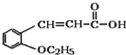 +CH3CH2OH
+CH3CH2OH![]()
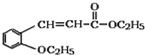 +H2O;正确答案:
+H2O;正确答案: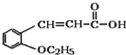 +CH3CH2OH
+CH3CH2OH![]()
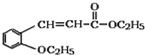 +H2O。
+H2O。
(5)有机物C 分子式为C9H10O2,属于芳香羧酸,一定含有-COOH,因此符合条件的有机物可能有:含有-CH2-CH2-COOH与苯环直接相连,有1种; 含有 -CH(CH3)-COOH与苯环直接相连,有1种; 苯环上连有1个-CH2COOH和1个 -CH3 ,共有3种; 苯环上连有1个-COOH和1个-CH2-CH3 ,有3种;苯环上连有1个-COOH和2个-CH3 ,有6种,最后共计有14种;正确答案:14。


科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,也常用于鱼类、肉类等食品的染色和防腐,易溶于水,微溶于乙醇. 某化学兴趣小组对亚硝酸钠进行多角度探究:
i.亚硝酸钠的制备
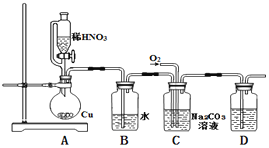
(1)实验中用恒压滴液漏斗,相比普通分液漏斗,显著的优点是____.
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为_______________。
ii. 探究亚硝酸钠与硫酸反应气体产物成分.
已知:①NO+NO2+2OH﹣═2NO2﹣+H2O ②气体液化的温度:NO2:21℃,NO:﹣152℃

(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是___________.
(4)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接):
A、C、______、______、______.
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体.
①确认A中产生的气体含有NO,依据的现象是_________________.
②装置B的作用是____________________.
iii. 设计实验证明酸性条件下NaNO2具有氧化性:___________。
供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下的a L氯化氢气体溶于100mL水中,得到的盐酸的密度为b g/mL,则该盐酸的物质的量的浓度是( ) mol/L
A. 10 a /22.4 B. 10 a /22.4(a +0.1)
C. ab/(22400+36.5a) D. 1000ab/(2240+36.5a)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将NO2与SO2以体积比1∶2置于恒容密闭容器中,发生如下反应:
NO2(g)+SO2(B)![]() NO(g)+SO3(g)△H=-41.8kJ·mol-1,能说明反应达到平衡状态的是( )
NO(g)+SO3(g)△H=-41.8kJ·mol-1,能说明反应达到平衡状态的是( )
A. 体系压强保持不变 B. 混合气体颜色保持不变
C. NO和SO3的物质的量之比保持不变 D. 每消耗1molNO2的同时生成1molSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁是一种具有芳香族性质的有机过渡金属化合物。二茂铁熔点是173℃,在100℃时开始升华,沸点是249℃,不溶于水,易溶于苯、乙醚、汽油、柴油等有机溶剂;化学性质稳定,400℃以内不分解。实验室制备二茂铁装置示意图如下图,实验步骤为:

①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a 中加入60mL 无水乙醚到三颈烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a 滴入5.5 mL 新蒸馏的环戊二烯(C5H6、密度0.95g/cm3),搅拌;
③将6.5g 无水FeCl2 与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25ml 装入仪器a中,慢慢滴入三颈烧瓶中,45min 滴完,继续搅拌45min;
④再从仪器a 加入25mL 无水乙醚搅拌;
⑤将三颈烧瓶中液体转入分液漏斗,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b 的名称是__________________,作用是_____________________。
(2)步骤①中通入氮气的目的是_____________________。
(3)三颈烧瓶的适宜容积应为__________ (填序号);①100ml、②250ml、③500ml;步骤⑤所得的橙黄色溶液的溶剂是_____________________。
(4)KOH、FeCl2、C5H 6反应生成二茂铁[Fe(C5H5)2]和KCl 的化学方程式为_____________________。
(5)二茂铁粗产品的提纯过程在上图中进行,其操作名称为________________。二茂铁及其衍生物可做抗震剂用于制无铅汽油,它们比曾经使用过的四乙基铅安全得多,其中一个重要的原因是_________________________________。
(6)最终得到纯净的二茂铁4.8g,则该实验的产率为___________________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某些共价键的键能如下表所示,火箭燃料肼(N2H4)的燃烧的热化学方程式是:N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣5 akJmol﹣1则O﹣H的键能为( )
共价健 | N﹣N | N﹣H | O=O | N≡N |
键能kJmol﹣1 | 3a | 2.5a | 4a | 8a |
A.2a kJmol﹣1
B.2.5a kJmol﹣1
C.3a kJmol﹣1
D.3.5a kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2(g) + 3H2(g)![]() 2NH3(g) ΔH = 92 kJ·mol-1,下图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度。下列说法中,不正确的是
2NH3(g) ΔH = 92 kJ·mol-1,下图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度。下列说法中,不正确的是

A.X表示温度
B.L2>L1
C.反应速率 υ(M)>υ(N)
D.平衡常数 K(M)>K(N)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单晶硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝,硼,磷等杂质).粗硅与氯气反应生成四氯化硅(反应温度450—500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。
氯气的制取:

(1)实验室用MnO2和浓盐酸制取氯气,若要制得干燥,纯净的氯气,所需装置的接口连接顺序是 ___(填小写字母)。
(2)写出实验室制取氯气的离子方程式:____ 。
(3)装置A中恒压分液漏斗M与常用分液漏斗相比,其优点是 _____,装置D的作用是____。
将上述方法制取的氯气通入下图装置中可以制得四氯化硅。
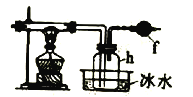
[资料]
a.四氯化硅遇水极易水解
b.硼、铝、铁,磷在高温下均能与氯气直接反应生成相应的氯化物
c.有关物质的熔沸点见下表:
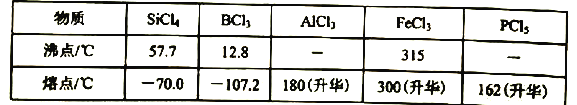
(4)装置f中盛放的药品是____,h瓶中左边用粗导管导出物质的目的是____。
(5)从b瓶得到的液体中蒸馏出SiCl4,所需用到的仪器是 ___。
A.容量瓶 B.温度计 C.冷凝管 D.分液漏斗
(6)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O 。某同学称取5.000 g残留物,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000 × 10-2 mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL,滴定终点的现象是____,残留物中铁元素的质量分数是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不能溶解于NaOH溶液的该衍生物共有 ( )
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com