
【题目】单晶硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝,硼,磷等杂质).粗硅与氯气反应生成四氯化硅(反应温度450—500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。
氯气的制取:

(1)实验室用MnO2和浓盐酸制取氯气,若要制得干燥,纯净的氯气,所需装置的接口连接顺序是 ___(填小写字母)。
(2)写出实验室制取氯气的离子方程式:____ 。
(3)装置A中恒压分液漏斗M与常用分液漏斗相比,其优点是 _____,装置D的作用是____。
将上述方法制取的氯气通入下图装置中可以制得四氯化硅。
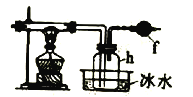
[资料]
a.四氯化硅遇水极易水解
b.硼、铝、铁,磷在高温下均能与氯气直接反应生成相应的氯化物
c.有关物质的熔沸点见下表:
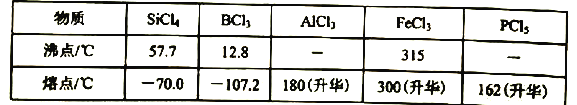
(4)装置f中盛放的药品是____,h瓶中左边用粗导管导出物质的目的是____。
(5)从b瓶得到的液体中蒸馏出SiCl4,所需用到的仪器是 ___。
A.容量瓶 B.温度计 C.冷凝管 D.分液漏斗
(6)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O 。某同学称取5.000 g残留物,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000 × 10-2 mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL,滴定终点的现象是____,残留物中铁元素的质量分数是_______。
【答案】 aedih MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 平衡气压,使液体顺利流下 除去氯气中的HCl气体 碱石灰 防止导管堵塞 BC 溶液变为红色,且半分钟内不褪色(或浅紫色等) 4.48%
Mn2++Cl2↑+2H2O 平衡气压,使液体顺利流下 除去氯气中的HCl气体 碱石灰 防止导管堵塞 BC 溶液变为红色,且半分钟内不褪色(或浅紫色等) 4.48%
【解析】(1)实验室用MnO2和浓盐酸制取氯气,生成的氯气中往往含有氯化氢和水蒸气,若要制得干燥,纯净的氯气,需要先用饱和的食盐水除去氯化氢,再用浓硫酸干燥,所需装置的接口连接顺序为aedih,故答案为:aedih;
(2)实验室制取氯气的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)装置A中恒压分液漏斗M与常用分液漏斗相比,其优点是可以平衡气压,使液体顺利流下,装置D中的饱和食盐水可以除去氯气中的HCl气体,故答案为:平衡气压,使液体顺利流下;除去氯气中的HCl气体;
(4) 四氯化硅遇水极易水解,装置f中盛放的药品可以是碱石灰,防止外界空气中的水蒸气进入h,根据表格数据,四氯化硅沸点较低,容易凝华,h瓶中左边用粗导管导出物质,可以防止导管堵塞,故答案为:碱石灰;防止导管堵塞;
(5)从b瓶得到的液体中蒸馏出SiCl4,所需用到的仪器有温度计、冷凝管、蒸馏烧瓶、酒精灯等,故选BC;
(6)用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,MnO4-转变成Mn2+溶液颜色有紫色变成无色,KMnO4标准溶液在酸性条件下进行氧化还原滴定时,不需要指示剂,判断是否达到滴定终点的方法为:当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色,利用关系式法计算:
5Fe2+~~~~~~~~~MnO4-
4×10-3mol 1.000×10-2molL-1×0.02L×![]()
铁元素的质量为:4×10-3mol×56g/mol=2.24×10-1g,铁元素的质量分数![]() ×100%=4.48%,故答案为:溶液变为红色,且半分钟内不褪色;4.48%。
×100%=4.48%,故答案为:溶液变为红色,且半分钟内不褪色;4.48%。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】若NA代表阿伏加德罗常数,下列说法正确的是( )
A. 46gNO2和N2O4的混合液中总原子数为3NA
B. 4℃时9mL水和11.2L氮气含有相同的分子数
C. 同温同压下,NA个CO2与NA个N2和O2的混合气体的体积不相等
D. 1.01×105Pa时,11.2 L氧气所含的原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H(结构简式为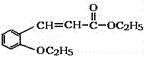 )是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,其合成路线如下:
)是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,其合成路线如下:
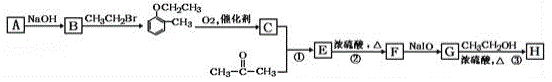
已知:①![]()
②
请回答下列问题:
(1)A的化学名称为_______________,G中所含官能团的名称是________________________;①和②的反应类型分别是______________、__________________。
(2)检验有机物A 中官能团的方法为__________________________________。
(3)高分子化合物M 的结构简式为__________________。
(4)反应③的化学反应方程式为__________________________________。
(5)有机物C 有多种同分异构体,其中属于芳香羧酸类的同分异构体有___________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米二氧化锆(ZrO2)是制备特种陶瓷(china)最重要的原料之一。由锆英石(主要成分为ZrSiO4)制备二氧化锆的工艺流程如图所示:
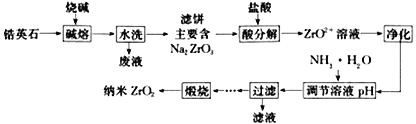
(1)写出“碱熔”时主要反应的化学方程式__________________________________。
(2)“水洗”所产生的“废液”主要成分为NaOH 和__________(填化学式),试写此成分的一种用途________________________________。
(3)写出“酸分解”生成ZrO2+反应的离子方程式__________________________________。
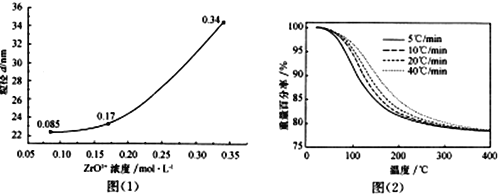
(4)根据图(1)分析ZrO2+浓度对ZrO2粒径的影响_____________________________________。
(5)ZrO2+溶液中常含有Fe3+(浓度为0.03mol·L-l),一般用草酸络合处理净化。若未净化处理直接加入氨水调节溶液pH,能否使ZrO2+完全转化为纯净的ZrO(OH)2沉淀,试通过计算说明。已知ZrO2+完全沉淀时浓度为1.0×10 -5 mol·L-l ,ZrO(OH)2、Fe(OH)3的Ksp分别为4.0×10-26、8.0×10-38, ![]() ≈3.16。__________________________________________________。
≈3.16。__________________________________________________。
(6)ZrO(OH)2煅烧制取纳米ZrO2时,升温速率与重量百分率之间的关系如图(2)所示。
煅烧时最佳升温速率为________________,理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想以N2和H2为反应物,以溶有X的稀盐酸为电解质溶液,制造出新型燃料电池,装置如图所示。下列说法正确的是
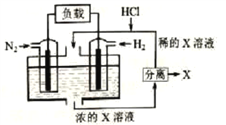
A. 放电时H+向左移动,生成的物质X是NH4Cl
B. 通入H2的一极为正极
C. 通入N2的电极反应为:N2+6H+-6e-=2NH3
D. 放电过程右边区域溶液pH逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用H2S废气制取H2的方法有利于环保。
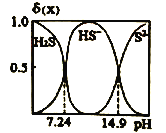
(l) H2S的电子式是____,H2S溶液中H2S、HS-,S2-的物质的量分数δ(X)随pH的变化如图所示,H2S的电离平衡常数ka1= ___________
![]()
(2)利用H2S废气制取H2的方法有多种。
①热化学硫碘循环法 已知循环反应如下:
H2S(g)+ H2SO4(aq)═S(s)+ SO2(g)+2 H2O(l)△H1=61 kJ/mol
SO2(g)+I2(g)+2 H2O(l)=2HI(aq)+ H2SO4(aq)△H2=-151 kJ/mol
2HI(aq)= H2(g)+ I2(g)△H3=110kJ/mol
写出硫化氢气体分解为氢气和固体硫的热化学方程式_____。
②高温热分解法
已知:H2S (g) =H2(g)+l/2S2(g)
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K_______(填“增大”、“减小”或“不变”)。若985℃时平衡常数K=0.04,则起始浓度c= ______mol/L 。
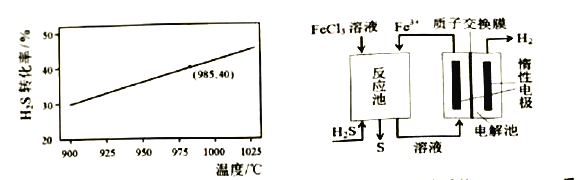
③电化学法 该法制氢过程的示意图如上图。循环利用的物质是____。反应池中化学反应方程式为______。电解池阳极电极反应式为____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水中的电离方程式:
①Ba(OH)2:________________________________________________;
②KAl(SO4)2:____________________________________________。
(2)写出下列物质发生水解的离子方程式:
①NaClO:________________________________________________________;
②FeCl3:_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制备气体时,若实验装置出现下图所示情况时,不漏气的是____


A. 装置甲用手握试管一段时间,再松开手
B. 装置乙放入CaCO3和稀盐酸,并关闭出气口活塞
C. 装置丙烧瓶内放入金属Zn和稀硫酸
D. 装置丁广口瓶中装有MnO2和H2O2,关闭出气口止水夹,打开分液漏斗活塞
(2)欲用萃取分液的方法在碘水中提取碘,一般可选用________为萃取剂,该操作中是否可改用乙醇萃取?________(填“是”或“否”),原因是_____________________。
分液漏斗使用前须________并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振摇并________后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先________,然后打开活塞放出下层液体,上层液体从上口倒出。
(3)分液后蒸馏提纯时,需要用到的玻璃仪器除了酒精灯、蒸馏烧瓶、温度计、牛角管、锥形瓶外,还有___________;蒸馏烧瓶加热时需加垫石棉网,瓶中液体需加沸石,若已开始加热,发现忘记加沸石,应进行______________操作;下列装置中温度计位置正确的是________,可能会导致收集到的产品中混有低沸点杂质的装置是________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com