
����Ŀ��H2��һ����Ҫ�������Դ��
��1����֪��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H2=-49.0kJmol-1
CH3OH(g)+H2O(g) ��H2=-49.0kJmol-1
CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H3=-41.1kJmol-1
CO2(g)+H2(g) ��H3=-41.1kJmol-1
H2��ԭ CO��Ӧ�ϳɼ״����Ȼ�ѧ����ʽΪ��CO(g)+2H2(g)![]() CH3OH(g) ��H1������H1��___kJmol-1���÷�Ӧ�Է����е�����Ϊ___
CH3OH(g) ��H1������H1��___kJmol-1���÷�Ӧ�Է����е�����Ϊ___
A������ B������ C���κ��¶�������
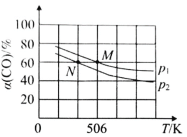
��2�����º�ѹ�£����ݻ��ɱ���ܱ������м��� 1molCO��2.2mol H2��������ӦCO(g)+2H2(g)![]() CH3OH(g)��ʵ����ƽ��ʱCO��ת�������¶ȡ�ѹǿ�ı仯��ͼ��ʾ����P1__P2���жϵ�������_____��
CH3OH(g)��ʵ����ƽ��ʱCO��ת�������¶ȡ�ѹǿ�ı仯��ͼ��ʾ����P1__P2���жϵ�������_____��
��3������Ӧ CO(g)+2H2(g)![]() CH3OH(g)���¶Ȳ���������㶨Ϊ1���ܱ������з�������Ӧ�����и����ʵ����ʵ�����ʱ��仯�����ʾ��
CH3OH(g)���¶Ȳ���������㶨Ϊ1���ܱ������з�������Ӧ�����и����ʵ����ʵ�����ʱ��仯�����ʾ��
ʱ��/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
�����и�������Ϊ�жϸ÷�Ӧ�ﵽƽ���־����____(����ĸ)��
A��������ѹǿ���ֲ��� B��2v��
C������������Է����������ֲ��� D�����������ܶȱ��ֲ���
������ʼѹǿΪP0 kPa�����ڸ��¶��·�Ӧ��ƽ�ⳣ��Kp=___(kPa)-2����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
�۷�Ӧ�������õ�λʱ���ڷ�ѹ�ı仯��ʾ����10min��H2�ķ�Ӧ����v(H2)=___kPamin-1��
���𰸡�-90.1 B > ����ӦΪ�����������С�ķ�Ӧ����ѹƽ�����ƣ�CO��ת����������ͼ֪��ͬ�¶�ʱP1��CO��ת���ʴ���P2 AC 9/p02 P0/30
��������
��1�����ݸ�˹��������֪����CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H2=-49.0kJmol-1����CO(g)+H2O(g)
CH3OH(g)+H2O(g) ��H2=-49.0kJmol-1����CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H3=-41.1kJmol-1����+�ڵã�CO(g)+2H2(g)
CO2(g)+H2(g) ��H3=-41.1kJmol-1����+�ڵã�CO(g)+2H2(g)![]() CH3OH(g) ��H1=(-49.0kJmol-1)+( -41.1kJmol-1)= -90.1 kJmol-1,���Դ˷�ӦΪ���ȷ�Ӧ���÷�Ӧ���µ��������Է����У���B��ȷ���𰸣� -90.1�� B��
CH3OH(g) ��H1=(-49.0kJmol-1)+( -41.1kJmol-1)= -90.1 kJmol-1,���Դ˷�ӦΪ���ȷ�Ӧ���÷�Ӧ���µ��������Է����У���B��ȷ���𰸣� -90.1�� B��
��2����ӦCO(g)+2H2(g)![]() CH3OH(g) ������Ӧ�����������С�ķ�Ӧ����������������ʱ������ѹǿ����ѧƽ�������ƶ���CO��ƽ��ת����������ͼʾ��֪��COת����P1>P2������ѹǿ��P1>P2���𰸣�>;����ӦΪ�����������С�ķ�Ӧ����ѹƽ�����ƣ�CO��ת����������ͼ֪��ͬ�¶�ʱP1��CO��ת���ʴ���P2 ��
CH3OH(g) ������Ӧ�����������С�ķ�Ӧ����������������ʱ������ѹǿ����ѧƽ�������ƶ���CO��ƽ��ת����������ͼʾ��֪��COת����P1>P2������ѹǿ��P1>P2���𰸣�>;����ӦΪ�����������С�ķ�Ӧ����ѹƽ�����ƣ�CO��ת����������ͼ֪��ͬ�¶�ʱP1��CO��ת���ʴ���P2 ��
��3����A����Ϊ��Ӧ CO(g)+2H2(g)![]() CH3OH(g)�������������ȵķ�Ӧ�����¶Ȳ���������㶨Ϊ1���ܱ������У���������ѹǿ���ֲ��� ��˵����Ӧ�ﵽƽ���ˣ���A��Ϊ�жϸ÷�Ӧ�ﵽƽ���־����A��ȷ��
CH3OH(g)�������������ȵķ�Ӧ�����¶Ȳ���������㶨Ϊ1���ܱ������У���������ѹǿ���ֲ��� ��˵����Ӧ�ﵽƽ���ˣ���A��Ϊ�жϸ÷�Ӧ�ﵽƽ���־����A��ȷ��
B����v��(H2)=2v��(CH3OH) ʱ������֤����Ӧ�ﵽƽ��״̬�ˣ�����B����Ϊ�жϸ÷�Ӧ�ﵽƽ���־����B����
C������������Է���������ֵ�ϵ���ƽ��Ħ���������͵������������������ʵ�������Ϊ�����ʶ������壬�������������䣬��ѧ��Ӧ�����������ȣ����Ե�ƽ��Ħ���������ֲ��䣬˵����Ӧ�ﵽ��ƽ��״̬����C��ȷ��
D�����������ܶ���=m/V,��Ϊm��V���ֲ��䣬���������䣬����ܶȲ��䣬����Ϊ�жϸ÷�Ӧ�ﵽƽ���־����D����
���Ա���𰸣�AC��
���ݷ�ӦCO(g)+2H2(g)![]() CH3OH(g)�����е����ݿ�֪10minʱ���ﵽƽ�⣬������ʵ���Ϊ��Ϊ��
CH3OH(g)�����е����ݿ�֪10minʱ���ﵽƽ�⣬������ʵ���Ϊ��Ϊ��
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
��ʼ�� 2 4 0
�仯�� 1 2 1
ƽ���� 1 2 1
���ݰ���٤�����ɣ�����ʼѹǿΪP0 kPa����ƽ��ѹǿΪ2/3P0������ƽ�ⳣ��Kp=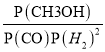 = (2/3P0��1/4)/[2/3P0��1/4��(2/3P0��1/2)2]= 9/p02,�𰸣�9/p02��
= (2/3P0��1/4)/[2/3P0��1/4��(2/3P0��1/2)2]= 9/p02,�𰸣�9/p02��
�۸���ͼ����֪������ʼѹǿΪ2/3P0��10min��ƽ��ѹǿΪ1/3P0����H2�ķ�Ӧ����v(H2)= 1/3P0��10min =1/30 P0kPamin-1,���Ա���𰸣�P0/30��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��������пհף�
��1��9gNH4+�����ʵ���Ϊ___�����к����ӵ���ĿΪ___������NA��ʾ��
��2��ͬ��ͬѹ�£�ͬ����İ����ͼ��������������Ϊ___��ͬ�����İ����ͼ�������������Ϊ___��
��3����֪24��A��40��Bǡ����ȫ��Ӧ����0.4molC��32��D����C��Ħ������Ϊ___��
��4��ij��������Ӫ��Һ�к���NH4+��Cl-�� K+�� SO42������ú�0.6mol/LNH4+��0.5mol/LCl-��0.5mol/LK+����SO42�������ʵ���Ũ��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ���Ͻ�(��������)����Ϊԭ�ϻ�������ͭ�Ĺ����������£�

����˵����ȷ����
A. ��ͭ���ڹ���ϡ���ᣬ���ˡ����¸���ô�ͭ
B. ���ʱ�ô�������������������ҺΪ�������Һ
C. ��ϡ���ᴦ������ʱ��Ҫ������������ԭ��Ӧ
D. ����ҺB�п�����ȡ�̷�(FeSO4��7H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���һͭ����ȼ�ϵ�������ߡ��ɱ��ͣ����й����ķ�չǰ�����õ��ͨ��һ�ָ��ӵ�ͭ��ʴ�����������������зŵ����Ϊ2Li+Cu2O+H2O==2Cu+2Li��+2OH��������˵������ȷ����

A. �ŵ�ʱ�������ĵ缫��ӦʽΪCu2O+H2O+2e��=2OH��+2Cu
B. �ŵ�ʱ������������������Li���ƶ�
C. ͨ����ʱ��ͭ�缫����ʴ���������Cu2O
D. ������Ӧ�����У�������ΪO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����һ���¶�����ͬ�������Һ�м���������ʱ�����ǿ��(I)�������ʼ�����(V)�ı仯���ߡ�(��������Һ������ڶ������֮��)����˵����ȷ���ǣ� ��
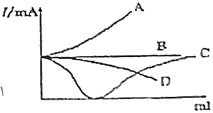
A.�������Һ����μ����Ũ�ȵİ�ˮ��ǡ����ȫ��Ӧ
B.��Ba(OH)2��Һ����μ����Ũ�ȵ�H2SO4������
C.��������Һ����μ����Ũ�ȵ�NaOH��Һ����
D.��ˮ�еμ�Ũ������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ͭ��Ũ��������ڼ��������·�����Ӧ����ѧ����ʽ���£�����ƽ����Cu+2H2SO4![]() CuSO4+A��+2H2O����ͨ����������������������⣺
CuSO4+A��+2H2O����ͨ����������������������⣺
��1���ڲμӷ�Ӧ�������У�����ԭ��������δ����ԭ����������ʵ���֮��Ϊ___��A���ʿ�����ǿ�Ӧ�����κ�ˮ����AӦ������___(����ĸ������д)��
A���� B������������ C���� D������� E���ǵ����
��2��һ������ͭƬ�뺬1.2mol��H2SO4��Ũ�����ַ�Ӧ(Ũ�������)������÷�Ӧ������ת����0.4mol���ӣ����ɵ�A�����ڱ���µ����Ϊ___L(��������ȫ���ݳ�)��
��3������2���з�Ӧ�����õ���Һϡ�ͺ���������Ba(OH)2��Һ��Ӧ�����ó���������Ϊ___g��д���˹����з�����Ӧ�����ӷ���ʽ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ�ص�һ��ͬλ��X��ԭ��������ΪA����N�����ӣ�����![]() ԭ�����HmX���ӣ���a��HmX���������ӵ����ʵ����ǣ� ��
ԭ�����HmX���ӣ���a��HmX���������ӵ����ʵ����ǣ� ��
A. ![]() (A-N+m)molB.
(A-N+m)molB. ![]() (A-N)molC.
(A-N)molC. ![]() (A-N)molD.
(A-N)molD. ![]() (A-N+m)mol
(A-N+m)mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(CrN)��һ�����õ���ĥ���ϣ�ʵ���ҿ�����ˮ�Ȼ���(CrCl3)�백���ڸ����·�Ӧ�Ʊ�����Ӧԭ��ΪCrCl3+NH3![]() CrN+3HCl.�ش��������⣺
CrN+3HCl.�ش��������⣺
(1)�Ʊ���ˮ�Ȼ������Ȼ����к�ǿ����ˮ�ԣ�ͨ�����Ȼ�������(CrCl3��6H2O)����ʽ���ڡ�ֱ�Ӽ�����ˮ�����õ�Cr2O3���йط�Ӧ�Ļ�ѧ����ʽΪ______________�����Ȼ��������Ʊ���ˮ�Ȼ����ķ�����_____________________________��
(2)�Ʊ���������ijʵ��С������Ʊ���������װ������ͼ��ʾ(�г������װ��ʡ��)��
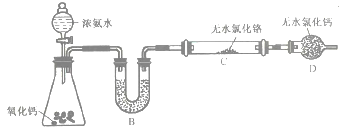
��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
��ʵ�鿪ʼʱ��Ҫ�ȴ�װ��A�л����������װ��C��Ŀ����___________________��
��װ��B��ʢ�ŵ��Լ���____________��װ��D��������_____________________��
����ͬѧ��Ϊ��װ����һ��ȱ�ݣ���ȱ����_______________________��
(3)�Ȼ����Ĵ��Ȳⶨ���Ƶõ�CrN�к���Cr2N���ʣ�ȡ��Ʒ14.38g�ڿ����г�ּ��ȣ��ù������(Cr2O3)������Ϊ16.72g������Ʒ��CrN����������Ϊ_____________(�������3λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͻ���������ͨ�����ȵ����ϳ�һ�ֿ�����������Ļ�����û���������б����ϵ�һ�Ȼ�����3�֣�1mol�û����������ʱ�������6mol�������ж����ֻ���������ǣ���ʾ����һ�������£�ȩ��Ҳ������H2�����ӳɷ�Ӧ���� ��
A. ![]() B.
B. ![]()
C. ![]() D.
D. 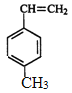
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com