
【题目】为更合理地表示溶液的酸碱性,科学家提出“酸度”(用AG表示)概念,AG=lg![]() 。下列叙述中正确的是( )
。下列叙述中正确的是( )
①任何温度下,纯水的AG等于0
②溶液的AG越小,酸性越强
③25 ℃时,0.1 mol·L-1盐酸的AG=12
④25 ℃时,某溶液的AG=-10,其pH=10
A.①③ B.②④
C.①② D.③④
科目:高中化学 来源: 题型:
【题目】
(1)计算需要NaOH固体质量 g。
(2)有以下仪器:①烧杯 ②药匙 ③250mL容量瓶 ④500mL容量瓶 ⑤玻璃棒⑥托盘天平 ⑦量筒。配制以上两种溶液必须使用的玻璃仪器 (填序号),还缺少的仪器是 。
(3)定容的具体操作方法是: 。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为 mL,如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。
(5)配制过程中,下列操作会引起结果偏高的是 (填序号)
①未洗涤烧杯、玻璃棒 ②称量NaOH的时间太长
③定容时俯视刻度 ④容量瓶不干燥,含有少量蒸馏水
⑤NaOH溶液未冷却至室温就转移到容量瓶 ⑥量取浓硫酸时,仰视量筒刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知N2(g) +3H2(g)![]() 2NH3(g) △H=-92.3kJ·mol-1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,达到平衡状态II,则下列说法正确的是________
2NH3(g) △H=-92.3kJ·mol-1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,达到平衡状态II,则下列说法正确的是________
A.两个平衡状态的平衡常数的关系:KI <KII
B.H2的百分含量相同
C.N2的转化率:平衡I <平衡II
D.反应放出的热量:QI=QII< 92.3 kJ
(2)若相同条件下,向第三个体积相同的密闭容器中充入一定量的N2、H2和NH3,要求反应从逆反应开始达到平衡,且平衡时氢气的体积分数仍为50%,则加入的氨气的物质的量的范围是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活、社会可持续发展密切相关。下列说法不正确的是( )
A.光化学烟雾是氮氧化物受紫外线照射后与空气中的一些碳氢化合物作用后生成的一种有毒烟雾
B.“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气
C.绿色化学的核心是应用化学原理对环境污染进行治理
D.航天飞机上使用的隔热陶瓷瓦,大多是以碳纤维做增强体的新型复合材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学遍及人们的生活、工作和生产。下列说法不正确的是( )
A.合成氨工业中使用的氮气来自于空气
B.可用热的纯碱溶液洗涤餐具上的油污
C.亚硝酸钠是一种食品防腐剂,使用时其用量可以不加限制
D.利用合适的催化剂可以将机动车尾气中的CO和NO转化为无害物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
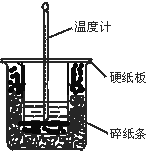
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验改用60 mL 0.50 mol· L-1盐酸跟50 mL 0.55 mol· L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热 (填“相等”“不相等”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL浓度为2mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
A.加入适量6 mol·L-1的盐酸 B.加入少量醋酸钠溶液
C.加热 D.加入少量金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_____________。
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL 煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________。
(4)丙组同学取10 ml 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl3溶液混合。分别取 2 mL 此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有______(填离子符号),由此可以证明该氧化还原反应为____________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是________________,生成沉淀的原因是________________(用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积为2 L的密闭容器中加入2 molA和3 molB,保持温度为30℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)![]() 3C(g),达到平衡后生成1.2 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol。
3C(g),达到平衡后生成1.2 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol。
请回答下列问题
(1)该反应的平衡常数K随温度升高而 (填“增大”、“减少”或“不变”),该反应的焓变△H 0(填“>”、“<”或“=”)。
(2)30℃时,平衡混合气中C的体积分数ω= ,A物质的转化率与B物质的转化率之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com