
【题目】H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示,下列说法正确的是( ) 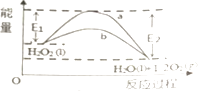
A.有MnO2条件下的反应曲线是a曲线
B.a曲线变为b曲线,反应的活化分子百分数增大
C.a曲线变为b曲线,平衡时H2O2的转化率增大
D.b曲线的热化学方程式为:H2O2(l)═H2O(l)+ ![]() O2(g)△H=﹣(E1﹣E2)KJmol﹣1
O2(g)△H=﹣(E1﹣E2)KJmol﹣1
【答案】B
【解析】解:A.催化剂降低反应活化能而改变反应速率,但不影响平衡移动,则焓变不变,所以有MnO2条件下的反应曲线是b曲线,故A错误;
B.催化剂降低反应所需活化能,导致活化分子百分数增大,b曲线中有催化剂,如果a曲线变为b曲线,反应的活化分子百分数增大,故B正确;
C.在双氧水的分解反应中,二氧化锰是正催化剂,增大反应速率但不影响平衡移动,所以双氧水转化率不变,故C错误;
D.该反应的焓变为△H=(E1﹣E2)KJmol﹣1或)△H=﹣(E2﹣E1)KJmol﹣1,故D错误;
故选B.
【考点精析】根据题目的已知条件,利用催化剂和化学平衡状态本质及特征的相关知识可以得到问题的答案,需要掌握催化剂的催化作用具有很强的选择性,某种催化剂往往只能催化某一种反应或某一类反应,使用生物酶制剂时的选择性更为突出;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】下列有关叙述或化学用语表示正确的是( )
A.S2﹣的结构示意图: ![]()
B.过氧化氢的电子式: ![]()
C.Ge原子的简化电子排布式:[Ar]4s24p2
D.氯化钠的分子式:NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色晶体,极微溶于水,不溶于醇类。可与水缓慢反应,易与酸反应。实验室通常用CaCl2在碱性条件下与H2O2反应制得(该反应剧烈并大量放热),装置如图所示,请回答下面的问题:
I.CaO2的制备

(1)漏斗在使用时其上口的玻璃塞应________(填“打开”或“关闭”),支管B的作用是________。
(2)将盛有浓CaCl2溶液的装置置于冰水混合物中。其原因是:使反应平稳进行、___________。
(3)加入H2O2与浓氨水的混合溶液,使反应开始。
①反应的化学方程式是_______________。
②滴加H2O2与浓氨水混合溶液之前,还应进行的操作是______。
(4)待反应结束后,经______(填操作)得CaO2粗产品。
Ⅱ.CaO2纯度的测定:将一定量的CaO2溶于稀硫酸,用标准KMnO4溶液滴定生成的H2O2(KMnO4反应后生成Mn2+),计算确定CaO2的含量。
(5)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定,所得的数据如下表所示,则样品的纯度__________。
实验序号 | ① | ② | ③ | ④ |
消耗KMnO4体积/mL | 19.98 | 20.02 | 20.20 | 20.00 |
(6)测得CaO2样品的纯度偏低,其原因可能是______(选填编号)。
A.烘烤时间不足
B.配制KMnO4标准溶液定容时俯视容量瓶刻度线
C.在洁净干燥的酸式滴定管中未润洗即装标准液
D.滴定前尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物是大气污染物,可以通过以下方法处理:
I.催化还原法:在汽车排气管上安装一个催化转化器,发生反应:
2NO(g) + 2CO(g) ![]() N2(g) + 2CO2(g) △H1
N2(g) + 2CO2(g) △H1
(1)已知:①N2(g) +O2(g)![]() 2NO(g) △H2=+180kJ/mol
2NO(g) △H2=+180kJ/mol
②CO与O2 反应相关的化学键键能数据如下:
化学键 | O=O | C=O | C≡O |
键能/(kJ/mol) | 497 | 803 | 1072 |
则△H1=__________。
(2)在一定温度下,向容积为1L的密闭容器中充入2 molNO、1molCO,10min时反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图1所示:
N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图1所示:
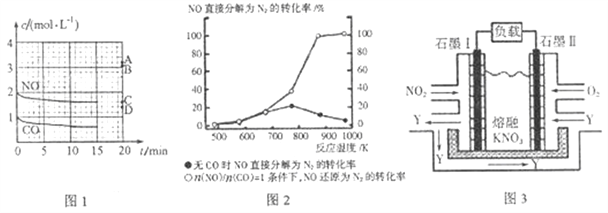
①该反应的平衡常数K=______(结果保留3位有效数字);前10min内用氮气表示的平均反应速率为______。
②若保持其他条件不变,15min时再向该容器中充入少量N2,则此时反应的v正______ v逆(填“>”、“=”或“<”),原因是____________。
③若保持其他条件不变,15min时压缩容器的容积至0.5L,20min时反应重新达到平衡,则此时NO的浓度对应的点应是图1中的______(填字母)。
④某科研小组研究发现以Ag-ZSM-5为催化剂,NO转化为N2的转化率随温度变化情况如图2 所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因是______。
II.利用电化学原理,将NO2、O2 和熔融KNO3制成燃料电池,其原理如图3。
(3)该电池在工作过程中NO2转变成绿色硝化剂Y,Y 是一种氧化物,可循环使用,石墨I附近发生的电极反应式为______。相同条件下,消耗的O2 和NO2 的体积比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由a、b、c、d四种金属按下表中装置进行实验。下列说法正确的是

A. 装置甲中化学能全部转化为电能
B. 装置乙中b电极发生的电极反应式为Cu2++2e-=Cu
C. 装置丙中SO42-向a电极移动,溶液的pH变小
D. 四种金属活动性由强到弱的顺序是b>e>d>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,不能与CO2发生反应的是( )。
①Na2O ②Na2O2 ③NaCl ④NaOH ⑤NaHCO3
A.①④B.②③C.③⑤D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是生命之源,它与我们的生活密切相关.在化学实验和科学研究中,水也是一种常用的试剂.
(1)写出与H2O分子互为等电子体的一种阴离子的化学式为 .
(2)水分子在特定条件下容易得到一个H+,形成水合氢原子(H3O+).下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)向CuSO4溶液中滴加氨水,先产生蓝色沉淀,然后沉淀溶解,溶液呈深蓝色.请写出生成配合离子的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中进行的可逆反应:2SO2(g)+O2(g) ![]() 2SO3(g),下列能判断该反应已经达到化学平衡状态的是( )
2SO3(g),下列能判断该反应已经达到化学平衡状态的是( )
A.SO2、O2、SO3的浓度相等
B.SO2、O2、SO3的浓度不再发生变化
C.SO2、O2、SO3在密闭容器中共存
D.反应停止,正、逆反应速率都等于零
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com