
【题目】下列化学反应的离子方程式中正确的是( )
A.盐酸与碳酸钙反应:CO32-+2H+=CO2↑+H2O
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3- =CaCO3↓+H2O
C.氯气溶于水:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
D.Ba(OH)2与稀H2SO4反应的离子方程式:H++OH-=H2O
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
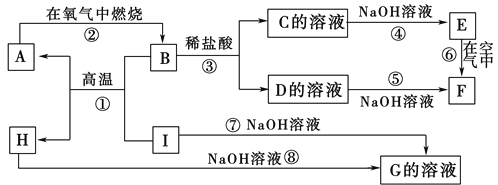
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________。
(2)反应①的化学方程式为_____________________________________
反应③的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________。
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究团队实现了电化学合成(又称电解合成)H2O2,该方法的原理如图所示,下列有关说法错误的是( )
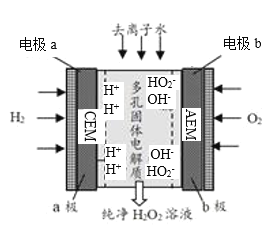
![]()
A.电极a为阳极,CEM为阳离子交换膜
B.该方法是一种制取H2O2的绿色方法
C.电极b上的电极反应式为O2+H+-2e-=HO2-
D.通过调节通入去离子水的量可以控制流出溶液中H2O2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.01NA
B.标准状况下,22.4L酒精含有的分子数为NA
C.在常温常压下,28gN2与CO混合物气体中所含的分子数目一定为NA
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售盐酸的总酸量(g/100mL)。
Ⅰ.实验步骤:
(1)用酸式滴定管取待测盐酸溶液20.00mL于锥形瓶中,向其中滴加2滴___作指示剂。
(2)读取盛装0.1000mol/LNaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为____mL。
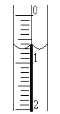
(3)滴定。当___时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(4)甲同学在处理数据时计算得:
平均消耗的NaOH溶液的体积V=(15.95+15.00+15.05+14.95)/4mL = 15.24mL。
指出他的计算的不合理之处:___。按正确数据处理,可得c(待测盐酸)=___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为( )
A. 2:1:2 B. 1:1:2 C. 2:2:1 D. 1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯原子对O3的分解有催化作用:
O3+Cl === ClO+O2 ΔH1
ClO+O === Cl+O2 ΔH2
大气臭氧层的分解反应是O3+O===2O2 ΔH,该反应的能量变化如图:
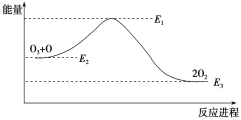
下列叙述中,正确的是( )
A. 反应O3+O===2O2的ΔH=E1-E3
B. O3+O===2O2是吸热反应
C. ΔH=ΔH1+ΔH2
D. 2O2===O3+O 是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1 ②N2H4(g)+O2(g)= N2(g)+2H2O(g) △H=-534kJ·mol-1下列关于肼和NO2反应的热化学方程式中,正确的是( )
A. 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l) △H= -1135.7kJ·mol-1
B. 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H= -1000.3kJ·mol-1
C. N2H4(g)+NO2(g)= ![]() N2(g)+2H2O(l) △H= -500.15kJ·mol-1
N2(g)+2H2O(l) △H= -500.15kJ·mol-1
D. 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H= -1135.7kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com