
【题目】碳、氮及其化合物在工农业生产、生活中有着重要的作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·molˉ1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
同一条件下,若2molCH4 还原NO2 至N2,生成气态水和二氧化碳。整个过程中放出的热量为1734kJ,则ΔH2=__________;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应为:Fe2O3(s)+3CH4(g)![]() 2Fe(s)+3CO(g)+6H2(g) ΔH>0。
2Fe(s)+3CO(g)+6H2(g) ΔH>0。
①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为_______。
②若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是_____(填序号)。
A.CH4的转化率等于CO的产率
B.混合气体的密度保持不变
C.速率:2v(CO)=v(H2)
D.固体的总质量保持不变
③该反应达到平衡时某物理量随温度变化如图所示,当压强由P1升高到P2时,平衡常数KA___KB(填“>”、“<”或“=”)。纵坐标可以表示的物理量有哪些______。(填序号)

A.H2的逆反应速率
B.CH4的的转化率
C.混合气体的平均相对分子质量
D.CO的体积分数
(3)甲酸是易溶于水的一元弱酸。
①常温下,将1L 0.1mol/L HCOOH溶液与1L0.1mol/LNaOH溶液混合后,下列关系不正确的是____(填序号)。
a.c(H+)水·c(OH-)水=1×10-14 b.2c(H+)+c(HCOOH)=2c(OH-)+c(HCOO-)
c.c(Na+)=c(HCOOH)+c(HCOO-) d.c(HCOO-)>c(Na+)>c(H+)>c(OH-)
②向1L 0.1mol/L HCOONa溶液中加水稀释后,c(HCOOH)/c(HCOO-)的数值______(填“增大”“减小”或“不变”)。
【答案】 -1160kJ·mol-1 0.012 mol/(L·min) bd = ac ac 增大
【解析】(1)将两个热化学方程式叠加,可得总反应方程式:2CH4(g) + 4NO2(g) = 2N2(g)+2CO2(g) + 4H2O(g) ΔH=ΔH1+ΔH2=-1734 kJ/mol,-574 kJ/mol+ΔH2=-1734 kJ/mol,解得ΔH2=-1160kJ/mol。(2)①Δn(Fe2O3)= 3.2g÷160g/mol=0.02mol,则根据反应方程式中物质反应的关系可知Δn(CO)= 3Δn(Fe2O3)=0.06mol,用CO表示的化学反应速率是V(CO)= 0.06mol÷5L÷1min=0.012mol/(L·min)。②a.根据碳元素守恒可知:在任何时刻都存在CH4的转化率等于CO的产率,因此不能据此判断反映是否处于平衡状态,错误;b.由于Fe、Fe2O3都是固体物质,若反应未达到平衡状态,则气体的质量就会发生改变,混合气体的密度也会发生改变,因此可以利用混合气体密度不变来判断反应处于平衡状态,正确;c.由于H2、CO都是生成物,任何时刻二者的速率比都等于方程式的计量数的比。故不能根据v(CO)与v(H2)的比值不变判断反应处于平衡状态,错误;d.若反应未达到平衡状态,则固体的质量就会发生改变,因此可以根据固体的总质量不变来判断反应处于平衡状态,正确。答案选bd。③平衡常数只与温度有关系,当压强由P1升高到P2时,平衡常数KA=KB。a.增大压强,化学反应速率加快,因此可能表示H2的逆反应速率,a正确;b.正反应体积增大,增大压强平衡向逆反应方向进行,甲烷的降低,b错误;c. 正反应体积增大,增大压强平衡向逆反应方向进行,所以混合气体的平均相对分子质量增大,c正确;d. 正反应体积增大,增大压强平衡向逆反应方向进行,CO的体积分数减小,d错误,答案选ac;(3)①常温下,将1L 0.1mol/L HCOOH溶液与1L0.1mol/LNaOH溶液混合后得到甲酸钠溶液,则a.温度不变,水的离子积常数不变,即c(H+)水·c(OH-)水=1×10-14,a正确;b.根据质子守恒c(H+)+c(HCOOH)=c(OH-),b错误;c.根据物料守恒可知c(Na+)=c(HCOOH)+c(HCOO-),c正确;d.甲酸钠水解,溶液显碱性,则c(Na+)>c(HCOO-)> c(OH-)>c(H+),d错误,答案选ac;②向1L 0.1mol/L HCOONa溶液中加水稀释后常见水解,c(HCOOH)/c(HCOO-)的数值增大。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】丁子香酚可用于配制康乃馨型香精及制作杀虫剂和防腐剂,结构简式如图。

(1)丁子香酚分子式为______________。
(2)下列物质在一定条件下能跟丁子香酚反应的是___________。
a.NaOH溶液 b.NaHCO3溶液 c.FeCl3溶液 d.Br2的CCl4溶液
(3)符合下述条件的丁子香酚的同分异构体共有____________种,写出其中任意任一种结构简式___________。
①与NaHCO3溶液反应
②苯环上只有两个取代基
③苯环上的一氯取代物只有两种
(4)丁子香酚的某种同分异构体A可发生如下转化(部分反应条件已略去)。
提示:RCH=CHR′![]() RCHO+R′CHO
RCHO+R′CHO
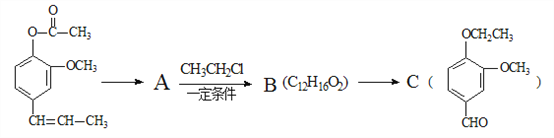
A→B的化学方程式为_______________________,C中滴加少量溴水振荡,主要现象为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法、乙醚浸取法的主要工艺为:

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是__________;
(2)操作Ⅰ需要的玻璃仪器主要有:烧杯、玻璃棒、__________,操作Ⅱ的名称是__________;操作Ⅲ的名称是__________;
(3)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定青蒿素分子式的装置。

①按上述所给的测试信息。装置的连接顺序应是__________(每个装置限用一次)。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是__________;
③青蒿素样品的质量为28.2 g。用合理改进后的装置进行试验,称得A管增重66 g,B管增重19.8 g,则测得青蒿素的最简式是__________。
④要确定该有机物的分子式,还必须知道的数据是__________。
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是__________(填字母代号)
A.乙醇 B.乙酸 C.葡萄糖 D.乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种常用的学习用品——圆规的材料组成:

(1)圆规含有的金属单质是___________(填化学式),请写出它在氧气中燃烧的化学方程式____________。
(2)这些材料中属于有机合成材料的是_________(填序号)。
(3)铅笔芯的主要成分是_________,请写出它的另一种用途_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠及其化合物具有广泛的用途。
(1)工业上制备碳酸氢钠的化学方程式为____________。
(2)用Na2CO3熔融作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示,正极的电极反应式为__________。

(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是_______,根据表中数据,浓度均为0.01 mol·L-1下列四种酸的溶液分别稀释100倍,pH变化最大的是_______(填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当100 mL 2mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH<7,则溶液中各离子浓度由大到小的顺序为_______。
②常温下,已知Ksp[Cu(OH)2]=2×10-20, Ksp[CuS]=1.3×10-36。向浓度为0.1mol/L,体积为10mL的氢氧化钠溶液中,逐滴加入浓度为0.1mol/L 硫酸铜溶液至pH=6时Cu2+的浓度为______。向该溶液中滴入一滴0.1mol/L的硫化钠溶液,_______(填“有”或“没有”)CuS沉淀析出。(一滴约为0.05mL)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知锶与钙同主族,下列对锶及其化合物的叙述正确的是
A. 碳酸锶难溶于水 B. 氢氧化锶的碱性比氢氧化钙弱
C. 单质锶跟冷水不反应 D. 锶是第四周期元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com