
【题目】下列物质中仅含有非极性共价键的是
A.H2OB.N2C.H2SD.MgCl2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2 , 该反应的化学方程式是 .
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3 . .
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:将B中反应后的固体溶解于水 ![]() 白色沉淀
白色沉淀 ![]() 仍有部分白色沉淀不溶解,证明有Na2SO4生成
仍有部分白色沉淀不溶解,证明有Na2SO4生成
上述方案是否合理? . 请简要说明两点理由:
①;② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
(1)【提出猜想】
猜想1:
猜想2:
猜想3:
为了验证猜想,该小组设计实验加以探究.
【实验探究】该小组同学按如图所示装置,将气体从a端通入,则;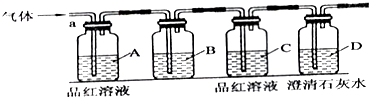
(2)B中应该装试剂(填编号).
A.氢氧化钠溶液
B.酸性高锰酸钾溶液
C.饱和碳酸钠溶液
D.饱和碳酸氢钠
(3)A中品红溶液的作用是 .
(4)D中澄清石灰水的作用是 .
(5)通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
【得出结论】由上述现象该小组同学确认该气体为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a g镁铝合金投入xmL,2mol/L的盐酸中,金属完全溶解,再加入ymL,1mol/L NaOH溶液,沉淀达到最大值,质量为(a+1.7)g,则下列说法不正确的是( )
A.镁铝合金与盐酸反应转移电子数为0.1NA
B.沉淀为Mg(OH)2和Al(OH)3混合物
C.x=2y
D.a的取值范围为0.9g<a<1.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物是棕红色、易潮解,100℃左右时升华.下图是两个学生设计的实验装置、左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示.试回答: 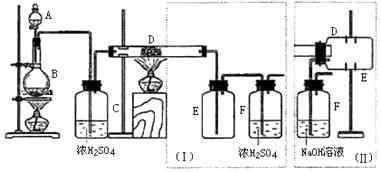
(1)B中反应的化学方程式为:;
(2)D中的反应开始前,需排除装置中的空气,应采取的方法是: .
(3)D中反应化学方程式为: .
(4)装置(Ⅰ)的主要缺点是: .
(5)装置(Ⅱ)的主要缺点是: . 如果选用此装置来完成实验,则必须采取的改进措施是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=+890 kJmol﹣1
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890 kJmol﹣1
C.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890 kJmol﹣1
D.2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=﹣890 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
已知:A、B、C、D四种元素,原子序数依次增大。A是短周期元素中金属性最强的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素。试回答下列有关问题:
(1)写出D元素价电子的电子排布式。
(2)D可形成化合物[D(H2O)6](NO3)3。
①[D(H2O)6](NO3)3中阴离子的立体构型是。NO3中心原子的轨道杂化类型为。
②在[D(H2O)6]3+中D3+与H2O之间形成的化学键称为 , 1 mol [D(H2O)6] 3+中含有的σ键有mol。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中(填化学式)为非极性分子。另一种物质的电子式为。
(4)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的剖面图: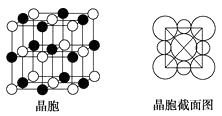
晶胞中距离一个A+最近的C有个,这些C围成的图形是;若晶体密度为ρ g·cm3 , 阿伏加德罗常数的值用NA表示,则A+的离子半径为cm(用含NA与ρ的式子表达)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com