
【题目】Na2O2是一种常见的过氧化物,具有强氧化性和漂白性。 通常可用作漂白剂和呼吸面具中的供氧剂。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:
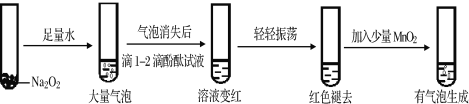
①用化学方程式解释使酚酞试液变红的原因_______________________,
依据实验现象推测红色褪去的原因是_________________。
②加入MnO2反应的化学方程式为________________________。
③ Na2O2的电子式为_____________
(2)实验小组两名同学共同设计如下装置探究过氧化钠与二氧化硫的反应。通入SO2,将带余烬的木条插入试管C中,木条复燃。
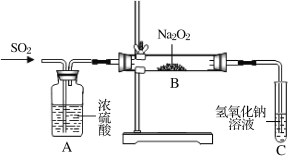
请回答下列问题:
①甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是____。
检验反应后B中的白色固体含有Na2SO3的方法是_________________。
②乙同学认为反应的后B中有Na2SO3还会有Na2SO4。乙同学猜想的理由是:_____。
为检验产物中Na2SO4的存在,乙同学设计并实施了如下实验方案:
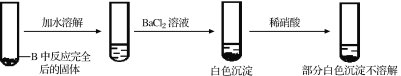
甲同学认为该实验方案的现象不能证明有Na2SO4生成,其理由为_______。
③ 测定B中反应完全后的固体中Na2SO4含量的实验方案:称取样品a 克加水溶解,_______,烘干,称量得BaSO4沉淀b 克,则Na2SO4的质量分数为____(列出计算式即可)。
【答案】2Na2O2 +2H2O = 4 NaOH +O2↑ 反应生成的H2O2具有漂白作用 2H2O2 ![]() 2H2O +O2↑
2H2O +O2↑ ![]() 2Na2O2 + 2SO2 = 2 Na2SO3 +O2 取反应B中的白色固体少许,滴入稀硫酸,生成无色能使品红溶液褪色的气体,说明含Na2SO3 过氧化钠具有强氧化性,二氧化硫有较强的还原性 稀硝酸能将亚硫酸钡氧化为硫酸钡 加盐酸酸化的氯化钡溶液,过滤,洗涤 142b/233a
2Na2O2 + 2SO2 = 2 Na2SO3 +O2 取反应B中的白色固体少许,滴入稀硫酸,生成无色能使品红溶液褪色的气体,说明含Na2SO3 过氧化钠具有强氧化性,二氧化硫有较强的还原性 稀硝酸能将亚硫酸钡氧化为硫酸钡 加盐酸酸化的氯化钡溶液,过滤,洗涤 142b/233a
【解析】
(1)①过氧化钠和水反应生成氢氧化钠是碱,碱遇酚酞变红;红色褪去的可能原因是过氧化钠和水反应生成的过氧化氢具有氧化性;
②过氧化氢在二氧化锰做催化剂分解生成水和氧气;
③ Na2O2属于离子化合物,含有O22-离子,据此写出电子式。
(2)①根据反应物和生成物写出方程式,根据得失电子数相等配平方程式;要证明白色固体中含有Na2SO3只需检验出含有SO32-就可以了;
②根据过氧化钠具有强氧化性,二氧化硫有较强的还原性,两者发生氧化还原反应生成Na2SO4;硫酸钠和亚硫酸钠均有氯化钡反应生成沉淀,亚硫酸钡加硝酸时氧化生成硫酸钡,不能说明是否含硫酸钡;
③利用亚硫酸钡易溶于盐酸,硫酸钡不溶分析判断;根据沉淀硫酸钡的质量计算硫酸钡的物质的量,进一步求出硫酸钠的质量,最后计算Na2SO4的质量分数。
(1)①过氧化钠和水反应生成氢氧化钠是碱,碱遇酚酞变红,反应方程式为2Na2O2 +2H2O = 4 NaOH +O2↑,红色褪去的可能原因是过氧化钠和水反应生成的过氧化氢具有氧化性,能氧化有色物质,
因此,本题正确答案是:2Na2O2 +2H2O = 4 NaOH +O2↑;反应生成的H2O2具有漂白作用;
②过氧化氢在二氧化锰做催化剂分解生成水和氧气,反应的化学方程式为:2H2O2 ![]() 2H2O +O2↑,
2H2O +O2↑,
因此,本题正确答案是:2H2O2 ![]() 2H2O +O2↑;
2H2O +O2↑;
③ Na2O2属于离子化合物,含有O22-离子,电子式为![]() ;
;
(2)①Na2O2与SO2反应生成了Na2SO3和O2,结合得失电子守恒知,该反应方程式为:2Na2O2 + 2SO2 = 2 Na2SO3 +O2,要证明白色固体中含有Na2SO3只需检验出含有SO32-就可以了,则取反应生成白色固体少许,滴入稀硫酸,生成无色气体使品红溶液褪色,说明含Na2SO3,
因此,本题正确答案是:2Na2O2 + 2SO2 = 2 Na2SO3 +O2;取反应生成白色固体少许,滴入稀硫酸,生成无色气体使品红溶液褪色,说明含Na2SO3;
②因为过氧化钠具有强氧化性,二氧化硫有较强的还原性,两者发生氧化还原反应生成Na2SO4;由实验流程可以知道,稀硝酸具有强氧化性,它也会将亚硫酸钡氧化为硫酸钡,最终也生成硫酸钡沉淀,则不能说明反应的后B中有Na2SO3还会有Na2SO4,
因此,本题正确答案是:过氧化钠具有强氧化性,二氧化硫有较强的还原性;稀硝酸能将亚硫酸钡氧化为硫酸钡;
③因为亚硫酸钡易溶于盐酸,硫酸钡不溶,所以测定B中反应完全后固体组成的实验方案为称取样品a克加水溶解,加盐酸酸化的氯化钡溶液,过滤,洗涤烘干,称量沉淀质量为b克,计算含量;
b克BaSO4的物质的量为![]() mol,则样品中含Na2SO/span>4的质量为
mol,则样品中含Na2SO/span>4的质量为![]() mol
mol![]() 142g/mol=
142g/mol=![]() g,所以Na2SO4的质量分数为142b/233a,
g,所以Na2SO4的质量分数为142b/233a,
因此,本题正确答案是:加盐酸酸化的氯化钡溶液,过滤,洗涤;142b/233a。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有机物的结构简式可以用“键线式”表示,其中线表示键,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。已知利用某些有机物之间的转化可贮存太阳能,如降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应为 (反应吸热),下列叙述中错误的是( )
(反应吸热),下列叙述中错误的是( )
A. NBD和Q互为同分异构体
B. Q可使溴水褪色
C. Q的一氯代物只有3种
D. NBD的同分异构体可以是芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应。硼与氯气反应生成三氯化硼(BCl3),生成的三氯化硼遇水水解产生白雾(已知:BCl3的熔点为-107.3℃,沸点为12.5℃ ),且三氯化硼用于制取乙硼烷(B2H6)。某兴趣小组设计如图所示装置制备三氯化硼。
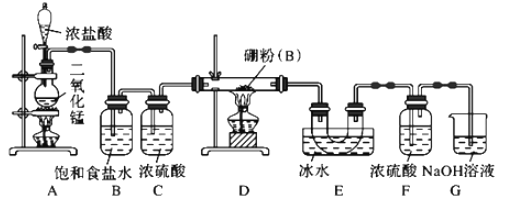
回答下列问题:
(1)装置A中发生反应的离子方程式为_____________________________。
(2)装置B中的作用是________________,装置E的作用是______________________。
(3)装置D中发生反应的化学方程式为______________________________________。
(4)装置F的作用是________________,可以用一个盛装________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3->I-,氧化性IO3->I2。在含3mol NaHSO3的溶液中逐滴加人KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是
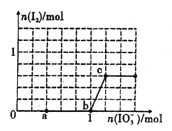
A. 0-a段发生反应:3HSO3-+IO3-=3SO42-+I-+3H+
B. a~b段共消耗NaHSO3的物质的量为1.8mol
C. b~c段反应:氧化产物为I2
D. 当溶液中I-与I2的物质的量之比为5 : 1时,加入的KIO3为1.lmol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;V和Z元素原子的最外层都只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子的L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。
回答下列问题:
(1)V的一种核素中质子数为中子数的![]() ,则该核素的名称为________,常用于制造________。
,则该核素的名称为________,常用于制造________。
(2)W元素在周期表中的位置为_______________________________。
(3)X元素的离子结构示意图为________。
(4)Z的最高价氧化物对应水化物的化学式为:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向恒温恒压容器中充入2 mol NO、1 mol O2,发生反应:2NO(g)+O2(g) ![]() 2NO2(g)。下列情况不能说明反应已达到平衡状态的是( )
2NO2(g)。下列情况不能说明反应已达到平衡状态的是( )
A. 容器体积不再改变 B. 混合气体的颜色不再改变
C. 混合气体的密度不再改变 D. NO与O2的物质的量的比值不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晋朝人常璩在《华阳国志》里有这样一段话:临邛县“有火井,夜时光映上昭。民欲其火,先以家火投之。顷许如雷声,火焰出,通耀数十里。以竹筒盛其火藏之,可拽行终日不灭也……”,请回答下列问题。
(1)话中描述的物质是一种最简单有机物甲烷,其分子的结构式为_______。
(2)写出“顷许如雷声,火焰出”涉及的化学反应方程式:_____________________。
(3)下列有关甲烷的说法正确的是________(填选项字母)。
A.它属于化石能源
B.它的分子中含有非极性键
C.它的分子中所有原子的最外层都达到了8电子稳定结构
D.(2)中反应发生时伴随有旧极性键的断裂和新极性键的形成
(4)甲烷不仅可以直接用来燃烧,还是重要的化工原料,它可以与水在高温条件下反应制得水煤气(CO和H2),反应的化学方程式为__________________,反应得到的水煤气中CO和H2的质量比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL 0.1 mol·L-1 NaOH溶液中加入 0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度:a > b,且a点所示溶液中由水电离出的c(OH-)=10-8.7mol/L
C. pH=7时溶液中c(HA)>c(Na+)=c(A-)> c(H+)=c(OH-)
D. b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com