
【题目】下列实验操作可以达到实验目的的是( )
A.用10mL量筒量取5.60mL浓硫酸
B.用托盘天平称量5.85g NaCl
C.将容量瓶放在烘箱中烘干
D.在烧杯中溶解固体药品时用玻璃棒搅拌
科目:高中化学 来源: 题型:
【题目】下列实验操作或事故处理正确的是( )
A.利用溶于水后“过滤”操作能分离NaCl和Ba(OH)2
B.实验结束后,用嘴吹灭酒精灯
C.皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗
D.稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】危险化学药品的包装标签上印有警示标志,下列化学药品名称与警示标志对应正确的是( )
A.汽油—易燃品B.浓硫酸—易爆品
C.酒精—剧毒品D.浓硝酸—放射性物品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成。
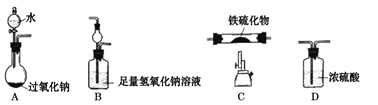
[实验步骤]
(1)组装仪器:上述四个装置的正确连接顺序为____;
(2)检査装置气密性:应如何操作?____;
(3)加入药品,开始实验:应先____,一段时间后再____;
(4)停止反应:当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O2,其目的是____;
(5)测定S元素的质量:将B中所得溶液加水配制成250 mL溶液,取25.00 mL所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为2.33g。之前所取铁硫化物得质量为6g,则FexSy的化学式为____;
[实验反思与再探究]
(6)有同学认为步骤(5)可以设计为:取25.00 mL所配溶液,加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称得BaSO3沉淀的质量。你认为此方案____(填“是”或“否”)合理,理由是____。
(7)有同学为了继续探究反应后硬质玻璃管中固体的成分,他将固体取出,完全溶于稀硫酸中,再向溶液中加入K3Fe(CN)6溶液,未观察到明显现象,则硬质玻璃管中所发生反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应: ![]() +
+ ![]()
![]()
![]() 如果要合成化合物A,其结构为:
如果要合成化合物A,其结构为: ![]() 下列说法不正确的是( )
下列说法不正确的是( )
A.化合物A和HBr 按照物质的量1:1加成时,有三种不同的产物
B.该反应的原理是加成反应
C.合成A的原料可能是:丙炔和2,3﹣二甲基﹣1,3﹣丁二烯
D.合成A的原料可能是:2﹣丁炔和2﹣甲基﹣1,3﹣丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5 , 反应PCl5(g)PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据见表:下列说法正确的是( )
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50s的平均速率v(Cl2)=0.0016 molL﹣1min﹣1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 molL﹣1 , 则该反应的△H<0
C.温度为T时,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2 , 反应达到平衡前v(正)<v(逆)
D.温度为T时,起始时向容器中充入0.5 mol PCl3和0.5 mol Cl2 , 达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂D.海域天然气水合物试采连续60天
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com