
【题目】用NA代表阿伏加德罗常数的数值。下列说法中,正确的是( )
A.2.3g金属钠由原子完全变成离子时,得到的电子数为0.1NA
B.0.2NA个硫酸分子与19.6磷酸(H3PO4)含有相同的氧原子数
C.28g氮气所含的原子数为NA
D.NA个氧气分子与NA个氢气分子的质量比为8∶1
科目:高中化学 来源: 题型:
【题目】I.(1)三种弱酸HA、H2B、HC,电离平衡常数的数值为1.8×10-5、5.6×10-11、4.9×10-10、4.3×10-7(数据顺序已打乱),已知三种酸和它们的盐之间能发生以下反应:
① HA + HB- (少量)=A-+ H2B,② H2B(少量) + C-=HB-+ HC,③ HA(少量) + C-=A-+ HC 。
则三种酸对应的电离平衡常数分别为(请在下面填空):________
HA | H2B | HC | ||
Ka | Ka1 | Ka2 | Ka3 | Ka4 |
数值 | ||||
(2)常温下0.1 mol/L CH3COOH溶液加水稀释过程,下列表达式数据一定变小是________。
A.c(H+) B.n(H+) C. c(CH3COO-)/ c(H+) D.c(CH3COOH)/c(H+)
II.工业废水中常含有一定量的Cr2O72- 和CrO42-,它们会对人体及生态系统产生很大的伤害,必须进行处理。还原沉淀法是常用的一种方法。

(1)转化过程中存在平衡2CrO42- + 2H+![]() Cr2O72- + H2O能说明反应到达平衡状态的是____。
Cr2O72- + H2O能说明反应到达平衡状态的是____。
A.CrO42-和Cr2O72-的浓度相同 B.ν正(Cr2O72-)=2 ν逆(CrO42-)
C.溶液的pH值保持不变 D.溶液颜色保持不变
(2)若1 L转化后所得溶液中含铬元素质量为28.6 g,CrO42- 有10/11转化为Cr2O72-(已知铬元素相对原子质量为52)。
① 转化后所得溶液中c(Cr2O72-)=_________________。
② 已知:常温下该反应的平衡常数K=1014,上述溶液转化后H+的物质的量浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中说明氢气作为燃料的优点的是( )
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境
③氢气是一种再生能源 ④燃烧时放出大量热量
A. ①②③B. ①②④C. ①③④D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.5L的NaCl溶液中含有0.5molNa+。下列关于该溶液的说法不正确的是( )
A. 该溶液中溶质的物质的量浓度为1 mol·L-1
B. 该溶液中含有58.5gNaCl
C. 配制1000mL该溶液需用58.5gNaCl
D. 量取100mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A.乙醇与钠反应生成乙醇钠
B.乙烯燃烧生成二氧化碳和水
C.乙烯与氯化氢反应生成氯乙烷
D.乙醇与乙酸反应生成乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A. 含有NA个氧原子的氧气在标准状况下的体积约为22.4 L
B. 2 L 0.3 mol·L-1的硫酸钾溶液中钾离子浓度为0.6 mol·L-1
C. 常温常压下,32 g O2和O3的混合气体所含原子数为2NA
D. 25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,现有![]() ;
;![]() 个HCl分子;
个HCl分子;![]() ;
;![]()
![]() ,对这四种气体的关系有以下四种表述:其中正确的是 ______ .
,对这四种气体的关系有以下四种表述:其中正确的是 ______ .
a.体积:![]()
b.物质的量:![]()
c.质量:![]()
d.氢原子个数:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取并制备碳酸锂,可以提高海水的综合利用价值,满足工业上对碳酸锂的需求。制备碳酸锂的一种工艺流程如下:

已知:①海水中某些离子浓度如下:
离子 | Li+ | Mg2+ | Ca2+ | Mn2+ | Cl- |
浓度(mol/L) | 0.113 | 0.049 | 0.001 | 0.010 | 0.501 |
②碳酸锂的溶解度:
温度(℃) | 0 | 10 | 30 | 50 | 70 | 90 |
溶解度(g/L) | 1.54 | 1.43 | 1.25 | 1.08 | 0.91 | 0.83 |
![]() 几种难溶电解质的溶度积(25℃):
几种难溶电解质的溶度积(25℃):
物质 | Li2CO3 | MgCO3 | MnCO3 | CaCO3 | Mg(OH)2 |
Ksp | 2.5×10-2 | 6.8×10-6 | 2.3×10-11 | 2.8×10-9 | 6×10-10 |
请回答下列问题:
![]() 精制除杂阶段的滤渣为MgCO3、______
精制除杂阶段的滤渣为MgCO3、______![]() 写化学式
写化学式![]()
![]() 用HCl调pH为4~5的目的是_________。
用HCl调pH为4~5的目的是_________。
![]() 二次除镁过程中,若使Mg2+浓度为6×10-4mol/L,应控制pH为______。
二次除镁过程中,若使Mg2+浓度为6×10-4mol/L,应控制pH为______。
![]() 沉锂阶段,实际测得不同纯碱加入量条件下的碳酸锂沉淀结果如下表:
沉锂阶段,实际测得不同纯碱加入量条件下的碳酸锂沉淀结果如下表:
序号 |
| 沉淀质量(g) | Li2CO3含量(%) | 锂回收率(%) |
0.9:2.0 | 10.09 | 92.36 | 77.67 | |
1.0:2.0 | 10.97 | 90.19 | 82.46 | |
1.1:2.0 | 11.45 | 89.37 | 85.27 | |
1.2:2.0 | 12.14 | 84.82 | 85.85 |
综合以上信息及考虑实际生产时的原料成本,应按照______![]() 填序号
填序号![]() 中CO32-与Li+物质的量之比加入纯碱制备碳酸锂。
中CO32-与Li+物质的量之比加入纯碱制备碳酸锂。
![]() 沉锂温度需控制在
沉锂温度需控制在![]() ,主要原因是______。
,主要原因是______。
![]() 碳化分解具体过程为:①向碳酸锂与水的浆料中通入CO2气体,充分反应后,过滤;②加热滤液使其分解。写出②反应中的化学方程式:__________。写出在碳化分解中可循环利用物质的电子式:_________。
碳化分解具体过程为:①向碳酸锂与水的浆料中通入CO2气体,充分反应后,过滤;②加热滤液使其分解。写出②反应中的化学方程式:__________。写出在碳化分解中可循环利用物质的电子式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示。
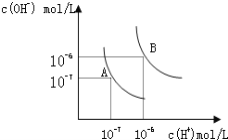
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从_____________增加到_____________。
(2)保持100℃的恒温,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为____________________。
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈________(填“酸性”,“中性”或“碱性”),醋酸体积____________氢氧化钠溶液体积。(填“ >” 或“=”或“<” )。
(4)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,上述离子浓度大小关系中正确的是(选填字母)________。
②若上述关系中D是正确的,则溶液中的溶质为____________________;
③若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol/L,则c(SO42-)= _____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com