
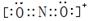 (2分)四面体(1分)
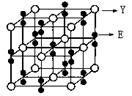
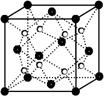
(2分)四面体(1分) 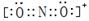 ;NCl3的中心价电子对数为4,分子的VSEPR模型是四面体;(2)某化合物由O、K两种元素组成,根据其晶胞结构利用切割法分析,1个晶胞中含有8个O,4个K,该化合物的化学式为KO2;(3)在化合物K2CrO4的水溶液入适量硫酸,发生的反应为2H++CrO42—===Cr2O72—+H2O,能观察到的现象是溶液由黄色变成橙色;(4)A的简单氢化物NH3极易溶于E的简单氢化物H2O,其原因是NH3、H2O都是极性分子,且它们分子间还能形成氢键;(5)A的最高价氧化物对应水化物HNO3的稀溶液与铝单质反应时,氮元素被还原到最低价,生成硝酸铝、硝酸铵和水,该反应的化学方程式是8Al + 30HNO3 = 8Al(NO3)3 + 3NH4NO3 + 9H2O。
;NCl3的中心价电子对数为4,分子的VSEPR模型是四面体;(2)某化合物由O、K两种元素组成,根据其晶胞结构利用切割法分析,1个晶胞中含有8个O,4个K,该化合物的化学式为KO2;(3)在化合物K2CrO4的水溶液入适量硫酸,发生的反应为2H++CrO42—===Cr2O72—+H2O,能观察到的现象是溶液由黄色变成橙色;(4)A的简单氢化物NH3极易溶于E的简单氢化物H2O,其原因是NH3、H2O都是极性分子,且它们分子间还能形成氢键;(5)A的最高价氧化物对应水化物HNO3的稀溶液与铝单质反应时,氮元素被还原到最低价,生成硝酸铝、硝酸铵和水,该反应的化学方程式是8Al + 30HNO3 = 8Al(NO3)3 + 3NH4NO3 + 9H2O。

科目:高中化学 来源:不详 题型:填空题

| A.离子键 | B.共价键 | C.配位键 | D.金属键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 图a
图a| | BeCO3 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 分解温度 | 100℃ | 540℃ | 960℃ | 1289℃ | 1360℃ |


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | Mn | Fe | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com