
【题目】实验过程中要养成安全、环保意识。下列说法正确的是 ( )
A.浓碱飞溅到皮肤上,应立刻涂上硫酸溶液
B.金属钠着火,立刻用水扑灭
C.实验剩余一氧化碳可直接排放到实验室外
D.水银洒落在地上,应撒上硫粉并进行处理
科目:高中化学 来源: 题型:
【题目】Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
元素 | Mn | Fe | |
电离能/kJmol﹣1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
回答下列问题:
(1)Mn元素价电子层的电子排布式为 , 比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是 .
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断三氯化铁晶体为晶体.
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为 , 其中体心立方晶胞空间利用率为 . 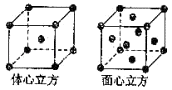
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。若榨汁时加入维生素C,可以有效防止这种现象发生。这说明维生素C具有
A. 还原性 B. 氧化性 C. 碱性 D. 酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小,性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质可以自由迁移,正极反应式为:MnO2+Li++e﹣=LiMnO2 . 回答下列问题:
(1)外电路的电子方向是由极流向极.(填字母)
(2)该电池的负极反应式为 .
(3)如果14g的锂完全溶解放电,所产生的电量用来电解水,会产生L的H2(在标准状况下).
(4)MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4 , 反应的化学方程式为 , K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用A+、B-、C2-、D、E、F分别表示含有18个电子的几种微粒(离子或分子),请回答下列问题:
(1)A元素是________、B元素是________、C元素是_______(用元素符号表示)。
(2)B的单质可用来制“84”消毒液的主要成分,写出反应的离子方程式________________。
(3)用文字描述比较B、C两元素的非金属性强弱的方法(必要时可用方程式,至少一条):___________________________________。
(4)D是由两种元素组成的双原子分子,用电子式表示其形成过程________________。
(5)E是所有含18个电子的微粒中氧化能力最强的分子,其与水反应的化学方程式为___________________。
(6)F分子中含有4个原子,既有极性键又有非极性键,其电子式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量数是 37 的原子, 可能有( )
A.19 个质子, 18 个中子, 20 个电子
B.18 个质子, 19 个中子, 18 个电子
C.19 个质子, 18 个中子, 18 个电子
D.17个质子, 20 个中子, 18 个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产、生活中有广泛的应用.
(1)铜可采用如下方法制备:火法炼铜:Cu2S+O2 ![]() 2Cu+SO2
2Cu+SO2
湿法炼铜:CuSO4+Fe═FeSO4+Cu
上述两种方法中,铜元素均被(填“氧化”或“还原”)成铜单质.
(2)印刷电路板上使用的铜需要回收利用.方法一:用FeCl3溶液浸泡印刷电路板制备CuCl22H2O,实验室模拟回收过程如下:![]()
①证明步骤Ⅰ所加FeCl3溶液过量的方法是 .
②步骤2中所加的氧化剂最适宜的是 .
A.HNO3B.H2O2C.KMnO4
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的“试剂1”是 . (写出一种即可)
④蒸发农缩CuCl2溶液时,要滴加浓盐酸,目的是(用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl22H2O.
方法二:用H2O2和稀硫酸共同浸泡印刷电路板制备硫酸铜时,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(nq)═CuSO4(aq)+2H2O(l)△H1=﹣320kJ/mol
又知:2H2O(l)═2H2O(l)+O2(g)△H2=﹣196kJ/mol
H2(g)+ ![]() O2(g)═H2O(l)△H3=﹣286kJ/mol
O2(g)═H2O(l)△H3=﹣286kJ/mol
则反应Cu(s)+H2SO4(aq)═CuSO4(aq)+H2(g)的△H= .
(3)欲实现反应Cu+H2SO2═CuSO4+H2 , 在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com