
【题目】燃烧1g乙炔生成二氧化碳和液态水放出热量50kJ,则下列热化学方程式书写正确的是( )
A.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+50 kJ?mol﹣1
B.C2H2(g)+ ![]() O2(g)═2CO2(g)+H2O(l)△H=﹣1 300 kJ
O2(g)═2CO2(g)+H2O(l)△H=﹣1 300 kJ
C.2C2H2+5O2═4CO2+2H2O△H=﹣2 600 kJ
D.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2 600 kJ?mol﹣1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】咖啡酸(如图),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
(1)咖啡酸的化学式是其中含氧官能团的名称为、 .
(2)咖啡酸可以发生的反应是(填写序号).
①水解反应 ②加成反应 ③酯化反应 ④消去反应
(3)1mol咖啡酸与浓溴水反应时最多消耗mol Br2 .
(4)咖啡酸与NaHCO3溶液反应的方程式
(5)蜂胶的主要活性成分为CPAE,分子式为C17H16O4 , 该物质在一定条件下可水解生成咖啡酸和一种醇,该醇为芳香醇且分子结构中无甲基,此芳香醇的结构简式为 , 咖啡酸跟该芳香醇在一定条件下反应生成CPAE的化学方程式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷和丙烯混合物共m mol,与n mol的氧气点燃后完全反应,得到CO和CO2的混合气体,以及63g水.试求:
①当m=1时,丙烷和丙烯的质的量之比: .
②当m=1时,且反应后CO和CO2混合气体物质的量是反应前氧气的物质的量的 ![]() 时,则n=;
时,则n=;
③m的取值范围是:;
④n的取值范围是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中处处有化学,下列叙述正确的是
A.人的皮肤在强紫外线的照射下不会失去生理活性
B.常用新制的氢氧化铜检验司机酒后驾车
C.棉花和木材的主要成分都是纤维素
D.蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹食醋缓解不适
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示实验装置可用于制取乙炔. 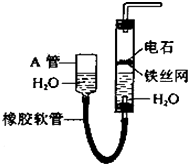
请填空:
(1)A管的作用是 , 制取乙炔的化学方程式是 .
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 , 乙炔发生了反应.
(3)乙炔通入溴水的CCl4溶液中观察到的现象是 .
(4)为了安全,点燃乙炔前应 , 乙炔燃烧时的实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1molL﹣1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( ) 
A.三种酸的电离常数关系:KHA>KHB>KHD
B.滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣)
C.pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣)
D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH﹣)﹣c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: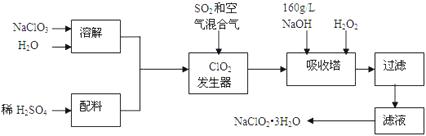
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出产品NaClO23H2O;
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(1)发生器中发生反应的离子方程式为。发生器中鼓入空气的作用可能是。
a.将SO2氧化成SO3 , 增强酸性 b.将NaClO3还原为ClO2 c.稀释ClO2以防止爆炸
(2)吸收塔内发生反应的化学方程式为;吸收塔内的温度不能超过20℃,其目的是。
(3)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。以下还可以选择的还原剂是(选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(4)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是。
(5)某学习小组用碘量法测定粗产品中亚氯酸钠的含量,实验如下:
a.准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250 ml待测溶液。(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-)
b.移取25.00 ml待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定至终点,重复2次,测得平均值为V ml 。(已知:I2+2S2O32-=2I-+S4O62-)
①达到滴定终点时的现象为 。
②该样品中NaClO2的质量分数为 (用含m、c、V的代数式表示,结果化成最简。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)N2O4(g)(无色),如图所示. 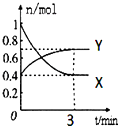
(1)曲线(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) , v(逆) . (填“加快”或“减 慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号); A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,可形成氢氧燃料电池.通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种.试回答下列问题: 
(1)酸式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”).
(2)碱式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com