
ΓΨΧβΡΩΓΩΈ¬Ε»ΈΣTΓφΘ§œρΧεΜΐ≤ΜΒ»ΒΡΚψ»ίΟή±’»ίΤς÷–Ζ÷±πΦ”»κΉψΝΩΜν–‘ΧΩΚΆ1mol NO2Θ§ΖΔ…ζΖ¥”ΠΘΚ2C(s)+2NO2(g)N2(g)+2CO2(g)Ζ¥”ΠœύΆ§ ±ΦδΘ§≤βΒΟΗς»ίΤς÷–NO2ΒΡΉΣΜ·¬ ”κ»ίΤςΧεΜΐΒΡΙΊœΒ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A.TΓφ ±Θ§ΗΟΖ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐΈΣ![]()
B.ΆΦ÷–cΒψΥυ ΨΧθΦΰœ¬Θ§v(’ΐ)ΘΨv(Ρφ)
C.œρaΒψΤΫΚβΧεœΒ÷–≥δ»κ“ΜΕ®ΝΩΒΡNO2Θ§¥οΒΫΤΫΚβ ±Θ§NO2ΒΡΉΣΜ·¬ ±»‘≠ΤΫΚβ¥σ
D.»ίΤςΡΎΒΡ―Ι«ΩΘΚPa:PbΘΨ6:7
ΓΨ¥πΑΗΓΩBD
ΓΨΫβΈωΓΩ
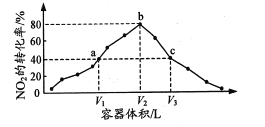
”…Ζ¥”Π![]() Ω…÷Σ»ίΤςΧεΜΐ‘Ϋ¥σΘ§―Ι«Ω‘Ϋ–ΓΘ§Ζ¥”ΠΆυ’ΐΖΫœρ“ΤΕ·Θ§NO2ΒΡΉΣΜ·¬ ΧαΗΏΘ§”…ΆΦœώΩ…÷ΣΘ§œύΆ§ ±ΦδΘ§aΘ§bΈΣ“―¥οΒΫΤΫΚβΒψΘ§cΜΙΈ¥¥οΒΫΤΫΚβΘ§άϊ”ΟΜ·―ßΤΫΚβ≥Θ ΐΚΆΒ»–ßΤΫΚβΫχ––Ζ÷ΈωΓΘ
Ω…÷Σ»ίΤςΧεΜΐ‘Ϋ¥σΘ§―Ι«Ω‘Ϋ–ΓΘ§Ζ¥”ΠΆυ’ΐΖΫœρ“ΤΕ·Θ§NO2ΒΡΉΣΜ·¬ ΧαΗΏΘ§”…ΆΦœώΩ…÷ΣΘ§œύΆ§ ±ΦδΘ§aΘ§bΈΣ“―¥οΒΫΤΫΚβΒψΘ§cΜΙΈ¥¥οΒΫΤΫΚβΘ§άϊ”ΟΜ·―ßΤΫΚβ≥Θ ΐΚΆΒ»–ßΤΫΚβΫχ––Ζ÷ΈωΓΘ
A. aΒψ ±Ζ¥”Π¥οΒΫΤΫΚβΘ§NO2ΉΣΜ·¬ ΈΣ40%Θ§‘ρ
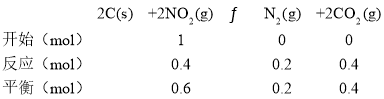
TΓφ ±Θ§ΗΟΖ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐΈΣ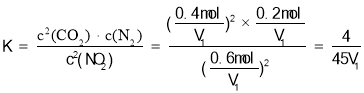 Θ§Ι A¥μΈσΘΜ
Θ§Ι A¥μΈσΘΜ
B. ΆΦ÷–cΒψΜΙΈ¥¥οΒΫΤΫΚβΘ§Ζ¥”ΠΆυ’ΐΖΫœρΫχ––Θ§v(’ΐ)ΘΨv(Ρφ)Θ§Ι B’ΐ»ΖΘΜ
C. œρaΒψΤΫΚβΧεœΒ÷–≥δ»κ“ΜΕ®ΝΩΒΡNO2Θ§Β»–ß”ΎΦ”―ΙΘ§ΤΫΚβΡφ“ΤΘ§ΉΣΜ·¬ ΫΒΒΆΘ§C¥μΈσΘΜ
D.”…AΩ…÷ΣaΒψ ±»ίΤςΡΎΤχΧεΈο÷ ΒΡΝΩΈΣ1.2molΘΜbΒψ ±Ζ¥”Π»ΐΕΈ ΫΈΣ
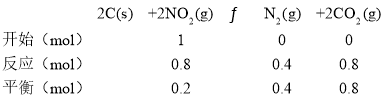
‘ρbΒψ»ίΤςΡΎΤχΧεΈο÷ ΒΡΝΩΈΣ1.4molΘ§”…”ΎV1ΘΦV2Θ§‘ρPa:PbΘΨ6:7Θ§Ι D’ΐ»ΖΘΜ
Ι ¥πΑΗ―ΓΘΚBDΓΘ


 ΩΈ ±―ΒΝΖΫ≠Υ’»ΥΟώ≥ωΑφ…γœΒΝ–¥πΑΗ
ΩΈ ±―ΒΝΖΫ≠Υ’»ΥΟώ≥ωΑφ…γœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΤϊ≥ΒΈ≤ΤχΚΆ»ΦΟΚΈ≤Τχ «‘λ≥…Έμω≤ΒΡ÷ς“Σ‘≠“ρ÷°“ΜΓΘ
(1)ΙΛ“Β…œάϊ”ΟΦΉΆι¥ΏΜ·ΜΙ‘≠NOΘ§Ω…Φθ…ΌΒΣ―θΜ·ΈοΒΡ≈≈Ζ≈ΓΘ
“―÷ΣΘΚCH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΠΛH=-574kJΓΛmol1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΠΛH =-1160kJΓΛmol1
ΦΉΆι÷±Ϋ”ΫΪNO2ΜΙ‘≠ΈΣN2ΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ____________________________ΓΘ
(2)Φθ…ΌΤϊ≥ΒΈ≤ΤχΈέ»ΨΒΡ‘≠άμΈΣ2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΠΛH ΘΦ0ΓΘœρΚψΈ¬Κψ»ίΟή±’»ίΤς÷–≥δ»κNOΚΆCOΘ§”Ο¥ΪΗ–Τς≤βΒΟΒΡ ΐΨί»γœ¬±μΥυ ΨΘΚ
N2(g)+2CO2(g) ΠΛH ΘΦ0ΓΘœρΚψΈ¬Κψ»ίΟή±’»ίΤς÷–≥δ»κNOΚΆCOΘ§”Ο¥ΪΗ–Τς≤βΒΟΒΡ ΐΨί»γœ¬±μΥυ ΨΘΚ
±Φδ/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/ΓΝ10-3molΓΛL1 | 9.00 | 4.00 | 2.00 | 1.00 | 1.00 |
c(CO)/ΓΝ10-3molΓΛL1 | 9.00 | 4.00 | 2.00 | 1.00 | 1.00 |
ΔΌΈΣΝΥΧαΗΏΈ≤Τχ¥ΠάμΒΡ–ßΙϊΘ§Ω…≤…»ΓΒΡ¥κ ©”–____________Θ®–¥≥ωΝΫ÷÷Φ¥Ω…Θ©ΓΘ
ΔΎ¥ΥΧθΦΰœ¬¥οΒΫΤΫΚβ ±Θ§ΦΤΥψΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐK=____________________ΓΘ
(3)ΙΛ“Β…œ”Ο«β―θΜ·ΡΤ»ή“Κά¥Ά§ ±Έϋ ’SO2ΚΆΒΣΒΡ―θΜ·ΈοΤχΧε(NOx)Θ§Ω…ΒΟΒΫNa2SO3ΓΔNaHSO3ΓΔNaNO2ΓΔNaNO3Β»»ή“ΚΓΘΘ®“―÷ΣΘΚ≥ΘΈ¬œ¬Θ§HNO2ΒΡΒγάκ≥Θ ΐΈΣKa=7ΓΝ10-4Θ§H2SO3ΒΡΒγάκ≥Θ ΐΈΣKa1=1.2ΓΝ10-2ΓΔKa2=5.8ΓΝ10-8Θ©ΓΘ
ΔΌ≥ΘΈ¬œ¬Θ§œύΆ§≈®Ε»ΒΡNa2SO3ΓΔNaNO2»ή“Κ÷–pHΫœ¥σΒΡ «________»ή“ΚΓΘ
ΔΎ≥ΘΈ¬œ¬Θ§NaHSO3œ‘_________–‘Θ®ΧνΓΑΥαΓ±ΓΑΦνΓ±ΜρΓΑ÷–Γ±Θ©Θ§≈–ΕœΒΡάμ”… «________________________________________________Θ®Ά®ΙΐΦΤΥψΥΒΟςΘ©ΓΘ
(4)νφΥΊ(Ce)≥ΘΦϊ”–+3ΓΔ+4ΝΫ÷÷ΦέΧ§ΓΘNOΩ…“‘±ΜΚ§Ce4+ΒΡ»ή“ΚΈϋ ’Θ§…ζ≥…NO2-ΓΔNO3-Θ®Εΰ’ΏΈο÷ ΒΡΝΩ÷°±»ΈΣ1ΓΟ1)ΓΘΩ…≤…”ΟΒγΫβΖ®ΫΪ…œ ωΈϋ ’“Κ÷–ΒΡNO2-ΉΣΜ·ΈΣΈόΕΨΈο÷ Θ§Ά§ ±‘Ό…ζCe4+Θ§Τδ‘≠άμ»γΆΦΥυ ΨΓΘ

ΔΌCe4+¥”ΒγΫβ≤έΒΡ__________(ΧνΉ÷ΡΗ¥ζΚ≈)ΩΎΝς≥ωΓΘ
ΔΎ–¥≥ω“θΦΪΒΡΒγΦΪΖ¥”Π Ϋ______________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ’ΐΕΓΟ― «“Μ÷÷”ΟΆΨΚήΙψΒΡΜ·ΙΛ≤ζΤΖΘ§ΕΨ–‘ΚΆΈΘœ’–‘–ΓΘ§ «Α≤»Ϊ–‘ΚήΗΏΒΡ”–Μζ»ήΦΝΘ§Ε‘–μΕύΧλ»ΜΦΑΚœ≥…”Ά÷§ΓΔ ς÷§ΓΔœπΫΚΓΔ”–ΜζΥαθΞΓΔ…ζΈοΦνΒ»ΕΦ”–Κή«ΩΒΡ»ήΫβΡήΝΠΘ§ΜΙΩ…ΉςΈΣΒγΉ”ΦΕ«εœ¥ΦΝΚΆΕύ÷÷”–ΜζΚœ≥…≤ΡΝœΓΘΩ…Ά®Ιΐ“‘œ¬Ζ¥”Π‘≠άμ÷Τ»Γ’ΐΕΓΟ―ΘΚ
2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
ΦΚ÷ΣœύΙΊΈο÷ ΒΡ≤ΩΖ÷–≈œΔ»γœ¬ΘΚ
Ζ–Βψ(Γφ) | ΟήΕ»(g/cm3) | »ήΫβΕ»(g) | œύΕ‘Ζ÷Ή”÷ ΝΩ | |
’ΐΕΓ¥Φ | 117.7 | 0.81 | 7.9 | 74 |
’ΐΕΓΟ― | 142 | 0.77 | ≤Μ»ή”ΎΥ° | 130 |
Ρ≥ΩΈΆβΜ·―ß―ßœΑ–ΓΉι≤ι‘ΡœύΙΊΉ Νœ…ηΦΤΝΥ“‘œ¬ Β―ι≤Ϋ÷ηΚœ≥…’ΐΕΓΟ―ΘΚ
ΔΌ‘Ύ100 mLΝΫΩΎ…’ΤΩ÷–Φ”»κ30.0 mL’ΐΕΓ¥ΦΓΔ5.0 mL≈®ΝρΥαΚΆΦΗΝΘΖ– ·Θ§≥δΖ÷“Γ‘»ΓΘ‘ΎΖ÷Υ°Τς÷–Φ”»κ3.0 mL±ΞΚΆ ≥―ΈΥ°Θ§Α¥ΆΦΦΉΉιΉΑ“«ΤςΘ§Ϋ”Ά®άδΡΐΥ°ΘΜ
ΔΎΖ¥”ΠΘΚ‘ΎΒγ»»ΧΉ…œΦ”»»Θ§ ΙΤΩΡΎ“ΚΧεΈΔΖ–Θ§ΜΊΝςΖ¥”Π‘Φ1–Γ ±ΓΘΒ±Νσ“Κ≥δ¬ζΖ÷Υ°Τς ±Θ§¥ρΩΣΖ÷Υ°ΤςΖ≈≥ω“Μ≤ΩΖ÷Υ°ΓΘΒ±Υ°≤ψ≤Μ‘Ό±δΜ·Θ§ΤΩ÷–Ζ¥”ΠΈ¬Ε»¥ο150 ΓφΘ§Ζ¥”ΠΦΚΜυ±ΨΆξ≥…Θ§ΆΘ÷ΙΦ”»»ΘΜ
Δέ’τΝσΘΚ¥ΐΖ¥”Π“Κά以ΚσΘ§≤πœ¬Ζ÷Υ°ΤςΘ§ΫΪ“«ΤςΗΡ≥…’τΝσΉΑ÷Ο»γΆΦ±ϊΘ§‘ΌΦ”ΦΗΝΘΖ– ·Θ§’τΝσΘ§ ’Φ·ΝσΖ÷ΘΜ
ΔήΨΪ÷ΤΘΚΫΪΝσ≥ω“ΚΒΙ»κ Δ”–10 mLΥ°ΒΡΖ÷“Κ¬©ΕΖ÷–Θ§≥δΖ÷’ώ“ΓΘ§Ψ≤÷ΟΤζ»ΞΥ°“ΚΘ§”–Μζ≤ψ“ά¥Έ”Ο5 mLΥ°Θ§3 mL 5% NaOH»ή“ΚΓΔ3 mLΥ°ΚΆ3 mL±ΞΚΆ¬»Μ·ΗΤ»ή“Κœ¥Β”Θ§Ζ÷»ΞΥ°≤ψΘ§ΫΪ≤ζΈοΖ≈»κΫύΨΜΗ…‘οΒΡ–ΓΉΕ–ΈΤΩ÷–Θ§»ΜΚσΦ”»κ0.2ΓΪ0.4 9ΈόΥ°¬»Μ·ΗΤΘ§‘ΌΫΪ“ΚΧεΉΣ»κΉΑ÷Ο±ϊ÷–Ϋχ––’τΝσΘ§ ’Φ·ΒΫΝσΖ÷9.0 mLΓΘ
ΦΉ. 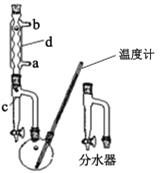 ““.
““. ![]() ±ϊ.
±ϊ.
«κΗυΨί“‘…œ≤ΌΉςΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)÷Τ±Η’ΐΕΓΟ―ΒΡΖ¥”Πάύ–Ά «___Θ§“«ΤςdΒΡΟϊ≥Τ «____ΓΘ
(2)‘Ύ≤Ϋ÷ηΔΌ÷–ΧμΦ” ‘ΦΝΒΡΥ≥–ρ «____ΓΘœύ±»ΉΑ÷Ο““Θ§ΉΑ÷ΟΦΉΒΡ”≈Βψ « ___ΓΘ
(3)‘Ύ≤Ϋ÷ηΔΎ÷–≤…”ΟΒγ»»ΧΉΦ”»»Εχ≤Μ≤…”ΟΨΤΨΪΒΤ÷±Ϋ”Φ”»»ΒΡ‘≠“ρΩ…Ρή «____ΓΘ
(4)‘Ύ≤Ϋ÷ηΔέ÷– ’Φ·ΝσΖ÷ “ΥΒΡΈ¬Ε»ΖΕΈßΈΣ____(Χν’ΐ»Ζ¥πΑΗ±ξΚ≈)ΓΘ
A.115ΓφΓΪll9Γφ B.140ΓφΓΪ144Γφ C. 148ΓφΓΪ152Γφ
(5)‘ΎΨΪ÷Τ÷–Θ§”–Μζ≤ψ‘Ύ____≤ψ(ΧνΓΑ…œΓ±ΜρΓΑœ¬Γ±)Θ§Φ”»κΈόΥ°¬»Μ·ΗΤΒΡΉς”Ο «____ΓΘ
(6)±Ψ–ΓΉι Β―ιΚσΥυΒΟ’ΐΕΓΟ―ΒΡ≤ζ¬ ‘ΦΈΣ ___%(ΦΤΥψΫαΙϊ±ΘΝτ“ΜΈΜ–Γ ΐ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΐΕ…‘ΣΥΊ”…”ΎΤδΧΊ βΒΡΚΥΆβΒγΉ”≈≈≤ΦΕχΤδ”–ΧΊ βΒΡ–‘÷ Θ§≥…ΈΣΜ·―ß―–ΨΩΒΡ÷ΊΒψΚΆ«Α―ΊΓΘ
(lΘ©Ιΐ≤®‘ΣΥΊ¥Π”Ύ÷ήΤΎ±μΒΡ____«χΚΆf «χΓΘ
(2Θ©ΙΐΕ…‘ΣΥΊΡή–Έ≥…ΦρΒΞΜ·ΚœΈοΘ§ΜΙΡή–Έ≥…Εύ÷÷≈δΈΜΜ·ΚœΈο
ΔΌ Ά®≥ΘΘ§dΙλΒά»ΪΩ’Μρ»Ϊ¬ζΒΡΙΐΕ…Ϋπ τάκΉ””κΥ°Ζ÷Ή”–Έ≥…ΒΡ≈δΚœΈοΈό―’…ΪΘ§Ζώ‘ρ”–―’…ΪΓΘ»γ[Co(H2O)6]2+œ‘ΖέΚλ…ΪΘ§Ψί¥Υ≈–ΕœΘ§[Mn(H2O)6]2+____Θ®ΧνΓΑ”–Γ±ΜρΓΑΈόΓ±Θ©―’…ΪΓΘ
ΔΎ Ni2+Ω…–Έ≥…Εύ÷÷≈δΚœΈοΘ§»γNi(CN)42-ΓΘ–¥≥ωCN-ΒΡΒγΉ” Ϋ____Θ§»τΤδ÷–ΝΫΗωCN-±ΜNO2-ΧφΜΜΘ§ΒΟΒΫΒΡ≈δΚœΈο÷Μ”–ΝΫ÷÷ΫαΙΙΘ§‘ρNi(CN)42-ΒΡΩ’ΦδΙΙ–Ά «_____, NO2-ΒΡΩ’ΦδΙΙ–Ά «_____Θ§Τδ÷–N‘≠Ή”ΒΡ‘”Μ·ΖΫ Ϋ «_____ΓΘ
Δέ ¥”ΫαΙΙΫ«Ε»Ζ÷Έω≤Δ±»ΫœCoF2”κCoCl2ΨßΧεΒΡ»έΒψΗΏΒΆ___________ΓΘ
Θ®3Θ©ΫπΓΔΆ≠Β»Ϋπ τΦΑΚœΫπΩ…”ΟΉς…ζ≤ζ ·ΡΪœ©ΒΡ¥ΏΜ·ΦΝΘ§œ¬ΆΦ «“Μ÷÷Ά≠ΫπΚœΫπΒΡΨßΑϊ Ψ“βΆΦΘΚ

ΔΌ ‘ΎΗΟΆ≠ΫπΚœΫπΒΡΨßΧε÷–Θ§”κCu‘≠Ή”ΨύάκœύΒ»«“ΉνΫϋΒΡAu‘≠Ή” ΐΈΣ_______ΓΘ
ΔΎ ‘≠Ή”Ήχ±ξ≤Έ ΐ «”Οά¥±μ ΨΨßΑϊΡΎ≤ΩΗς‘≠Ή”œύΕ‘ΈΜ÷ΟΒΡ÷Η±ξΘ§»τAΒΡ‘≠Ή”Ήχ±ξ≤Έ ΐΈΣΘ®0,0,0)ΘΜBΒΡ‘≠Ή”Ήχ±ξ≤Έ ΐΈΣΘ®0,1,0) , CΒΡ‘≠Ή”Ήχ±ξ≤Έ ΐΈΣΘ®l,0,0)ΓΘ‘ρDΒΡ‘≠Ή”Ή”Ήχ±ξ≤Έ ΐΈΣ_________ΓΘ
Δέ »τAuΓΔCu‘≠Ή”ΑκΨΕΖ÷±πΈΣr1ΚΆr2,‘ρΗΟΨßΑϊ÷–ΒΡ‘≠Ή”Ω’Φδάϊ”Ο¬ ΈΣ__________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕΓΜυœπΫΚΩ…”Ο”Ύ÷Τ‘λΤϊ≥ΒΡΎΧΞΘ§Κœ≥…ΕΓΜυœπΫΚΒΡ“Μ÷÷ΒΞΧεAΒΡΖ÷Ή”ΈΣC4H8Θ§A«βΜ·ΚσΒΟΒΫ2-ΦΉΜυ±ϊΆιΓΘΆξ≥…œ¬Ν–ΧνΩ’ΘΚ
Θ®1Θ©AΖ÷Ή”÷–ΒΡΙΌΡήΆ≈ΒΡΟϊ≥ΤΈΣ___ΓΘ
Θ®2Θ©–¥≥ωΫΪAΆ®»κœ¬Ν–ΝΫ÷÷»ή“ΚΚσ≥ωœ÷ΒΡœ÷œσΓΘ
AΆ®»κδεΥ°ΘΚ___Θ§
AΆ®»κδεΒΡΥΡ¬»Μ·ΧΦ»ή“ΚΘΚ___ΓΘ
Θ®3Θ©–¥≥ωA«βΜ·Κσ≤ζΈο2-ΦΉΜυ±ϊΆιΒΡΆ§Ζ÷“λΙΙΧεΒΡΫαΙΙΦρ ΫΘΚ___ΓΘ
Θ®4Θ©AΩ…“‘ΨέΚœΘ§–¥≥ωAΒΡΨέΚœΖ¥”Π___Θ®“‘Ζ¥”ΠΖΫ≥Χ Ϋ±μ ΨΘ©ΓΘ
Θ®5Θ©AΖΔ…ζΆιΜυΜ·Ζ¥”Π…ζ≥…“Μ÷÷ΧΰBΘ§ΫΪBΆξ»Ϊ»Φ…’ΚσΒΟΒΫCO2ΚΆH2OΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ8ΘΚ9Θ§”…¥ΥΩ…“‘»ΖΕ®BΒΡΜ·―ß ΫΈΣ___ΓΘΆ®ΙΐΕ‘BΒΡΫαΙΙ…ν»κ―–ΨΩΘ§ΖΔœ÷Τδ“Μ¬±¥ζΈο÷Μ”–4÷÷Θ§«“ΧΦΝ¥≤ΜΕ‘≥ΤΓΘ–¥≥ωBΒΡΫαΙΙΦρ ΫΘ§≤Δ”ΟœΒΆ≥ΟϋΟϊΖ®ΟϋΟϊΘΚ___ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕ‘”Πœ¬Ν––π ωΒΡΈΔΝΘMΚΆNΘ§ΩœΕ® τ”ΎΆ§÷ςΉε‘ΣΥΊ«“Μ·―ß–‘÷ œύΥΤΒΡ «Θ® Θ©
A.‘≠Ή”ΚΥΆβΒγΉ”≈≈≤Φ ΫΘΚMΈΣ1s22s2Θ§NΈΣ1s2
B.ΫαΙΙ Ψ“βΆΦΘΚM![]() Θ§N
Θ§N![]()
C.M‘≠Ή”ΜυΧ§2pΙλΒά…œ”–“ΜΕ‘≥…Ε‘ΒγΉ”Θ§N‘≠Ή”ΜυΧ§3pΙλΒά…œ”–“ΜΕ‘≥…Ε‘ΒγΉ”
D.M‘≠Ή”ΜυΧ§2pΙλΒά…œ”–1ΗωΈ¥≥…Ε‘ΒγΉ”Θ§N‘≠Ή”ΜυΧ§3pΙλΒά…œ”–1ΗωΈ¥≥…Ε‘ΒγΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ4÷÷ΕΧ÷ήΤΎ‘ΣΥΊWΓΔXΓΔYΓΔZΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ÷°ΚΆΈΣ19Θ§WΚΆX‘ΣΥΊ‘≠Ή”ΡΎ÷ Ή” ΐ÷°±»ΈΣ1:2Θ§X2+ΚΆZ-άκΉ”ΒΡΒγΉ” ΐ÷°≤νΈΣ8Θ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ « ( )
A. ”κWœύΝΎΒΡΆ§÷ςΉε‘ΣΥΊΩ…÷Τ≥…÷Ί“ΣΒΡΑκΒΦΧε≤ΡΝœ
B. XΒΞ÷ ≤ΜΩ…Ρή÷ΟΜΜ≥ωWΒΞ÷
C. ‘ΣΥΊ‘≠Ή”ΑκΨΕ¥”¥σΒΫ–ΓΒΡΥ≥–ρ «XΓΔYΓΔZ
D. WΓΔYΓΔZ‘ΣΥΊΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·Έο÷–Υα–‘Ήν«ΩΒΡ «HZO4
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΜ·ΚœΈοAΨ≠άν±»œΘΖ®ΚΆ÷ ΤΉΖ®Ζ÷ΈωΒΟ÷ΣΤδΖ÷Ή” ΫΈΣC8H8O2Θ§œύΕ‘Ζ÷Ή”÷ ΝΩΈΣ 136Θ§AΒΡΚΥ¥≈Ι≤’ώ«βΤΉ”–4ΗωΖε«“ΟφΜΐ÷°±»ΈΣ1ΘΚ2ΘΚ2ΘΚ3Θ§AΖ÷Ή”÷–÷ΜΚ§“ΜΗω±ΫΜΖΘ§«“±ΫΜΖ…œ÷Μ”–“ΜΗω»Γ¥ζΜυΘ§ΤδΚΥ¥≈Ι≤’ώ«βΤΉ”κΚλΆβΙβΤΉ»γΆΦΓΘΙΊ”ΎAΒΡœ¬Ν–ΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «Θ® Θ©
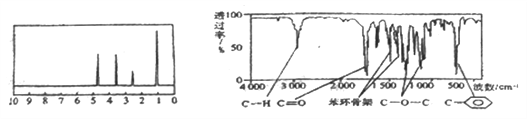
A. AΖ÷Ή” τ”ΎθΞάύΜ·ΚœΈοΘ§‘Ύ“ΜΕ®ΧθΦΰœ¬ΡήΖΔ…ζΥ°ΫβΖ¥”Π
B. A‘Ύ“ΜΕ®ΧθΦΰœ¬Ω…”κ3 mol H2ΖΔ…ζΦ”≥…Ζ¥”Π
C. ΖϊΚœΧβ÷–AΖ÷Ή”ΫαΙΙΧΊ’ςΒΡ”–ΜζΈο÷Μ”–“Μ÷÷
D. ”κA τ”ΎΆ§άύΜ·ΚœΈοΒΡΆ§Ζ÷“λΙΙΧε÷Μ”–2÷÷
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ3Θ§5©¹ΕΰΦΉ―θΜυ±ΫΖ” «÷Ί“ΣΒΡ”–ΜζΚœ≥…÷–ΦδΧεΘ§Ω…”Ο”ΎΧλ»ΜΈο÷ ΑΉΡϊΟ ΥΊΒΡΚœ≥…Θ§“Μ÷÷“‘Φδ±Ϋ»ΐΖ”ΈΣ‘≠ΝœΒΡΚœ≥…Ζ¥”Π»γœ¬ΘΚ
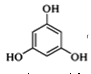 +2CH3OH
+2CH3OH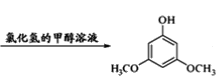 +2H2O
+2H2O
ΦΉ¥ΦΓΔ““Ο―ΚΆ3Θ§5©¹ΕΰΦΉ―θΜυ±ΫΖ”ΒΡ≤ΩΖ÷Έοάμ–‘÷ Φϊœ¬±μΘΚ

Θ®1Θ©Ζ¥”ΠΫα χΚσΘ§œ»Ζ÷άκ≥ωΦΉ¥ΦΘ§‘ΌΦ”»κ““Ο―Ϋχ––ίΆ»ΓΓΘ
ΔΌΖ÷άκ≥ωΦΉ¥ΦΒΡ≤ΌΉς «__ΓΘ
ΔΎίΆ»Γ”ΟΒΫΒΡΖ÷“Κ¬©ΕΖ Ι”Ο«Α–η__œ¥ΨΜΘ§Ζ÷“Κ ±”–Μζ≤ψ‘ΎΖ÷“Κ¬©ΕΖΒΡ__ΧνΘ®ΓΑ…œΓ±ΜρΓΑœ¬Γ±Θ©≤ψΓΘ
Θ®2Θ©Ζ÷άκΒΟΒΫΒΡ”–Μζ≤ψ“ά¥Έ”Ο±ΞΚΆNaHCO3»ή“ΚΓΔ±ΞΚΆ ≥―ΈΥ°ΓΔ…ΌΝΩ’τΝσΥ°Ϋχ––œ¥Β”ΓΘ”Ο±ΞΚΆNaHCO3»ή“Κœ¥Β”ΒΡΡΩΒΡ «__Θ§”Ο±ΞΚΆ ≥―ΈΥ°œ¥Β”ΒΡΡΩΒΡ «__ΓΘ
Θ®3Θ©œ¥Β”Άξ≥…ΚσΘ§Ά®Ιΐ“‘œ¬≤ΌΉςΖ÷άκΓΔΧα¥Ω≤ζΈοΘ§’ΐ»ΖΒΡ≤ΌΉςΥ≥–ρ «__Θ®ΧνΉ÷ΡΗΘ©ΓΘ
aΘ°’τΝσ≥ΐ»Ξ““Ο― bΘ°÷ΊΫαΨß cΘ°Ιΐ¬Υ≥ΐ»ΞΗ…‘οΦΝ dΘ°Φ”»κΈόΥ°CaCl2Η…‘ο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com