
【题目】已知元素X、Y、Z、W的原子序数分别为6、8、11、13,请回答:
(1)写出下列元素符号Z___________;
(2)写出下列元素在周期表中的位置W_______________;
(3)写出下列反应方程式:X单质在足量Y单质中反应_________________________。
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是( )
A. 用铜电极电解硫酸铜溶液:2Cu2++2H2O![]() 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
B. 0.01 mol·L-1NH4Al(SO4)2溶液与0.02 mol·L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-==2BaSO4↓+Al(OH)3↓+NH3·H2O
C. 偏铝酸钠溶液中通入过量的二氧化碳:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. NaClO溶液和FeCl2溶液混合:2ClO-+Fe2++2H2O==Fe(OH)2↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种绿色高效水处理剂.某学习小组用图所示装置(夹持仪器已略去)制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备K2FeO4.

查阅资料知K2FeO4的部分性质如下:
①溶于水、微溶于浓KOH溶液
②在0℃~5℃、强碱性溶液中比较稳定
③Fe3+和Fe(OH)3催化作用下发生分解
④酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2.
请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的作用是__.
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3.为保证反应生成KClO,需要将反应温度控制在0~5℃下进行,在不改变KOH溶液浓度的前提下,实验中可以采取的措施是__.
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO饱和溶液中即可制取K2FeO4,写出该反应的化学方程式__.
(4)制得的粗产品中含有Fe(OH)3、KCl等杂质.
提纯方案:
将一定量的K2FeO4粗产品溶于冷的3mol/L KOH溶液中,用砂芯漏斗(硬质高硼玻璃)过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥.
第一次和第二次过滤得到的固体分别对应的是(填化学式)__、__,过滤时不用普通漏斗而采用砂芯漏斗的原因是(用离子方程式说明)__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用。
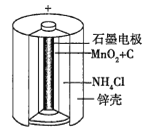
(1)锌锰干电池是应用最普遍的电池之一,如图为锌锰干电池的构造示意图,锌锰干电池的负极材料是________(填物质名称),负极发生的电极反应为_____________。若反应消耗32.5 g负极材料,则电池中转移电子的数目为________。
(2)目前常用的镍镉(Ni-Cd)可充电电池的总反应式可表示为Cd+2NiO(OH)![]() 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
①该电池可以在酸性条件下进行充、放电
②该电池放电时,负极的电极反应式为Cd-2e-+2OH-=Cd(OH)2
③该电池放电时,Cd极的质量减少
④该电池放电时,化学能转变为电能
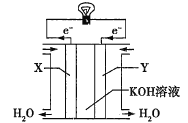
(3)如图为氢氧燃料电池的构造示意图,电解质溶液是KOH溶液。则X极为电池的________(填“正”或“负”)极,X极的电极反应式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、铁是生产、生活及生命中的重要元素。
(1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合能力。药品美蓝是其有效的解毒剂,解毒时美蓝发生_____反应(填“氧化”或“还原”)。
(2)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。 “引火铁”是一种极细的铁粉,它在空气中可以自燃,其原因是_____________。
Ⅱ、在1 L 2 mol·L-1稀硝酸溶液中逐渐加入铁粉,反应中氧化产物的物质的量与加入铁粉的物质的量的关系如图所示:
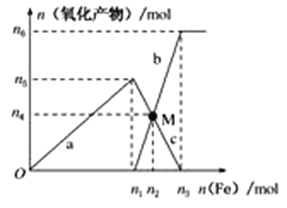
回答下列问题:
(1)写出加入n1mol铁所发生反应的离子方程式_______________________________。
(2)整个过程中转移电子的数目是________。
(3)若M点时再加入V L 2 mol·L-1的稀硝酸,恰好反应完全,则V为___________。
(4)研究表明硝酸的浓度越小,反应后氮的化合价越低。在极稀的硝酸溶液中加入少量铁粉,生成NH4+的离子方程式为___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个恒容的密闭容器中进行下列两个可逆反应:甲:![]() 乙:
乙:![]() 其中能表明甲、乙容器中反应都达到平衡状态的是
其中能表明甲、乙容器中反应都达到平衡状态的是
A. 恒温时,气体压强不再改变
B. 断裂氢氧键速率是断裂氢氢键速率的2倍
C. 混合气体密度不变
D. 单位时间内,消耗水蒸气质量与生产氢气质量比为9:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是( )
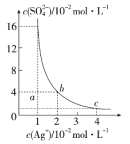
A.b点对应的Ksp等于c点对应的Ksp
B.采取蒸发溶剂的方法可以使溶液从a点变到b点
C.该温度下,Ag2SO4的溶度积常数(Ksp)为1.6×10-5(molL-1)3
D.0.02molL-1的AgNO3溶液与的0.2molL-1的Na2SO4溶液等体积混合不会生成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂钡氧化物二次电池。电池总反应为V2O4+xLi![]() LixV2O4,下列说法正确的是
LixV2O4,下列说法正确的是
A. 该电池充电时,锂极与外电源的负极相连
B. 该电池放电时,Li+向负极移动
C. 该电池充电时阴极的反应为LixV2O4-xe-=V2O4+xLi+
D. 若放电时转移 0.2 mol 电子,则消耗锂 1.4x g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式,回答下列问题:
①2H2(g)+O2(g)=2H2O(l) ΔH=﹣570kJ![]()
②2H2O(g)=2H2(g)+O2(g) ΔH=+483.6kJ![]()
③2C(s)+O2(g)=2CO(g) ΔH=﹣220.8kJ![]()
④C(s)+O2(g)=CO2(g) ΔH=﹣393.5kJ![]()
(1)上述反应中属于放热反应的是_____(填写序号);
(2)H2的燃烧热为_____;
(3)燃烧8g H2生成液态水,放出的热量为_____;
(4)H2O(l)=H2O(g)ΔH=______;
(5)CO的燃烧热的热化学方程式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com