
【题目】某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是( )
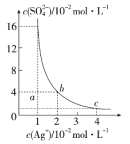
A.b点对应的Ksp等于c点对应的Ksp
B.采取蒸发溶剂的方法可以使溶液从a点变到b点
C.该温度下,Ag2SO4的溶度积常数(Ksp)为1.6×10-5(molL-1)3
D.0.02molL-1的AgNO3溶液与的0.2molL-1的Na2SO4溶液等体积混合不会生成沉淀
科目:高中化学 来源: 题型:
【题目】有M、V、W、X、Y、Z六种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;M元素的一种核素原子核内无中子,Z元素原子的最外层只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。V的单质在空气中含量最高。回答下列问题:
(1)M的一种核素中质子数为中子数的![]() ,则该核素的名称为__。
,则该核素的名称为__。
(2)Z的元素符号为__。
(3)X元素的单质与Z的最高价氧化物对应的水化物反应的离子反应方程式为__。
(4)Y的单质在加热条件下与铁反应的化学方程式为__。
(5)非金属性W__Y(填大于或小于)
(6)用一个方程式证明W和Y的非金属性强弱__。
(7)实验室中,V的最高价氧化物对应的水化物可用Y的最高价氧化物对应的水化物制得,写出相应的化学反应方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备高纯硅有多种方法,其中的一种工艺流程如下:

已知:流化床反应的产物中,除SiCl4外,还有SiHCl3、SiH2Cl2、SiH3Cl、FeCl3等。下列说法正确的是
A. 电弧炉中发生的反应为C+SiO2![]() CO2↑+Si
CO2↑+Si
B. SiCl4进入还原炉之前需要经过蒸馏提纯
C. 每生产l mol高纯硅,需要44. 8L Cl2(标准状况)
D. 该工艺Si的产率高,符合绿色化学要求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素X、Y、Z、W的原子序数分别为6、8、11、13,请回答:
(1)写出下列元素符号Z___________;
(2)写出下列元素在周期表中的位置W_______________;
(3)写出下列反应方程式:X单质在足量Y单质中反应_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁系元素是人体必需的微量元素,Fe3+可以与KSCN溶液、苯酚等发生显色作用。镁元素也是人体所必需的阳离子元素之一,它能够维持核酸结构的稳定性,调节机体免疫功能,对人体抵抗新冠病毒等病毒侵袭起着重要作用。
(1)Fe3+的基态核外电子排布式为____________________。
(2)与SCN互为等电子体且为非极性分子的化学式为_____________(任写一种)。
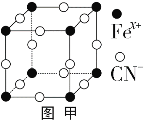
(3)普鲁士蓝俗称铁蓝,晶胞如图甲所示(K+未画出),平均每两个晶胞立方体中含有一个K+,又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为_________。
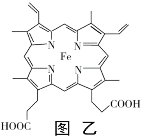
(4)血红素铁(图乙)用作铁强化剂,其吸收率比一般铁剂高3倍,在图乙中画出Fe2+与N原子间的化学键(若是配位键,需要用箭头加以表示)______________

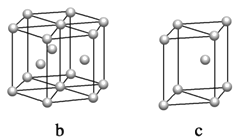
(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为____________;晶胞是图中的_________________(填a、b或c);配位数是__________________;晶胞的体积是2acm3,镁单质的密度为ρg·cm-3,已知阿伏伏德罗常数为NA,则镁的摩尔质量的计算式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均为中学化学中常见物质,在一定条件下,X能与强酸或强碱溶液发生如下图所示的反应![]() 部分反应物、生成物及反应条件略去
部分反应物、生成物及反应条件略去![]() 。则下列说法中不正确的是
。则下列说法中不正确的是![]()
气体![]() 气体Z
气体Z
A.若X为金属单质,则Y、Z可能为同一物质
B.若X为盐,则Y在标准状况下的密度一定是![]()
C.若X为盐,则Z一定能使湿润的红色石蕊试纸变蓝
D.若X为正盐,则其水溶液中水的电离程度比同温度下纯水的电离程度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据能量示意图,下列判断正确的是( )
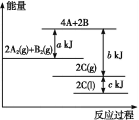
A.化学反应中断键要放出能量,形成化学键要吸收能量
B.该反应的反应物总能量小于生成物总能量
C.2A2(g)+B2(g)= 2C(g)ΔH=-(b+c-a)kJ·mol-1
D.由图可知,生成1 mol C(l),放出![]() (b+c-a)kJ热量
(b+c-a)kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是( )
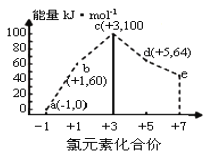
A.b→a+c反应的活化能为生成物总能量减反应物总能量
B.b→a+d反应的热化学方程式为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq) ΔH=-116kJmol-1
C.a、b、c、d、e中,c最稳定
D.一定温度下,Cl2与NaOH溶液反应生成的产物有a、b、d,溶液中a、b、d的浓度之比可能为11∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如![]() 溶液常用作电解液、电镀液等.请回答以下问题:
溶液常用作电解液、电镀液等.请回答以下问题:
![]() 亚铜离子
亚铜离子![]() 基态时的核外电子排布式为 ______
基态时的核外电子排布式为 ______
![]() 晶体的堆积方式是 ______ ,其配位数为 ______ ;
晶体的堆积方式是 ______ ,其配位数为 ______ ;
![]() 往硫酸铜溶液中加入过量氨水,可生成
往硫酸铜溶液中加入过量氨水,可生成![]() ,下列说法正确的是 ______
,下列说法正确的是 ______
A.![]() 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键
B.在![]() 中
中![]() 给出孤电子对,
给出孤电子对,![]() 提供空轨道
提供空轨道
C.![]() 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素
D.![]() 与
与![]() 互为等电子体,空间构型均为正四面体
互为等电子体,空间构型均为正四面体
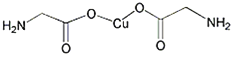
![]() 氨基乙酸铜的分子结构如图,碳原子的杂化方式为______。该分子中
氨基乙酸铜的分子结构如图,碳原子的杂化方式为______。该分子中![]() 键与
键与![]() 键个数比值为 ______
键个数比值为 ______
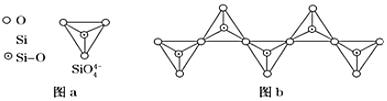
![]() 在硅酸盐中,
在硅酸盐中,![]() 四面体
四面体![]() 如图
如图![]() 通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图b为一种无限长单链结构的多硅酸根,Si与O的原子数之比为 ______ ,化学式为 ______ 。
通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图b为一种无限长单链结构的多硅酸根,Si与O的原子数之比为 ______ ,化学式为 ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com