
霉酚酸酯(结构如下图)是器官移植中抑制细胞增殖最常用的药物。下列说法正确的是
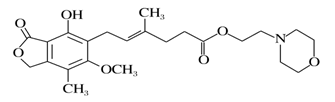
A. 霉酚酸酯能溶于水
B. 霉酚酸酯能与浓溴水发生取代反应
C. 1 mol霉酚酸酯能与含4 mol NaOH的水溶液完全反应
D. 霉酚酸酯既可以催化加氢,又可以使酸性KMnO4溶液褪色
【知识点】有机物分子中的官能团及其结构
【答案解析】D 解析:A、霉酚酸酯是大分子有机物,含有的亲水基(-OH)较少,难溶于水,故A错误;
B、霉酚酸酯结构中含有酚羟基的结构,但是邻位和对位已不能取代,故B错误;
C、1mol 霉酚酸酯中含有酯基2mol,能与含2molNaOH的水溶液反应,含有酚羟基1mol,能与含1molNaOH的水溶液反应,所以1mol 霉酚酸酯能与含3molNaOH的水溶液完全反应,故C错误;
D、霉酚酸酯中含有碳碳双键,既可以催化加氢,又可以使酸性KMnO4溶液褪色,故D正确;
故答案选D
【思路点拨】本题考查有机物的结构和性质,题目难度不大,注意把握有关官能团决定性质的知识,要求学生熟记官能团具有的性质,并熟练运用。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
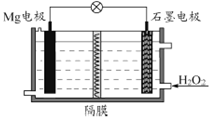
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是
A. Mg电极是该电池的正极
B. H2O2在石墨电极上发生氧化反应
C. 石墨电极附近溶液的pH增大
D. 溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
(1)③、④、⑦的原子半径由大到小的顺序为(用元素符号表示,下同) ▲ ;
(2)⑥和⑦的最高价含氧酸的酸性强弱为(用酸的化学式表示) ▲ ;
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 ▲ ;
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性.
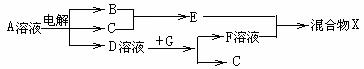
①写出D溶液与G反应的化学方程式: ▲ ;
②写出检验A溶液中溶质的阴离子的方法: ▲ ;
③常温下,若电解1L0.1mol/L的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为: ▲ ;
④若上图中各步反应均为恰好完全转化,则混合物X中含有的物质有: ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅
B.酸性高锰酸钾溶液和溴水都既能鉴别出甲烷和乙烯又能除去甲烷中含有的乙烯再经干燥而获得纯净的甲烷
C.煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来
D.石油中含有C5~C11的烷烃,可以通过分馏得到汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列实验事实:①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;②将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝;③向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液。下列判断不正确的是
A.化合物KCrO2中Cr元素为+3价 B.实验①证明Cr2O3是两性氧化物
C.实验②证明氧化性:Cr2O72->I2 D.实验③证明H2O2既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
铬及其化合物应用广泛。例如用经硫酸酸化处理的三氧化铬(CrO3)硅胶测试司机呼出的气体,根据硅胶颜色的变化可以判断司机是否酒驾
(1)基态铬原子的电子排布式为 。
(2)右图是部分主族元素第一电离能梯度图,图中,a点对应
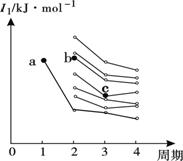 的元素为氢,b、c两点对应的元素分别为 、
的元素为氢,b、c两点对应的元素分别为 、
(填元素符号)。
(3)测试过程中,乙醇被氧化为乙醛(CH3CHO)。乙醇与乙醛
的相对分子质量相差不大,但乙醇的沸点(78.5℃)却比乙醛的沸点(20.8℃)高出许多,其原因是 。
(4)氯化铬酰(CrO2Cl2)可用作染料溶剂,熔点为-96.5℃,沸点为117℃,能与四氯化碳等有机溶剂互溶。氯化铬酰晶体属于 (填晶体类型)。
(5)将CrCl3·6H2O溶解在适量水中得到深绿色溶液,溶液中Cr3+以[Cr(H2O)5Cl]2+ 形式存在。
①上述溶液中,不存在的微粒间作用力是 (填标号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力
②[Cr(H2O)5Cl]2+中Cr3+的轨道杂化方式不是sp3,理由是 。
(6)在酸性溶液中,H2O2能与重铬酸盐作用生成蓝色的CrO5,离子方程式为:
4H2O2 + 2H+ + Cr2O72- =2CrO5 + 5H2O根据下图所示Cr2O72-和CrO5的结构判断,上述反应 (填“是”或“不是”)氧化还原反应。
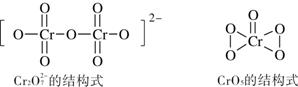
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的量的说法中正确的是( )
|
| A. | 物质的量是国际单位制中的七个基本物理量之一 |
|
| B. | 物质的量实质上就是物质的质量 |
|
| C. | 物质的量是一种物理量的单位 |
|
| D. | 摩尔既是物质的量的单位,又是粒子数量的单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)一定条件下,发生反应CO(g)+H2O(g)  CO2(g)+H2(g),向2 L密闭容器中通入2 mol CO(g)、1 mol H2O(g),2 min 后反应达到平衡时,测得CO的物质的量为1.6 mol,用H2O(g)表示该反应速率为 ,此温度下,该反应的平衡常数为 。若往容器中再加入2 mol CO(g),则重新
CO2(g)+H2(g),向2 L密闭容器中通入2 mol CO(g)、1 mol H2O(g),2 min 后反应达到平衡时,测得CO的物质的量为1.6 mol,用H2O(g)表示该反应速率为 ,此温度下,该反应的平衡常数为 。若往容器中再加入2 mol CO(g),则重新 达到平衡时的CO总转化率
达到平衡时的CO总转化率
20%(填“>”、“<”或“=”)。
(2)在一密闭容器中发生反应2NO2 2NO+O2 ΔH>0,反应
2NO+O2 ΔH>0,反应 过程中NO2的浓度随时间变化的情况如下图所示:
过程中NO2的浓度随时间变化的情况如下图所示:
若曲线A、B分别表示的是该反应在某不同条件 下的反应情况,则曲线B此条件可能是________(填“增大压强”、“减小压强”、“升高温度”、“降低温度”或“使
下的反应情况,则曲线B此条件可能是________(填“增大压强”、“减小压强”、“升高温度”、“降低温度”或“使 用催化剂”)。
用催化剂”)。
(3)一定温度下,在密闭容器中N2O5可发生下列反应:
①2N2O5(g)  4NO2(g)+O2(g) ②2NO2(g)
4NO2(g)+O2(g) ②2NO2(g)  2NO(g)+O2(g)
2NO(g)+O2(g)
若达平衡时,c(NO2)=0.6 mol·L-1,c(O2)=1.3 mol·L-1,则反应②中NO2的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com