
X��Y��Z��M��WΪ���ֶ�����Ԫ�أ�X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��X��Z���γ�XZ2���ӣ�Y��M�γɵ���̬�������ڱ�״̬�µ��ܶ�Ϊ0.76 g��L��1��W����������X��Y��Z��M����Ԫ��������֮�͵�1/2������˵����ȷ����
A��ԭ�Ӱ뾶��W>Z>Y>X>M
B����XZ2ͨ��W������ˮ��Ӧ�����Һ�У����ɵ���һ��ֻ��һ��
C����X��Y��Z��M����Ԫ�ع�ͬ�γɵĻ�������һ���й��ۼ����������Ӽ�
D��CaX2��CaM2��CaZ2��3�ֻ������У��������������Ӹ�����Ϊ1��2
C
��������
��������� X��Y��Z��M��WΪ���ֶ�����Ԫ�أ�X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��X��Z���γ�XZ2���ӣ�Y��M�γɵ���̬�������ڱ�״̬�µ��ܶ�Ϊ0.76 g��L��1������Է���������0.76��22.4��17����Ϊ����������M����Ԫ�أ�Y�ǵ�Ԫ�أ���X��̼Ԫ�أ�Z����Ԫ�ء�W����������X��Y��Z��M����Ԫ��������֮�͵�1/2����W������������1+6+7+8����2��11����W����Ԫ�ء�A��ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶��������ԭ�Ӱ뾶��W>X>Y>Z>M��A����B����CO2ͨ��W������ˮ��Ӧ�����Һ�У����ɵ��ο�����̼���ƣ�Ҳ������̼�����ƣ������Ƕ��ߵĻ���B����C.��H��C��N��O����Ԫ�ع�ͬ�γɵĻ�������һ���й��ۼ���Ҳ���������Ӽ���������Σ�C��ȷ��D��CaC2��CaH2��CaO2��3�ֻ������У��������������Ӹ����ȷֱ�Ϊ1��1��1��2��1��1��D����ѡC��
���㣺����Ԫ�����ڱ���Ԫ�������ɵ�Ӧ��
��������� ����1�����ʵĽṹ������ ����2��Ԫ����������Ԫ�����ڱ� ��������

 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ��̨�и�����ѧ��һģ��ϲ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�鲻��������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ�����и���3��ģ�⿼�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣��������ƣ�NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС���������ʵ��̽������������֪����
��2NO + Na2O2 = 2NaNO2
��2NO2 + Na2O2 = 2NaNO3
������KMnO4��Һ�ɽ�NO2������ΪNO3����MnO4����ԭ��Mn2+��
��.��Ʒ�Ʊ�����飺������װ���Ʊ�NaNO2��

��1��д��װ��A��ƿ�з�����Ӧ�Ļ�ѧ����ʽ���������ת��
�ķ������Ŀ ��
��2��Bװ�õ������� ��
��3����ͬѧ��Ϊװ��C�в��ﲻ�����������ƣ�����̼���ƺ��������ƣ�Ϊ�Ʊ�����NaNO2Ӧ��B��Cװ�ü�����һ��װ�ã����ڿ��ڻ������ӵ�װ��ͼ��������ʢ�ŵ��Լ���

��4�������ʵ�����װ��C��NaNO2�Ĵ��ڣ�д������������ͽ��ۣ� ��
��.�����IJⶨ
��ȡװ��C�з�Ӧ��Ĺ���4.000g����ˮ���250mL��Һ��ȡ25.00mL��Һ����ƿ�У���0.1000mol/L����KMnO4��Һ���еζ���ʵ�������������±���ʾ��
����� | 1 | 2 | 3 | 4 |
KMnO4��Һ���/mL | 20.60 | 20.02 | 20.00 | 19.98 |
��5����һ��ʵ�����ݳ����쳣����������쳣��ԭ������� ��˫��ѡ��
A����ʽ�ζ���������ˮϴ����δ�ñ�Һ��ϴ
B����ƿϴ����δ����
C���ζ��������Ӷ���
D���ζ����˸��Ӷ���
��6�����ݱ������ݣ��������ù������������Ƶ��������� ��
���������4λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ������ѧ��3���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йص������Һ������Ũ�ȹ�ϵ��ȷ����
A��pH=1��NaHSO4��Һ��c(H+)=c(SO42-)+c(OH-)
B������AgCl��AgI���������Һ��c(Ag+)>c(C1-)=c(I-)
C��pH��ȵĢ�NH4Cl ��(NH4)2SO4 ��NH4HSO4��Һ�У�c(NH4+)��С˳��:�٣��ڣ���
D���������ʵ�����NaHC2O4��Na2C2O4����Һ�� 3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ��У����3��������ѧ�Ծ��������棩 ���ͣ������
ѡ��[��ѧ��ѡ�����ʽṹ������]��15�֣�
ǰ������Ԫ��A��B��C��D��E��F��ԭ������������������A��Bͬ���ڣ���̬��AB2��������C��Eԭ�Ӷ���һ��δ�ɶԵ��ӣ�C+��E-��һ�����Ӳ㣬Eԭ�ӵõ�һ�����Ӻ�3p���ȫ������D�����������D����������Ϊ40%���Һ���������������������FΪ��ɫ���ʣ���F+��F2+�������ӡ��ش��������⣺
��1��Ԫ�ص縺�ԣ�D____E (�������)��
��2��A��C�����۵�A_____C(�������)��
��3��AE4��Aԭ���ӻ������ʽΪ:________�ӻ������̬��������Ϊ_______��
��4��F�ĺ�������Ų�ʽΪ______����F������������μ��백ˮ�Ȳ���������������ܽ�Ϊ����ɫ��Һ�������Ҵ���������ɫ���壬�þ�����F��NH3֮��Ļ�ѧ��Ϊ_______��
��5���⻯��ķе㣺B��D�ߵ�ԭ��______��
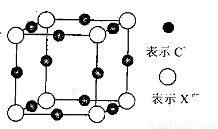
��6��Ԫ��X��ij��̬������Xn-�����е������ó���K��L���Ӳ㣬CnX�������С�ṹ��Ԫ��ͼ��ʾ���þ����������Ӻ������Ӹ�����Ϊ___��������ÿ��Xn-��__���Ⱦ����C+���Ӱ�Χ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ��У����3��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪ij�л���X�Ľṹ��ʽ��ͼ��ʾ�������й���������ȷ����

A��X�Ļ�ѧʽΪC10H10O6
B��X��һ������������FeCl3��Һ������ɫ��Ӧ
C��1 mol X�ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ�Ϊ3 mol��4 mol��1 mol
D��X��һ���������ܷ�����ȥ��Ӧ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ����������ظ���һģ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
(14��)��̼����(2Na2CO3��3H2O2)��һ�ּ�ϴ�ӡ�Ư�ס�ɱ����һ�����ϵƯ����ij��ȤС���Ʊ���̼���Ƶ�ʵ�鷽����װ��ʾ��ͼ���£�
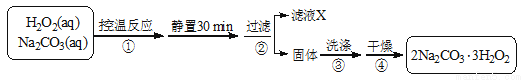
��֪������Ӧ��2Na2CO3 (aq) + 3H2O2 (aq)  2Na2CO3��3H2O2 (s) ��H < 0
2Na2CO3��3H2O2 (s) ��H < 0
����Ӧ��2H2O2 = 2H2O + O2��
50��ʱ2Na2CO3��3H2O2 (s) ��ʼ�ֽ�
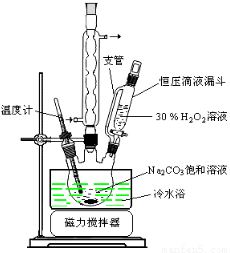
��ش��������⣺
��1������ٵĹؼ��ǿ����¶ȣ�ԭ���� , ���ʩ��_______��_________��_________��
��2������ҺX�м�������NaCl�����������̼���ƣ�ԭ����_________________��
��3���������ѡ����ˮ�Ҵ�ϴ�Ӳ�Ʒ��Ŀ���� ��
��4�����������У��������̼����ʧЧ���� ��
A��NaHCO3 B��MnO2 C��Na2SiO3 D��Na2SO3
��5����̼���Ʋ�Ʒ��������������̼���ƣ������������ⶨ��̼���Ƶ�������������������裺ȡ��Ʒ�ܽ������BaCl2��Һ�����ˡ�ϴ�ӡ��������������Ҫֱ�Ӳⶨ���������У� ��Ʒ������m1g������������m2g(����ĸ��ʾ��ע���京��)����Ʒ�й�̼�������������ı���ʽΪ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и���3��������黯ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ��Ӧ�����ӷ���ʽ��д��ȷ����
A��������Һ��Mg(OH) 2��Ӧ��Mg(OH) 2 +2H+ ===Mg2+ +2H2O
B��̼������Һ�ʼ��ԣ�CO32�� +2H2O  H2CO3 +2OH��
H2CO3 +2OH��
C��NH4HC03��Һ�����NaOH��Һ��Ӧ��NH4+ +OH�� ===NH3��H2O
D���ö��Ե缫��ⱥ��ʳ����Һ��2Cl��+2H2O  2OH�� +Cl2��+H2��
2OH�� +Cl2��+H2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com