

| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
分析 β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂,加入过量浓硫酸溶解β-锂辉矿,加入碳酸钙除去过量的硫酸调节溶液PH=5,使铁离子和铝离子沉淀完全,加入水洗过滤洗去矿泥,然后加入氢氧化钙和碳酸钠沉淀镁离子和钙离子,过滤得到溶液中主要是锂离子的溶液,蒸发浓缩,加入碳酸钠沉淀锂离子生成碳酸锂,洗涤后加入盐酸溶解得到纯净的氯化锂溶液,加热蒸干得到氯化锂,电解熔融氯化锂得到金属锂.
(1)升温、增大接触面积,加快搅拌,增加浸出时间等措施;
(2)LiAlSi2O6 与H2SO4(浓)反应生成硫酸锂、硫酸铝、二氧化硅和水,结合原子守恒配平得到化学方程式;
(3)加入CaCO3,可除去反应Ⅰ中过量的H2SO4,降低溶液中c(H+),根据pH=5,可使Fe3+、Al3+完全沉淀.
(4)反应Ⅲ要除去镁离子,加入过量氢氧化钙后生成氢氧化镁沉淀,然后用碳酸钠除去过量的钙离子杂质,所以沉淀为氢氧化镁、碳酸钙;
(5)蒸发浓缩过程中主要发生锂离子结合碳酸根离子生成碳酸锂;
(6)由于温度越高,Li2CO3的溶解度越小,所以应用热水洗涤Li2CO3.
(7)由于在加热蒸干LiCl溶液时,会产生少量的LiOH,受热分解生成Li2O,所以电解时会产生O2.
解答 解:(1)将硅酸盐改为氧化物形式的方法为:依次将各元素写成氧化物形式,中间用“•”连接,同时要注意氧化物先后顺序,为Li2O•Al2O3•4SiO2,
故答案为:Li2O•Al2O3•4SiO2;
(2)LiAlSi2O6 与H2SO4(浓)反应生成硫酸锂、硫酸铝、二氧化硅和水,结合原子守恒配平得到化学方程式为:2LiAlSi2O6+4H2SO4(浓)=Li2SO4+Al2(SO4)3+4SiO2↓+4H2O,
故答案为:2,4,1,Al2(SO4)3,4SiO2↓,4;
(3)β-锂辉矿在加入过量浓硫酸后,只有SiO2不溶,同时Fe2+被氧化为Fe3+,并生成CaSO4沉淀,所以溶液中含有Fe3+、Al3+、Mg2+、Li+等离子,依据实验目的可知必须除去杂质离子,故在反应Ⅱ中加入碳酸钙的作用为:可除去反应Ⅰ中过量的H2SO4,降低溶液中c(H+),根据pH=5,可使Fe3+、Al3+完全沉淀,
故答案为:除去反应Ⅰ中过量的H2SO4;控制pH,使Fe3+、Al3+完全沉淀;
(4)利用题干信息知反应Ⅲ要除去Mg2+,但在加入沉淀剂Ca(OH)2时会引入大量Ca2+,故还需加入Na2CO3除去Ca2+,即沉淀A为Mg(OH)2沉淀与CaCO3沉淀的混合物,反应的离子方程式为:Mg2++2OH-═Mg(OH)2↓、Ca2++CO32-═CaCO3↓,
故答案为:Mg(OH)2、CaCO3;
(5)蒸发浓缩过程中主要发生锂离子结合碳酸根离子生成碳酸锂,反应的离子方程式为:2Li++CO32-=Li2CO3↓,
故答案为:2Li++CO32-=Li2CO3↓;
(6)实验室里分离固液混合物的操作是过滤,由题中给出Li2CO3的溶解度与温度的关系,可知洗涤Li2CO3沉淀要使用热水,Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗,
故答案为:热水;Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗;
(7)由有氧气产生可逆推知可能的原因:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2,
故答案为:加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2 ;
点评 本题考查了工业上以β-锂辉矿制取金属锂的方法,题目难度中等,试题涉及了化学式的书写、物质的分离与提纯、离子方程式的书写等知识,合理分析题中工艺流程是解题关键.


科目:高中化学 来源: 题型:选择题
| A. | 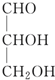 | B. | 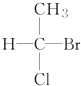 | C. | CH3CH2OH | D. | 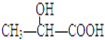 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol羟基(-OH)含有10NA个电子 | |
| B. | 在20gH218O中含有10NA个中子 | |
| C. | 标准状况下,22.4L四氯化碳含有NA个四氯化碳分子 | |
| D. | 1mol乙醇分子中含有共用电子对数目为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 完全沉淀的pH | 5.2 | 3.7 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y处于同一周期 | B. | 原子序数:a<b | ||
| C. | a-b=m+n | D. | 离子半径:Xn+>Ym- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 大气臭氧层的反应是:O+O3═2O2△H,该反应的能量变化如图所示,下列叙述中,正确( )
大气臭氧层的反应是:O+O3═2O2△H,该反应的能量变化如图所示,下列叙述中,正确( )| A. | O+O3═2O2是吸热反应 | B. | O+O3═2O2是放热反应 | ||
| C. | 反应O+O3═2O2的△H=E3-E2 | D. | 反应O+O3═2O2的△H=E3-E1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯银奖牌久置后表面变暗 | |
| B. | 黄铜(Cu、Zn合金)制的铜锣不易产生铜绿 | |
| C. | 纯锌与稀硫酸反应时,滴少量硫酸铜溶液后速率加快 | |
| D. | 生铁比熟铁(几乎是纯铁)容易生绣 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com