
某研究性学习小组就Na2O2的有关性质探究如下:向滴有酚酞的水中投入一定量的 Na2O2,观察到先有大量气泡产生,溶液变红,过一会儿溶液又变为无色。
Na2O2,观察到先有大量气泡产生,溶液变红,过一会儿溶液又变为无色。
对上述实验中溶液变红,过一会儿又褪色的原因,甲、乙两同学提出了不同的解释:
甲同学认为是Na2O2与水反应放出氧气,氧气有氧化性,将酚酞氧化而使溶液褪色;
乙同学则认为是Na2O2与水反应时产生了H2O2,H2O2的强氧化性使酚酞褪色。
(1)乙同学设计了如下实验来证明自己的猜想是正确的:在滴有酚酞的氢氧化钠溶液中滴加3%的H2O2溶液并振荡。
①若乙同学的猜想正确,可观察到的现象是___________________________。
②甲同学针对乙同学的上述验证实验提出还应增做实验才能更直接证明 Na2O2与水反应生成了H2O2,甲同学提出要增加的实验是什么?
Na2O2与水反应生成了H2O2,甲同学提出要增加的实验是什么?
(2)试设计简单实验证明甲同学的解释是否正确(画出简易装置图,说明简要步骤)。
解析 (1)①溶液的红色褪去,是因为H2O2有漂白性,能漂白酚酞。②H2O2在MnO2催化作 用下能放出氧气,可在加入过氧化钠后的水溶液中加入少量MnO2,有气泡放出可直接证明过氧化钠与水反应有H2O2生成。(2)如果要验证是氧气能氧化酚酞,则可向滴有
用下能放出氧气,可在加入过氧化钠后的水溶液中加入少量MnO2,有气泡放出可直接证明过氧化钠与水反应有H2O2生成。(2)如果要验证是氧气能氧化酚酞,则可向滴有 酚酞的氢氧化钠溶液中直接通入氧气来检验。
酚酞的氢氧化钠溶液中直接通入氧气来检验。
答案 (1)①溶液的红色褪去
②在滴有酚酞的水中加入足量过氧化钠,待反应完成后向溶液中加入少量二氧化锰粉末,有气体放出,证明过氧化钠与水反应时有H2 O2生成。
O2生成。
 (2)向滴有酚酞的氢氧化钠溶液中通入氧气,若红色褪去,证明甲同学的推测正确,反之,则不正确。实验装置图如图所示(可用广口瓶等其他仪器代替烧杯,合理即可)
(2)向滴有酚酞的氢氧化钠溶液中通入氧气,若红色褪去,证明甲同学的推测正确,反之,则不正确。实验装置图如图所示(可用广口瓶等其他仪器代替烧杯,合理即可)


科目:高中化学 来源: 题型:
pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1 000 mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是 ( )
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液的酸性弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸

查看答案和解析>>
科目:高中化学 来源: 题型:
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如下图所示,有关洋蓟素的说法正确的是( )
A.分子中含有4个手性碳原子
B.不能与氯化铁溶液发生显色反应
C.能发生酯化反应但不能发生水解反应
D.1mol洋蓟素最多可与11molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
二茂铁[(C5H5)2Fe] 分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料。它的结构如右图所示,下列说法正确的是( )
 A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
B.1mol环戊二烯(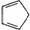 )中含有σ键的数目为5NA
)中含有σ键的数目为5NA
C.分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中提取镁的工艺流程可表示如下:
 贝壳
贝壳 石灰乳
石灰乳
海水 母液
母液 Mg(OH)2
Mg(OH)2
MgCl2·6H2O MgCl2
MgCl2 Mg
Mg
下列说法不正确的是 ( )。
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl2时阴极产生氯气
C.步骤⑤可将晶体置于HCl气体氛围中脱水
D.上述工艺流程中涉及化合、分解和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关气体体积的叙述中,正确的是 ( )。
A.在一定的温度和压强下,各种气态物质体积的大小由气体分子的大小决定
B.在一定的温度和压强下,各种气态物质体积的大小由物质的量的多少决定
C.不同的气体,若体积不同,则它们所含的分子数一定不同
D.气体摩尔体积是指1 mol任何气体所占的体积约为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
①48 g RO42-中,核外电子总数比质子总数多6.02×1023个,则R原子的摩尔质量为________。
②有一真空瓶的质量为M1 g,该瓶充入空气后总质量为M2 g;在相同状况下,若改充某气体A后,总质量为M3 g,则A的相对分子质量为________。
(2)(2014届江西师大附中期末)一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol·L-1的NaOH溶液(密度为1.12 g·mL-1)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.050 0 mol。
①原NaOH溶液的质量分数为________
②所得溶液中Cl-的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
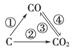
(1)右图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可为______________________________________;
图中变化过程哪些是吸热反应________(填序号)。
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g)CH3OH(g)
方法二 CO2(g)+3H2(g)CH3OH(g)+H2O(g)
在25℃、101 kPa下,1克甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧的热化学方程式:_____________________________________________;
某火力发电厂CO2的年度排放量是2 200万吨,若将此CO2完全转化为甲醇,则理论上由此获得的甲醇完全燃烧放热约是________kJ(保留三位有效数字)。
(3)金属钛冶炼过程中其中一步反应是将原料金红石转化:TiO2(金红石)+2C+2Cl2高温,TiCl4+2CO 已知:C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的ΔH=________。
(4)臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g)===3Ag2O(s) ΔH=-235.8 kJ·mol-1,
已知:2Ag2O(s)===4Ag(s)+O2(g)
ΔH=+62.2 kJ·mol-1,
则O3转化为O2的热化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
A.X极是电源负极,Y极是电源正极
B.a极的电极反应是2Cl--2e-===Cl2↑
C.电解过程中CuSO4溶液的pH逐渐增大
D.Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com