
��48 g RO42���У������������������������6.02��1023������Rԭ�ӵ�Ħ������Ϊ________��
����һ���ƿ������ΪM1 g����ƿ���������������ΪM2 g������ͬ״���£����ij�ij����A��������ΪM3 g����A����Է�������Ϊ________��
(2)(2014�콭��ʦ������ĩ)һ������������������ȼ�գ����û������100 mL 3.00 mol��L��1��NaOH��Һ(�ܶ�Ϊ1.12 g��mL��1)ǡ����ȫ���գ������Һ�к���NaClO�����ʵ���Ϊ0.050 0 mol��
��ԭNaOH��Һ����������Ϊ________
��������Һ��Cl�������ʵ���Ϊ________mol��
������(1)��1��RO42������������������������2������0.5 mol RO42�������������������������1 mol���� ��0.5 mol��M(R)��32 g��mol��1��
��0.5 mol��M(R)��32 g��mol��1��
��������֪����ƿ�п�������Ϊ(M2��M1)g������A������Ϊ(M3��M1)g���ɰ����ӵ�����֪������������ʵ�����ȣ���
 ��
��
M(A)�� ��29��
��29��
(2)�ٸ���c�� ����w��
����w��
��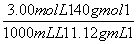 ��100%��10.7%
��100%��10.7%
�ڸ�����ԭ���غ��֪n(NaCl)��n(NaClO)��n(NaOH)��0.100 L��3.00 mol��
L��1��0.300 mol����n(NaCl)��0.300 mol��0.050 0 mol��0.25 mol����n(Cl��)��0.25 mol��
�𰸡�(1)��32 g��mol��1���� ��29
��29
(2)��10.7%����0.25


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йػ�ѧ������ȷ����
A��N2����ʽ��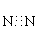
B��Cl-�Ľṹʾ��ͼΪ��
C��CO2�ı���ģ�ͣ�

D��������Ϊ37����ԭ��Ϊ Cl
Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и���ԭ���У��˴˵Ļ�ѧ����һ�����Ƶ��� (����)
A��Pԭ�ӣ�1s2��Qԭ�ӣ�2s2
B��Pԭ�ӣ�M�ܲ�����2�����ӣ�Qԭ�ӣ�N�ܲ�����2������
C��Pԭ�ӣ�2p�ܼ�����1��δ�ɶԵ��ӣ�Qԭ�ӣ�3p�ܼ���Ҳ��1��δ�ɶԵ���
D��Pԭ�ӣ������L�ܲ���ֻ��һ���չ����
Qԭ�ӣ������M�ܲ���Ҳֻ��һ���չ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о���ѧϰС���Na2O2���й�����̽�����£�����з�̪��ˮ��Ͷ��һ������ Na2O2���۲쵽���д������ݲ�������Һ��죬��һ�����Һ�ֱ�Ϊ��ɫ��
Na2O2���۲쵽���д������ݲ�������Һ��죬��һ�����Һ�ֱ�Ϊ��ɫ��
������ʵ������Һ��죬��һ�������ɫ��ԭ�ס�����ͬѧ����˲�ͬ�Ľ��ͣ�
��ͬѧ��Ϊ��Na2O2��ˮ��Ӧ�ų������������������ԣ�����̪������ʹ��Һ��ɫ��
��ͬѧ����Ϊ��Na2O2��ˮ��Ӧʱ������H2O2��H2O2��ǿ������ʹ��̪��ɫ��
(1)��ͬѧ���������ʵ����֤���Լ��IJ�������ȷ�ģ��ڵ��з�̪������������Һ�еμ�3%��H2O2��Һ����
������ͬѧ�IJ�����ȷ���ɹ۲쵽��������___________________________��
�ڼ�ͬѧ�����ͬѧ��������֤ʵ�������Ӧ����ʵ����ܸ�ֱ��֤�� Na2O2��ˮ��Ӧ������H2O2����ͬѧ���Ҫ���ӵ�ʵ����ʲô��
Na2O2��ˮ��Ӧ������H2O2����ͬѧ���Ҫ���ӵ�ʵ����ʲô��
(2)����Ƽ�ʵ��֤����ͬѧ�Ľ����Ƿ���ȷ(��������װ��ͼ��˵����Ҫ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ÿ��ֱ�����������������п���������ʵ�������
(����)��
| �� | �� | �� | �� | �� |
| �������������� | ������� | ��Һ���������� | ��״���������Ħ����� | �DZ�״����ij���ʵ����� |
| �����ӵ����� | �����ܶ� | ��Һ��� | ��״������������ | ���ʵ�Ħ������ |
A���٢ڢ� B���ڢۢ� C���٢ܢ� D���٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ�����ʾ��ȷ����(����)
A��Cl���Ľṹʾ��ͼ��
B��������ӵ����ģ�ͣ�
C���������Ƶĵ���ʽ��
D��������Ľṹʽ��H—O—Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ�������Ʊ���ϩ�ķ�����ʹ�Ҵ���ˮ����Ӧ���Լر�ʾΪCH3CH2OH����CH2===CH2����H2O����֪CH2===CH2(g)��C2H5OH(l)��ȼ���ȷֱ���1 411.0 kJ·mol��1��1 366.8 kJ·mol��1����ʵ������C2H5OH(l)�Ʊ�CH2===CH2(g)����1 molҺ̬ˮ�Ħ�HΪ(����)
A����44.2 kJ·mol��1
B����44.2 kJ·mol��1
C����2 777.8 kJ·mol��1
D����2 777.8 kJ·mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴Ӧ2NO2 2NO+O2�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ� ��
2NO+O2�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ� ��
�ٵ�λʱ��������n mol O2 ��ͬʱ����2n molNO �ڵ�λʱ��������n mol O2 ��ͬʱ����2n molNO2 ����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2:2:1��״̬ �ܻ���������ɫ���ٸı��״̬ �ݻ��������ܶȲ��ٸı��״̬
A.�٢� ���� B.�ڢ� ������ C.�٢ۢ� ������ D.�٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ԫ����Ԫ�����ڱ��е����λ�����±���ʾ�� ���зǽ���Ԫ��X�ĵ����ǵ���ɫ���塣�����жϲ���ȷ����
 A��ZΪCl
A��ZΪCl
B���ǽ����ԣ� X < T
C��ԭ�Ӱ뾶��R <T<Q��
D������������ˮ��������ԣ�T>Q
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com