
【题目】常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成两者溶液的体积之和),下列说法正确的是( )
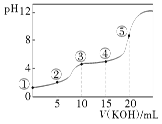
A.点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
B.点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
C.点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1
D.点⑤所示溶液中:c(OH-)= c(H+)+ c(HC2O4-)+ c(C2O42-)
【答案】C
【解析】
此题考查溶液中的电荷守恒,根据溶液不带电这一特性,溶液中的阳离子和阴离子所带电荷相同,根据所加物质的原子间的关系进行书写物料守恒。
A. 根据电荷守恒得出,点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),故A不正确,不符合题意。
B. 点③所示溶液中恰好反应生成KHC2O4,该溶液显酸性,故HC2O4-的电离程度大于其水解程度,故c(K+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4),B不正确,不符合题意。
C. 点④所示溶液中,根据物料守恒得出c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1,C正确,符合题意。
D. 点⑤所示溶液为K2C2O4溶液,依据电荷守恒c(K+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-)和物料守恒c(K+) =2c(H2C2O4)+2c(HC2O4-)+2c(C2O42-),可得溶液中的质子守恒c(OH-)= c(H+)+ c(HC2O4-)+ 2c(H2C2O4),故D答案不正确,不符合题意。
故答案选C。


科目:高中化学 来源: 题型:
【题目】用惰性电极电解,阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:

(1)电解饱和食盐水的化学方程式为______;
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是_________(填字母序号)。
a.Na2SO4b.Na2SO3 c.热空气吹出d.降低阳极区液面上方的气压
(3)食盐水中的I-若进入电解槽,可被电解产生的Cl2氧化为ICl,并进一步转化为IO3-,IO3-可继续被氧化为高碘酸根(IO4-),与Na+结合生成溶解度较小的NaIO4沉积于阳离子交换膜上,影响膜的寿命。
①从原子结构的角度判断ICl中碘元素的化合价应为________。
②NaIO3被氧化为NaIO4的离子方程式为_________;
(4)在酸性条件下加入NaClO溶液,可将食盐水中的I-转化为I2,再进一步除去。通过测定体系的吸光度,可以检测不同pH下I2的生成量随时间的变化,如图所示。已知:吸光度越高表明该体系中c(I2)越大。

用离子方程式解释10min时不同pH体系吸光度不同的原因:______;
②pH=4.0时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因:______;
③研究表明食盐水中I-含量≤0.2mgL-1时对离子交换膜影响可忽略。现将1m3含I-浓度为1.47mgL-1的食盐水进行处理,为达到使用标准,理论上至少需要0.05molL-1NaClO溶液___L。(已知NaClO的反应产物为NaCl,溶液体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X为医用药物,它的合成路线如下:

已知:①1. RCH=CH2
②RBr ![]() RMgBr
RMgBr ![]()
③ RCHO+R’CH2CHO+![]()
(1)A的名称为______,A分子中最多______个原子共面。
(2)写出第①步反应条件______;F的结构简式______;第⑤步反应类型:______;
(3)第③步的化学反应方程式:______;G和![]() 合成聚酯纤维宇航服的化学反应方程式:______;
合成聚酯纤维宇航服的化学反应方程式:______;
(4)G经反应可得到![]() ,写出K的同分异构体中含有一个手性碳(连有四个不同取代基的碳称为手性碳原子)的结构简式______。
,写出K的同分异构体中含有一个手性碳(连有四个不同取代基的碳称为手性碳原子)的结构简式______。
(5)已知:![]() 写出由1-戊醇和必要无机试剂合成G的路线,并在括号注明条件
写出由1-戊醇和必要无机试剂合成G的路线,并在括号注明条件
1-戊醇![]() _____
_____![]() ______________(______)G。
______________(______)G。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学给分子式为C12H26的某烷烃命名为“2,4-二甲基-3,5-二乙基己烷”,另一同学认为这样命名有错误,有关该烷烃的说法,你认为正确的是
A. 若该烷烃由单烯烃与氢气加成而得,则原单烯烃可有11种不同结构
B. 该烷烃的一氯代物有10种
C. 该烷烃正确名称应为2,4,5-三甲基-3-乙基庚烷
D. 该烷烃分子中含有5个支链
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气与碱溶液反应,在低温、稀碱溶液中主要产物是 ClO3-和 Cl-,在 75℃以上、浓碱溶液中主要产物是ClO-和 Cl-。研究小组用如下实验装置制取氯酸钾(KClO3),并测定其纯度。(夹持装置已省略)
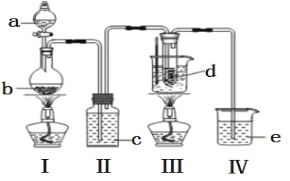
a 为浓盐酸,b 为MnO2,c 为饱和食盐水, d 为 30%KOH 溶液,e 为 NaOH 溶液
回答下列问题:
(1)检查装置气密性后,添加药品,待装置 III 水温升至 75℃开始反应。
①装置 II 的作用为_____________________________________。
②若取消装置 II,对本实验的影响是___________________。
③从装置 III 的试管中分离得到 KClO3 粗产品,其中混有的杂质是 KClO 和_____________(填化学式)。
(2)为测定产品 KClO3 的纯度,进行如下实验:
步骤 1:取 3.00g 样品溶于水配成 250mL 溶液。
步骤 2:取 25.00mL 溶液于锥形瓶中,滴加足量H2O2 溶液充分振荡以除尽ClO-。然后煮沸溶液 1~2 分钟,冷却。
步骤 3:加入过量KI溶液,再逐滴加入足量稀硫酸。(ClO3- +6I- +6H+= Cl-+3I2+3H2O)
步骤 4:加入指示剂,用 0.600mol/LNa2S2O3 标准溶液滴定至终点,消耗标准溶液 20.00mL。(2S2O32-+I2=S4O62-+2I-)
步骤 2 中除去 ClO-的离子方程式是_________________。
②样品中 KClO3 的貭量分数为_____。(保留三位有效数字,KClO3 式量:122.5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳氢化合物有多种,它们在工业生产、生活中有重要用途。
(1)工业上可由丁烯(C4H8)来制备丙烯(C3H6)和乙烯(C2H4),其主要反应原理为:
反应I:C4H8 (g) ![]()
![]() C3H6(g) ΔH1
C3H6(g) ΔH1
反应II:C4H8(g) ![]() 2C2H4 (g) ΔH2
2C2H4 (g) ΔH2
①已知烃的裂解是吸热反应,则ΔH1________ΔH2(填“>”、 “=”或“<”)。
②若某温度下反应达到平衡时C4H8、C3H6、C2H4的体积分数分别为20%、70%、10%,平衡时总压强为P,请计算该温度下反应II的平衡常数Kp=________(Kp为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
(2)石油危机日渐严重,甲烷的转化和利用在天然气化工行业有非常重要的作用。甲烷重整技术主要是利用甲烷和其他原料来制备合成气(CO和H2混合气体)。现在常见的重整技术有甲烷-水蒸气重整,甲烷-二氧化碳重整,其反应分别为:
CH4(g) + H2O(g) ![]() CO(g) + 3H2(g) ΔH>0
CO(g) + 3H2(g) ΔH>0
CH4(g) + CO2(g) ![]() 2CO(g) + 2H2(g)
2CO(g) + 2H2(g)
①下图为反应压强为0.3 MPa,投料比n(H2O)/n(CH4)为1,在三种不同催化剂催化作用下,甲烷-水蒸气重整反应中CH4转化率随温度变化的关系。
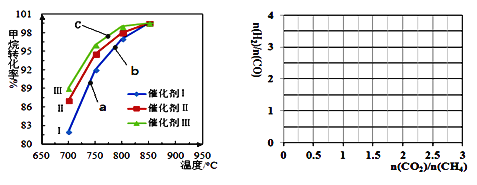
下列说法正确的是________。
A 在相同条件下,三种催化剂Ⅰ、Ⅱ、Ⅲ的催化效率由高到低的顺序是Ⅰ>Ⅱ>Ⅲ
B b点CH4的转化率高于a点,原因是b、a两点均未达到平衡状态,b点温度高,反应速率较快,故CH4的转化率较大
C C点一定未达到平衡状态
D 催化剂只改变反应速率不改变平衡移动,所以在850℃时,不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下达平衡时CH4的转化率相同
②催化剂Ⅰ也可以催化甲烷-二氧化碳重整。在催化剂Ⅰ催化下,反应温度850 oC ,n(H2O)/n(CH4)为1的体系中,加入CO2。画出反应达到平衡时n(H2)/n(CO)随进料时n(CO2)/n(CH4)的变化曲线。(已知:甲烷-二氧化碳重整的平衡常数>>甲烷-水蒸气重整反应的平衡常数)________ 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子)。
①阳极的电极反应式为________。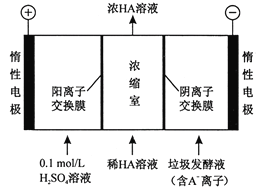
②电解过程中,采取一定的措施可控制阳极室的pH约为6~8,此时进入浓缩室的OH-可忽略不计。400 mL10 g/L 乳酸溶液通电一段时间后,浓度上升为 145 g/L(溶液体积变化忽略不计),则阴极上产生的H2在标准状况下的体积约为________L。(乳酸的摩尔质量为90g/ mol )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如图所示,E1表示反应A+B→X的活化能。下列有关叙述正确的是
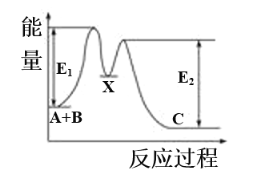
A. X是反应A+B→C的催化剂
B. 反应A+B→C的ΔH<0
C. E2表示反应X→C的活化能
D. 加入催化剂可改变反应A+B→C的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用图示装置进行实验,反应进行足够长时间后装置II中实验现象正确的是
① | ② | ③ | II中实验现象 |
| |
A | 浓盐酸 | 碳酸钙 | 滴有酚酞的稀碳酸钠溶液 | 溶液由红色变为浅红色 | |
B | 浓氨水 | 氧化钙 | 硫酸亚铁溶液 | 产生大量白色沉淀 | |
C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 | |
D | NH4Cl溶液 | NaAlO2溶液 | 紫色石蕊试液 | 溶液由紫色变为蓝色 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.通过传感器可以监测空气中甲醛的含量。该传感器的原理
如图所示:

(1)该装置的主要能量转化形式是_______________。b为______极,发生的电极反应式为_________________。
(2)在传感器工作过程中,电解质溶液硫酸的浓度___________(填“增大”“减小”“不变”)。当电路中转移0.2 mol电子时,传感器内参加反应的HCHO为_______g。
Ⅱ.用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。

(1)该电解槽的阴极发生_____反应(填“氧化”“还原”)。
(2)制得的硫酸溶液从出口_______(填“A”、“D”)导出,并简述原因________________________________________________(请用化学用语和文字解释)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com