
【题目】下列有关实验原理或操作正确的是( )
A. 选择合适的试剂,用图1装置可分别制取和收集少量CO2、NO 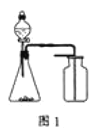
B. 除去石英(主要成分SiO2)中少量碳酸钙:用稀盐酸溶解后过滤
C. 洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干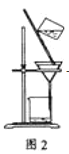
D. 用广泛pH试纸测得0.1molL-1NH4Cl溶液的pH=5.2
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O
C. C3H8O D. C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂联合生产等都是很好的“低碳”生产方式。下面是几家工厂利用废气、废液、废渣联合生产化肥硫酸铵的工艺:

请回答下列问题:
(1)操作②为______________________________________________________。
(2)工业合成氨的化学方程式为_____________________。
(3)沉淀池中生成硫酸铵的化学方程式________________________________________。
(4)在实验室中检验氨气的方法是_________________________________。
(5)副产品的化学式为________。该联合生产工艺中可以循环使用的物质是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的说法正确的是( )
A. 乙烷与![]() 在光照条件下发生取代反应,最多生成6种氯代烃
在光照条件下发生取代反应,最多生成6种氯代烃
B. 丙烯能分别使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,二者褪色原理相同
C. 甲苯分子中最多有12个原子共平面
D. 乙醇在不同条件下可被氧化生成二氧化碳、乙醛或乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铬铁矿[主要成分为![]() ,还含有
,还含有![]() 等杂质]为原料生产
等杂质]为原料生产![]() 的一种工艺流程如下:
的一种工艺流程如下:
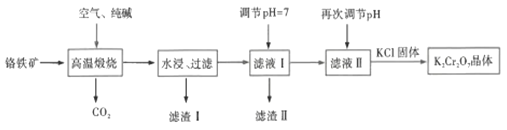
回答下列问题:
(1)![]() 可用氧化物的形式表示为___________。
可用氧化物的形式表示为___________。
(2)高温煅烧时![]() 分别与纯碱反应,固体产物分别为
分别与纯碱反应,固体产物分别为![]() 、___________;
、___________;![]() 发生反应的固体产物则为
发生反应的固体产物则为![]() 和一种红棕色固体,该反应的化学方程式为______________________;上述流程中,高温煅烧若在实验室中进行,适宜选用的仪器为___________(填标号)。
和一种红棕色固体,该反应的化学方程式为______________________;上述流程中,高温煅烧若在实验室中进行,适宜选用的仪器为___________(填标号)。
a.烧杯 b.蒸发皿 c.瓷坩埚 d.铁坩埚
(3)滤渣I的主要成分是___________;调节pH=7的目的是___________。
(4)再次调节pH是向滤液Ⅱ中加入![]() 使pH变小,溶液由黄色变为橙色,发生反应的离子方程式为______________________;能否用盐酸代替
使pH变小,溶液由黄色变为橙色,发生反应的离子方程式为______________________;能否用盐酸代替![]() 调节pH___________(填“能”或“否”)。
调节pH___________(填“能”或“否”)。
(5)向橙色溶液中加入![]() 固体,获得
固体,获得![]() 晶体的操作依次是加热浓缩、___________、过滤、洗涤、干燥。
晶体的操作依次是加热浓缩、___________、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液X中只可能溶有K+、Mg2+、Al3+、AlO2-、SiO32-、SO32-、CO32-、SO42-中的若干种离子,某同学对该溶液进行了如下实验:

下列判断错误的是
A. 气体甲可能是混合物
B. 沉淀甲是硅酸和硅酸镁的混合物
C. 白色沉淀乙的主要成分是氢氧化铝
D. K+、AlO2-和SiO32-一定存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3 和NaHCO3的说法错误的是
A. 等质量Na2CO3 和NaHCO3分别和足量盐酸反应,相同条件下前者生成CO2少
B. 将石灰水分别加入NaHCO3和Na2CO3中,前者不生成沉淀
C. 相同条件下Na2CO3 比NaHCO3更易溶于水
D. Na2CO3 固体中含少量NaHCO3,可用加热法除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某XY3气体ag,它的摩尔质量为bg·mol1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为_____;
(2)该气体所含原子总数为____;
(3)该气体在标准状况下的体积为____;
(4)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为____;将该溶液加水稀释至原体积的2倍后,再取出50 mL稀释后的溶液,则取出溶液的物质的量浓度____;
(5)标准状况下,相同体积的另一种气体CH4全部转化成CO2时转移的电子的物质的量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验小组在“探究碘水与FeCl2溶液能否反应”的系列实验中发现:在足量的稀KI溶液中,加入1~2滴FeCl3溶液,振荡后溶液呈黄色。
(查阅资料)
碘微溶于水,碘的水溶液颜色随浓度变化呈现黄色或棕色,碘水中含有碘单质;含Fe3+的溶液也呈黄色。
(提出问题)
Fe3+、I2的氧化性强弱情况。
(提出猜想)
(1)甲同学认为氧化性I2>Fe3+,故上述实验现象不是发生化学反应所致,则溶液呈黄色是因为含______;乙同学认为氧化性Fe3+>I2,故上述实验现象是发生化学反应所致,则溶液呈黄色是因为含_______。
(设计实验并验证)
(2)为验证乙同学的观点正确,丙同学选用下面所提供的试剂设计出以下两种方案进行实验,请完成下列表格。供选用的试剂:a.酚酞试液 b.四氯化碳 c.无水酒精 d.KSCN溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
试剂 | 实验现象 | |
方案1 | ____________ | ______ |
方案2 | ______ | _________ |
(实验结论)
氧化性:Fe3+>I2。
(拓展应用)
(3)①根据上述实验推测,若在FeI2溶液中通入氯气,首先被氧化的离子是________。
②在100mL FeI2溶液中通入2.24LCl2(标准状况下),溶液中若有![]() 的Fe2+ 被氧化,用离子方程式表示该反应过程:___。
的Fe2+ 被氧化,用离子方程式表示该反应过程:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com