
下列实验操作中正确的是( )
| A.用干燥的pH试纸测定某氯水的pH |
| B.做完银镜反应的试管可以用氨水来洗涤 |
| C.为了除去乙酸乙酯中混有的少量乙酸,加入足量氢氧化钠溶液,充分搅拌后分液 |
| D.如果苯酚浓溶液沾到皮肤上,应立即用酒精擦洗 |
D
解析试题分析:氯水具有强氧化性,能使pH试纸褪色,所以不能用的pH试纸测定某氯水的pH,A不正确;单质银不能溶解在氨水中,所以做完银镜反应的试管可以用硝酸来洗涤,B不正确;C中氢氧化钠能和乙酸乙酯反应,所以为了除去乙酸乙酯中混有的少量乙酸,应该用饱和的碳酸钠溶液,充分搅拌后分液,C不正确;苯酚能溶解在酒精中,则如果苯酚浓溶液沾到皮肤上,应立即用酒精擦洗,D正确,答案选D。
考点:考查化学实验基本操作的正误判断
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
下列叙述不正确的是
| A.实验I :反应开始时反应速率由慢变快,再变慢 |
| B.实验II :滴加几滴浓H2SO4后,溶液颜色由黄色变为橙色 |
| C.实验III:由该实验可以验证催化剂的催化效果 |
| D.实验IV:能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用下列实验装置进行相应的实验,能达到实验目的的是
| A.图I用于实验室制氨气并收集干燥的氨气 | B.图II用于除去CO2中含有的少量HCl |
| C.图III用于提取I2的CCl4溶液中的I2 | D.图IV用于检查碱式滴定管是否漏液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以下贮存物质的方法正确的是( )
| A.少量白磷贮存在二硫化碳中 |
| B.水玻璃贮存在带玻璃塞的玻璃瓶中 |
| C.少量钠贮存在酒精中 |
| D.少量钠贮存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验操作或事实与预期实验目的或所得结论一致的是( )
| 选项 | 实验操作或事实 | 实验目的或结论 |
| A | 某溶液 冒出气泡 冒出气泡 | 说明原溶液中一定含有CO32- |
| B | SiO2与纯碱高温可生成CO2 | 说明硅酸的酸性比碳酸强 |
| C | 碘化钾溶液久置显黄色 | 是由于I-被还原,析出的I2溶于溶液中 |
| D | 铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应 | 说明铁钉表面形成了一层致密稳定的氧化膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关化学实验的说法中正确的是
| A.烧杯、坩埚、试管、锥形瓶都可以用酒精灯直接加热 |
| B.银镜反应、乙醛与新制Cu(OH)2反应、实验室制取乙烯都必须用水浴加热 |
| C.制取氨气、氢气时都可以用向下排空气法收集 |
| D.石油的分馏、实验室制取乙炔和制取蒸馏水都要用到冷凝装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)下图中A、B、C、D是常见的普通玻璃试剂瓶。请把下列试剂的序号填写在适合盛放的试剂瓶下面的括号内:
a.浓硫酸 b.碳酸钠溶液 c.铝片 d.浓硝酸 e.氢氧化钠溶液 f.二氧化锰
| A | B | C | D |
 |  |  |  |
| ( ) | ( ) | ( ) | ( ) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
信息时代产生的大量电子垃圾对环境造成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:
回答下列问题:
⑴第①步Cu与酸反应的离子方程式为 ;得到滤渣1的主要成分为 。
⑵第②步加入H2O2的作用是 ,使用H2O2的优点是 ;调节pH的目的是使 生成沉淀。
⑶用第③步所得CuSO4·5H2O制备无水CuSO4的方法是 。
⑷由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:
上述三种方案中, 方案不可行,原因是 ;
从原子利用率角度考虑, 方案更合理。
⑸探究小组用滴定法测定CuSO4·5H2O(Mr=250)含量。取a g 试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol/L EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++ H2Y2-=CuY2-+ 2H+
写出计算CuSO4·5H2O质量分数的表达式ω= ;
下列操作会导致CuSO4·5H2O含量测定结果偏高的是 。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除静可与EDTA反应的干扰离子
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(14分)水中因含有机物而具有较高的化学耗氧量。常用酸性KMnO4氧化有机物测其含量。主要操作步骤如下:
(1)仪器A为 (填酸式或碱式)滴定管;要顺利完成实验,步骤Ⅲ中溶液颜色应为 。
(2)完善步骤Ⅳ涉及的离子方程式:
C2O42—+ MnO4—+ = Mn2++ CO2↑+
该步骤中滴入第一滴Na2C2O4时褪色较慢,以后的滴定中褪色较快,其原因是 。
(3)若步骤Ⅳ中所用Na2C2O4溶液为20.00ml,已知滴定后的液面如图所示,请在图中标出滴定前的液面。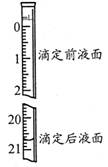
(4)若实验测量结果比实际有机物含量偏高,分别从以下两个方面猜想:
猜想1:水样中Cl—影响
猜想2:配制Na2C2O4标液定容时 。
(5)若猜想1成立,请根据资料卡片补充完善上述实验以消除Cl—影响。(限选试剂:AgNO3溶液、Ag2SO4溶液、KMnO4溶液、Na2C2O4溶液) 。
资料卡片:
1、有机质可HNO3被氧化。
2、AgCl不与酸性KMnO4溶液反应。
3、Ag2C2O4可被酸性KMnO4溶液氧化。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com