
【题目】中科院科学家发现,在常温常压与可见光照射下,N2与H2O在水滑石(LDH)表面发生反应:2N2(g) + 6H2O(g) ![]() 4NH3(g) + 3O2(g) – Q(Q>0)。关于该过程的说法错误的是
4NH3(g) + 3O2(g) – Q(Q>0)。关于该过程的说法错误的是
A.属于固氮过程
B.太阳能转化为化学能
C.反应物的总能量高于生成物的总能量
D.反应物的总键能高于生成物的总键能
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、Q、W、R的原子序数与其常见化合价关系如图所示。下列说法正确的是
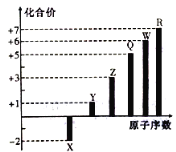
A.X、Y、Z、W、R的简单离子半径大小顺序为R>W>Z>Y>X
B.Q元素形成的可溶性盐的溶液不可能显酸性
C.X、Y、R形成的某种化合物可以用于漂白、消毒
D.Y、Z和W三者最高价氧化物对应的水化物间不能两两相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其原理如图所示。下列说法正确的是
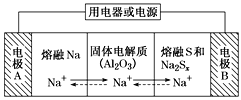
A.放电时,电极A为正极
B.充电时,Na+ 从电极A向电极B迁移
C.充电时,电极B反应式为S22-- 2e- === xS
D.该电池工作的适宜温度应控制在25 ℃左右
查看答案和解析>>
科目:高中化学 来源: 题型:
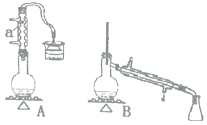
【题目】实验室用加热1一丁醇、浓H2SO4和溴化钠混合物的方法来制备1一溴丁烷,设计了如图所示的实验装置![]() 其中的夹持仪器已省略
其中的夹持仪器已省略![]() 。
。
已知:H2SO4+NaBr=NaHSO4+HBr, H2SO4(浓)+2HBr=Br2+SO2↑+2H2O
请回答下列问题:
(1)仪器a的名称为______。
(2)制备操作中,加入的浓硫酸事先要进行稀释,其目的是______![]() 填选项字母
填选项字母![]() 。
。
![]() 减少副产物烯和醚的生成
减少副产物烯和醚的生成![]() 减少
减少![]() 的生成
的生成![]() 水是反应的催化剂
水是反应的催化剂
(3)写出此实验制1一溴丁烷的总化学方程式______。
(4)有同学拟通过红外光谱仪鉴定所得产物中是否含有“![]() ”,来确定副产物中是否存在丁醚
”,来确定副产物中是否存在丁醚![]() 请评价该同学设计的鉴定方案是否合理?理由是______。
请评价该同学设计的鉴定方案是否合理?理由是______。
(5)为了进一步提纯1一溴丁烷,该小组同学查得相关有机物的有关数据如表:
物质 | 熔点 | 沸点 |
1一丁醇 |
|
|
1一溴丁烷 |
|
|
丁醚 |
|
|
1一丁烯 |
|
|
则用B装置完成此提纯实验时;,实验中要迅速升高温度至______收集所得馏分。
(6)若实验中所取1一丁醇、NaBr分别为![]() 、
、![]() ,浓硫酸
,浓硫酸![]() ,蒸出的粗产物经洗涤,干燥后再次蒸馏得到
,蒸出的粗产物经洗涤,干燥后再次蒸馏得到![]() 一溴丁烷,则1一溴丁烷的产率是______
一溴丁烷,则1一溴丁烷的产率是______![]() 保留2位有效数字
保留2位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国于2007年11月成功地发射了嫦娥一号探测卫星,确定对月球土壤中14种元素的分布及含量进行探测等,月球的矿产资源极为丰富,仅月面表层![]() 厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石
厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石![]() 、斜长石
、斜长石![]() 和橄榄石
和橄榄石![]() 等,下列说法或分析不正确的是( )
等,下列说法或分析不正确的是( )
A.月球上有游离态铁是因为月球上铁的活动性比地球上铁的活动性弱
B.辉石、斜长石及橄榄石均属于硅酸盐矿
C.橄榄石中铁为![]() 价
价
D.斜长石的氧化物形式可表示为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MoS2(辉钼矿的主要成分)可用于制取钼的化合物润滑添加剂氢化反应和异构化反应的催化剂等。回答下列问题:
(1)反应3MoS2+18HNO3+12HCl=3H2[MoO2Cl4]+18NO↑+6H2SO4+6H2O中,每溶解1mol MoS2,转移电子的物质的量为___________。
(2)已知:MoS2(s)= Mo(s)+S2(g) △H1
S2(g)+2O2(g)=2SO2(g) △H2
2MoS(s)+7O2(g)=2MoO3 (s)+4SO2(g) △H3
反应2Mo(s)+3O2(g)=2MoO3(s)的△H=___________(用含△H1、△H2、△H3的代数式表示)。
(3)利用电解法可浸取辉钼矿得到Na2MoO4和Na2SO4溶液(装置如图所示)。

①阴极的电极反应式为______________________。
②一段时间后,电解液的pH___________ (填“增大”“减小”或“不变”),MoO42-在电极___________(填“A”或“B”)附近生成。
③实际生产中,惰性电极A一般不选用石墨,而采用DSA惰性阳极(基层为TiO2,涂层为RuO2+IrO2),理由是_______________________。
(4)用辉钼矿冶炼Mo的反应为
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H。
①该反应的△H___________(填“>”或“<”)0;p1、p2、p3按从小到大的顺序为___________。
②在某恒容密闭容器中加入0.1 mol MoS2、0.2mol Na2CO3、0.4mol H2,一定温度下发生上述反应,下列叙述说明反应已达到平衡状态的是____________ (填标号)。
a.v正(H2)=v逆(CO)
b.气体的密度不再随时间变化
c.气体的压强不再随时间变化
d单位时间内断裂H一H键与断裂H—O键的数目相等
③在2L的恒温恒容密闭容器中加入0.1 mol MoS2、0.2 mol Na2CO3、0.4molH2,在1100K时发生反应,达到平衡时恰好处于图中A点,则此温度下该反应的平衡常数为___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。
回答下列问题:
(1)Te属于元素周期表中_____区元素,其基态原子的价电子排布式为_____。
(2)基态Na原子中,核外电子占据的原子轨道总数为____,最高能层电子云轮廓图形状为_____
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为_____(用元素符号表示)。
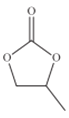
(4)CO32-的几何构型为______;碳酸丙烯酯的结构简式如图所示,则其中碳原子的杂化轨道类型为_________,1mol碳酸丙烯酯中键的数目为________.
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是_____,该配离子包含的作用力为__(填选项字母)。
A.离子键 B.极性键 C.配位键 D.氢键 E.金属键
(6)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为______,该晶胞的密度为ρg/cm3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为_____cm(用含ρ、NA的代数式表示)。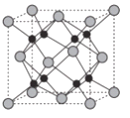
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据杂化轨道理论和价电子对互斥理论模型判断,下列分子或离子的中心原子的杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥理论模型 | 分子或离子的空间构型 |
A |
|
| 直线形 | 直线形 |
B |
|
| 平面三角形 | 三角锥形 |
C |
|
| 四面体形 | 平面三角形 |
D |
|
| 四面体形 | 正四面体形 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是( )
A.若2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol,则H2的燃烧热为241.8 kJ/mol
B.已知强酸与强碱在稀溶液里反应的中和热为57.3 kJ/mol,则H2SO4(aq)+ Ba(OH)2(aq)= BaSO4(s)+2H2O(l) ΔH =-114.6 kJ/mol
C.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH =-38.6 kJ/mol
2NH3(g) ΔH =-38.6 kJ/mol
D.已知25℃、101kPa条件下:4Al(s)+3O2(g)=2Al2O3(s) ΔH =-2834.9 kJ/mol,4Al(s)+2O3(g)=2Al2O3(s) ΔH =-3119.1 kJ/mol,则O2比O3稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com