
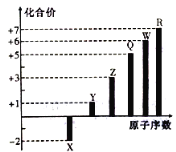
【题目】短周期元素X、Y、Z、Q、W、R的原子序数与其常见化合价关系如图所示。下列说法正确的是
A.X、Y、Z、W、R的简单离子半径大小顺序为R>W>Z>Y>X
B.Q元素形成的可溶性盐的溶液不可能显酸性
C.X、Y、R形成的某种化合物可以用于漂白、消毒
D.Y、Z和W三者最高价氧化物对应的水化物间不能两两相互反应
【答案】C
【解析】
短周期元素X、Y、Z、Q、W、R,且原子序数依次增大,通过图像可知,X只有-2价,可确定为O元素;Y、Z、Q、W、R,则为第三周期元素,Y化合价为+1,为Na元素;Z化合价+3为Al;Q最高化合价为+5为P元素;W为S元素;R为Cl元素。
A. X、Y、Z的离子具有相同的核外电子排布,且核外有2个电子层;W、R的离子具有相同的核外电子排布,且核外有3个电子层。具有相同的核外电子排布的离子,原子序数越大,半径越小;电子层数越多,半径越大,可知简单离子半径大小顺序为W>R>X>Y>Z,A不正确;
B.P元素形成的NaH2PO4,溶液显酸性,B错误;
C. X、Y、R形成的化合物中,NaClO可用作杀菌消毒的试剂,C正确;
D.Na、Al、S的最高价氧化物对应的水化物分别为NaOH、Al(OH)3、H2SO4.Al(OH)3为两性氢氧化物,既能与酸反应,又能与强碱反应,可两两反应,D错误;
答案为C


科目:高中化学 来源: 题型:
【题目】有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
(1)称取A9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。则A的相对分子质量为:___。
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。则A的分子式为:___。
(3)另取A9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。用结构简式表示A中含有的官能团为:___、__。
(4)A的核磁共振氢谱如图:则A中含有___种氢原子。
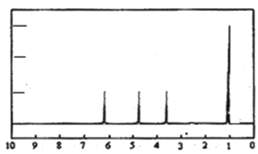
(5)综上所述,A的结构简式为___,跟NaHCO3溶液反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是非甾体雄激素物质,可通过以下方法合成:
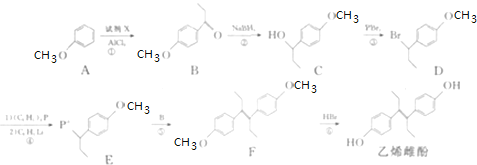
![]() 化合物B中的含氧官能团为 ______
化合物B中的含氧官能团为 ______ ![]() 填名称
填名称![]() ;
;
![]() 反应
反应![]() 中加入的试剂X的分子式为
中加入的试剂X的分子式为![]() ,X的结构简式为 ______ ;
,X的结构简式为 ______ ;
![]() 上述反应
上述反应![]() 、
、![]() 、
、![]() 、
、![]() 中,属于取代反应的是 ______
中,属于取代反应的是 ______ ![]() 填序号
填序号![]() ;
;
![]() 的一种同分异构体满足下列条件:
的一种同分异构体满足下列条件:
![]() 能发生银镜反应,其水解产物之一能与
能发生银镜反应,其水解产物之一能与![]() 溶液发生显色反应;
溶液发生显色反应;
![]() 核磁共振氢谱有4个峰.该同分异构体的结构简式为 ______
核磁共振氢谱有4个峰.该同分异构体的结构简式为 ______ ![]() 任写一种
任写一种![]() .
.
![]() 化合物
化合物![]() 可由
可由![]() 经五步反应合成:
经五步反应合成:
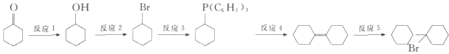
反应3的试剂为 ______ ![]()
![]() ;
;
反应2的化学方程为 ______ ;
反应5的化学方程式为: ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏合香醇可以用作食用香精,其结构简式如图1所示.
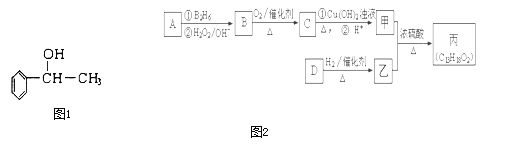
已知:R-CH=CH2 ![]() R-CH2CH2OH
R-CH2CH2OH
![]() 一
一![]() 苏合香醇的分子式为 ______ ,它不能发生的有机反应类型有
苏合香醇的分子式为 ______ ,它不能发生的有机反应类型有![]() 填数字序号
填数字序号![]() ______ .
______ .
![]() 取代反应
取代反应![]() 加成反应
加成反应![]() 消去反应
消去反应![]() 加聚反应
加聚反应![]() 氧化反应
氧化反应![]() 水解反应,
水解反应,
![]() 二
二![]() 有机物丙是一种香料,其合成路线如图
有机物丙是一种香料,其合成路线如图![]() 其中甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物.
其中甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物.
![]() 按照系统命名法,A的名称是 ______ .
按照系统命名法,A的名称是 ______ .
![]() 与新制
与新制![]() 悬浊液反应的化学方程式为 ______ .
悬浊液反应的化学方程式为 ______ .
![]() 丙中含有两个
丙中含有两个![]() ,D可发生银镜反应,在催化剂存在下1molD与2mol
,D可发生银镜反应,在催化剂存在下1molD与2mol![]() 可以反应生成乙,则D的结构简式为 ______ .
可以反应生成乙,则D的结构简式为 ______ .
![]() 甲与乙反应的化学方程式为 ______ .
甲与乙反应的化学方程式为 ______ .
![]() 苯环上有3个取代基或官能团,且显弱酸性的乙的同分异构体共有 _____ 种,其中3个取代基或官能团互不相邻的有机物结构简式为 ______ .
苯环上有3个取代基或官能团,且显弱酸性的乙的同分异构体共有 _____ 种,其中3个取代基或官能团互不相邻的有机物结构简式为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题。
(1)CS2是一种常用的溶剂,CS2的分子中存在________个σ键。在H—S、H—Cl两种共价键中,键的极性较强的是______,键长较长的是_____。
(2)氢的氧化物与碳的氧化物中,分子极性较小的是________(填分子式)。
(3)醋酸的球棍模型如图1所示。
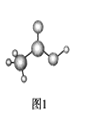
①在醋酸中,碳原子的轨道杂化类型有________;
②Cu的水合醋酸盐晶体局部结构如图2所示,该晶体中含有的化学键是________(填选项字母)。
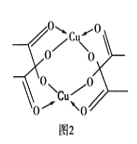
A.极性键 B.非极性键 C.配位键 D.金属键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述中,正确的说法有几项 ( )

①Mg(s)所具有的能量高于MgX2(s)所具有的能量
②MgCl2电解制Mg(s)和Cl2(g)是吸热过程
③热稳定性:MgI2>MgBr2>MgCl2>MgF2
④常温下氧化性:F2<Cl2<Br2<I2
A. 1项 B. 2项
C. 3项 D. 4项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应:2Ag+ + Cu = Cu2+ + 2Ag,设计如图所示原电池,下列说法错误的是( )。
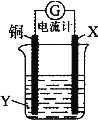
A.X可以是银或石墨
B.Y是硫酸铜溶液
C.电子从铜电极经外电路流向X电极
D.X极上的电极反应式为Ag+ + e-= Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锶是重要的化工基础原料,由工业级硝酸锶(含有Ba2+、Ca2+、Mg2+等杂质)制备分析纯碳酸锶的工艺流程如下:
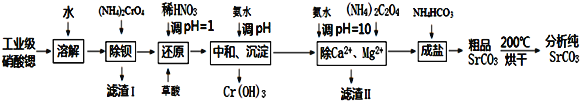
已知:①BaCrO4不溶于水,在水溶液中Cr2O72-与Ba2+不能结合。
②常温下,各物质的溶积常数如下表所示:
化合物 | Ca(OH)2 | CaC2O4 | Mg(OH)2 | MgC2O4 | Cr(OH)3 |
Ksp近似值 | 5.0×10-6 | 2.2×10-9 | 5.6×10-12 | 4.8×10-6 | 10-30 |
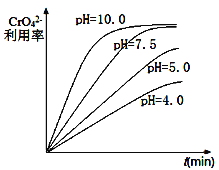
(1)“除钡”过程中CrO42-在不同pH时的利用率随时间变化曲线如下图所示,根据图像分析“除钡”过程中需要调节pH=7.5的原因_______________________________。
(2)“还原”过程中,应先调节pH=1.0,再加入草酸,加入草酸时发生反应的离子方程式为_____________________________。
(3)“滤渣Ⅱ”的主要成分为________________。
(4)“除Ca2+、Mg2+”后得到的滤液中除含有Sr(NO3)2外还含有过量的NH3·H2O,则“成盐”过程中发生反应的离子方程式为__________________________。
(5)“粗品SrCO3”烘干过程中除去的主要杂质为_____________________。
(6)在“中和、沉淀”步骤中,假定开始Cr3+,Zn3+浓度为0.1mol/L,调节至pH为_______时,铬开始沉淀;继续加碱调节至pH为_____时,铬刚好完全沉淀(离子浓度小于1×10-6mol/L时,即可认为该离子沉淀完全)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家发现,在常温常压与可见光照射下,N2与H2O在水滑石(LDH)表面发生反应:2N2(g) + 6H2O(g) ![]() 4NH3(g) + 3O2(g) – Q(Q>0)。关于该过程的说法错误的是
4NH3(g) + 3O2(g) – Q(Q>0)。关于该过程的说法错误的是
A.属于固氮过程
B.太阳能转化为化学能
C.反应物的总能量高于生成物的总能量
D.反应物的总键能高于生成物的总键能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com