
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述中,正确的说法有几项 ( )

①Mg(s)所具有的能量高于MgX2(s)所具有的能量
②MgCl2电解制Mg(s)和Cl2(g)是吸热过程
③热稳定性:MgI2>MgBr2>MgCl2>MgF2
④常温下氧化性:F2<Cl2<Br2<I2
A. 1项 B. 2项
C. 3项 D. 4项
【答案】A
【解析】分析:①依据图象分析判断,Mg(s)与X2(g)的能量高于MgX2(s),据此分析;
②MgCl2(s)的能量低于Mg(s)与Cl2(g);
③物质能量越高越活泼,越不稳定;
④根据元素周期律分析。
详解:①根据图像可知,Mg(s)与X2(g)的能量高于MgX2(s),但Mg(s)所具有的能量不一定高于MgX2(s)所具有的能量,①错误;
②MgCl2(s)的能量低于Mg(s)与Cl2(g),所以依据能量守恒判断由MgCl2制取Mg的反应是吸热反应,②正确;
③物质的能量越低越稳定,根据图象数据分析,化合物的热稳定性顺序为:MgI2<MgBr2<MgCl2<MgF2,③错误;
④同主族从上到下非金属性逐渐减弱,则氧化性:F2>Cl2>Br2>I2,④错误;答案选A。


科目:高中化学 来源: 题型:
【题目】利用水热和有机溶剂等软化学方法,可合成出含有有机杂化锌、锗以及砷等金属的硒化物,且该硒化物具有离子交换、催化、吸附、半导体等性能,显示出良好的应用前景。回答下列问题:
(1)锌基态原子核外电子排布式为:___________________。
(2)元素锗与砷中,第一电离能较大的是:___________________(填元素符号)。
(3)SeO32-离子中Se原子的杂化形式为:_____________,气态SeO3分子的立体构型为:__________,与SeO3互为等电子体的一种离子为:_________________。(填离子符号)。
(4)硒化锌是一种重要的半导体材料,其晶胞结构如下图所示(a代表Zn,b代表Se),该晶胞中Se原子周围与之紧邻的其他Se原子数为:_______________________。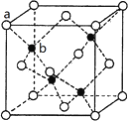
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某些植物树叶提取的挥发油中含有下列主要成分: 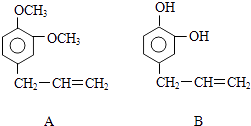
(1)写出A的分子式 .
(2)1molB与溴水充分反应,需消耗mol单质溴 .
(3)写出A与B在一定条件下相互反应,生成高分子化合物的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中A、C、D、E为短周期元素,最外层电子数之和为23,下列说法正确的是
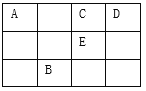
A. 元素A对应的氢化物,常温下一定是气态
B. 元素B、E的原子序数相差19
C. 与金属钠的反应中,1molC原子和1molE原子得电子数目一定相等
D. A、C、D均可形成18e-分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是:
A. 标准状况下,VL气态烯烃(CnH2n)含中子的数目为![]()
B. 1LFe2(SO4)3溶液中,若c(Fe3+)=2 molL-1,则SO42-的数目为3NA
C. 一定量的硝酸和铁粉反应放出0.5mol气体,则转移的电子数一定是1.5NA
D. 46g甲酸含H-O键的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )
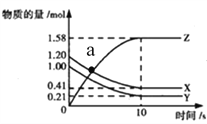
A. 反应的化学方程式为X(g)+Y(g)===Z(g)
B. a点正、逆反应速率相等
C. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
D. 反应开始到10s,Y转化率为79%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的原理为N2(g)+3H2(g)![]() 2NH3(g),请回答下列问题:
2NH3(g),请回答下列问题:
(1)已知拆开1mol H﹣H键、1mol N≡N、1mol N﹣H键分别需要吸收的能量为436kJ、946kJ、391kJ。则由N2和H2反应生成1mol NH3需要放出_________的热量。
(2)若N2、H2、NH3的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),则各物质的浓度有可能的是___________。
A.c=0.5mol/L B.b=0.5mol/L
C.c=0.4mol/L D.a=0.3mol/L
(3)若在2L密闭容器中,充入1 mol N2和3mol H2,2min时达到平衡。测得平衡时N2的浓度为0.3 mol/L。
①2min内v(NH3)=___________。
②平衡时容器的压强与起始时压强之比___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以正丁醇、溴化钠、硫酸为原料制备正溴丁烷的反应如下: NaBr+H2SO4═HBr+NaHSO4
CH3CH2CH2CH2OH+HBr ![]() CH3CH2CH2CH2Br+H2O
CH3CH2CH2CH2Br+H2O
在圆底烧瓶中加入原料,充分振荡后加入几粒沸石,安装装置Ⅰ.加热至沸腾,反应约40min.待反应液冷却后,改装为装置Ⅱ,蒸出粗产品.部分物理性质列表如下: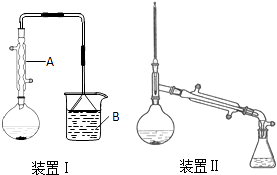
物质 | 正丁醇 | 正溴丁烷 |
沸点/℃ | 117.2 | 101.6 |
熔点/℃ | ﹣89.12 | ﹣112.4 |
密度/gcm﹣3 | 0.8098 | 1.2758 |
溶解性 | 微溶于水,溶于浓硫酸 | 不溶于水和浓硫酸 |
将所得粗产品倒入分液漏斗中,先用10mL水洗涤,除去大部分水溶性杂质,然后依次用5mL浓硫酸、10mL水、10mL饱和NaHCO3溶液、10mL水洗涤.分离出有机层,加入无水氯化钙固体,静置1h,过滤除去氯化钙,再常压蒸馏收集99~103℃馏分.
回答下列问题:
(1)仪器A的名称是 , 冷却水从A的(填“上”或“下”)口通入.
(2)在圆底烧瓶中加入的原料有:①10ml水;②7.5ml正丁醇;③10g溴化钠;④12mL浓硫酸.上述物质的加入顺序合理的是(填正确答案标号). a.①④②③b.④①②③c.③④①②
(3)烧杯B中盛有NaOH溶液,吸收的尾气主要是(填化学式).本实验使用电热套进行加热,总共使用了次.
(4)用浓硫酸洗涤粗产品时,有机层从分液漏斗(填“上口倒出”或“下口放出”).最后一次水洗主要是洗掉 .
(5)制备正溴丁烷时,不直接用装置Ⅱ边反应边蒸出产物,其原因是 .
(6)本实验得到正溴丁烷6.5g,产率为(只列式,不必计算出结果).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com