
【题目】实验室以正丁醇、溴化钠、硫酸为原料制备正溴丁烷的反应如下: NaBr+H2SO4═HBr+NaHSO4
CH3CH2CH2CH2OH+HBr ![]() CH3CH2CH2CH2Br+H2O
CH3CH2CH2CH2Br+H2O
在圆底烧瓶中加入原料,充分振荡后加入几粒沸石,安装装置Ⅰ.加热至沸腾,反应约40min.待反应液冷却后,改装为装置Ⅱ,蒸出粗产品.部分物理性质列表如下: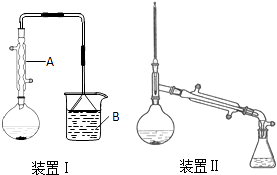
物质 | 正丁醇 | 正溴丁烷 |
沸点/℃ | 117.2 | 101.6 |
熔点/℃ | ﹣89.12 | ﹣112.4 |
密度/gcm﹣3 | 0.8098 | 1.2758 |
溶解性 | 微溶于水,溶于浓硫酸 | 不溶于水和浓硫酸 |
将所得粗产品倒入分液漏斗中,先用10mL水洗涤,除去大部分水溶性杂质,然后依次用5mL浓硫酸、10mL水、10mL饱和NaHCO3溶液、10mL水洗涤.分离出有机层,加入无水氯化钙固体,静置1h,过滤除去氯化钙,再常压蒸馏收集99~103℃馏分.
回答下列问题:
(1)仪器A的名称是 , 冷却水从A的(填“上”或“下”)口通入.
(2)在圆底烧瓶中加入的原料有:①10ml水;②7.5ml正丁醇;③10g溴化钠;④12mL浓硫酸.上述物质的加入顺序合理的是(填正确答案标号). a.①④②③b.④①②③c.③④①②
(3)烧杯B中盛有NaOH溶液,吸收的尾气主要是(填化学式).本实验使用电热套进行加热,总共使用了次.
(4)用浓硫酸洗涤粗产品时,有机层从分液漏斗(填“上口倒出”或“下口放出”).最后一次水洗主要是洗掉 .
(5)制备正溴丁烷时,不直接用装置Ⅱ边反应边蒸出产物,其原因是 .
(6)本实验得到正溴丁烷6.5g,产率为(只列式,不必计算出结果).
【答案】
(1)球形冷凝管;下
(2)a
(3)HBr;3
(4)上口倒出;有机物中少量的碳酸氢钠
(5)正丁醇、正溴丁烷的沸点相差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出,使产率降低
(6)![]() ×100%
×100%
【解析】解:(1)根据仪器a的结构特征,可知仪器a是球形冷凝管,冷凝管充满冷凝水充分冷却,冷却水从A的下口通入,
故答案为:球形冷凝管;下;(2)浓硫酸稀释时,必须将浓硫酸慢慢倒入水中,冷却后加入丁醇,减少挥发,最后加入NaBr,
故选:a;(3)正丁醇、溴化钠、硫酸反应时,会有挥发出来的HBr,用氢氧化钠溶液吸收,实验中在反应生成CH3CH2CH2CH2Br时要加热,装置Ⅱ蒸出粗产品需要加热,粗产品洗涤、分液后分离出有机层,加入无水氯化钙固体后常压蒸馏收集99~103℃馏分,也需要加热,所以共有三次用电热套进行加热,
故答案为:HBr;3;(4)有机层的密度小于浓硫酸,所以有机层在上层,要从分液漏斗上口倒出,按实验步骤可知,最后一次水洗主要是除去有机物中少量的碳酸氢钠,
故答案为:上口倒出;有机物中少量的碳酸氢钠;(5)正丁醇、正溴丁烷的沸点相差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出,使产率降低,所以制备正溴丁烷时,不直接用装置Ⅱ边反应边蒸出产物,
故答案为:正丁醇、正溴丁烷的沸点相差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出,使产率降低;(6)7.5ml正丁醇的物质的量为 ![]() mol=0.082mol,10g溴化钠的物质的量为
mol=0.082mol,10g溴化钠的物质的量为 ![]() mol=0.097mol,根据反应NaBr+H2SO4═HBr+NaHSO4、CH3CH2CH2CH2OH+HBr
mol=0.097mol,根据反应NaBr+H2SO4═HBr+NaHSO4、CH3CH2CH2CH2OH+HBr ![]() CH3CH2CH2CH2Br+H2O可知,是正丁醇不足量,则正溴丁烷理论产量为7.5×0.8098×
CH3CH2CH2CH2Br+H2O可知,是正丁醇不足量,则正溴丁烷理论产量为7.5×0.8098× ![]() g,故产率=[6.6g÷(7.5×0.8098×
g,故产率=[6.6g÷(7.5×0.8098× ![]() g)]×100%=
g)]×100%= ![]() ×100%,
×100%,
故答案为: ![]() ×100%.
×100%.
(1)根据装置图可知仪器A名称,冷凝管充满冷凝水充分冷却,逆流冷却效果好;(2)浓硫酸稀释时,必须将浓硫酸慢慢倒入水中,冷却后加入丁醇,减少挥发,最后加入NaBr;(3)正丁醇、溴化钠、硫酸反应时,会有挥发出来的溴化氢,用氢氧化钠溶液吸收;实验中在反应生成CH3CH2CH2CH2Br时要加热,装置Ⅱ蒸出粗产品需要加热,粗产品洗涤、分液后分离出有机层,加入无水氯化钙固体后常压蒸馏收集99~103℃馏分,也需要加热;(4)有机层的密度小于浓硫酸,有机层在上层;最后一次水洗主要是除去有机物中少量的碳酸氢钠;(5)正丁醇、正溴丁烷的沸点相差较小;(6)7.5ml正丁醇的物质的量为 ![]() mol=0.082mol,10g溴化钠的物质的量为
mol=0.082mol,10g溴化钠的物质的量为 ![]() mol=0.097mol,根据反应NaBr+H2SO4═HBr+NaHSO4、CH3CH2CH2CH2OH+HBr
mol=0.097mol,根据反应NaBr+H2SO4═HBr+NaHSO4、CH3CH2CH2CH2OH+HBr ![]() CH3CH2CH2CH2Br+H2O可知,是正丁醇不足量,根据正丁醇的质量计算正溴丁烷理论产量,产率=(实际产量÷理论产量)×100%.
CH3CH2CH2CH2Br+H2O可知,是正丁醇不足量,根据正丁醇的质量计算正溴丁烷理论产量,产率=(实际产量÷理论产量)×100%.


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述中,正确的说法有几项 ( )

①Mg(s)所具有的能量高于MgX2(s)所具有的能量
②MgCl2电解制Mg(s)和Cl2(g)是吸热过程
③热稳定性:MgI2>MgBr2>MgCl2>MgF2
④常温下氧化性:F2<Cl2<Br2<I2
A. 1项 B. 2项
C. 3项 D. 4项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 0.4 mol Cu2S 与足量稀硝酸反应,生成 Cu(NO3)2、S、NO 和 H2O,则参加反应的硝酸 中未被还原的硝酸的物质的量为
A.2 molB.1 molC.1.6 molD.2.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号内试剂除去下列各物质中的少量杂质,不正确的是
A.乙烷中的乙烯(Br2水)B.溴苯中的溴(KI溶液)
C.乙醇中的水(CaO)D.乙酸乙酯中的乙酸(饱和Na2CO3溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应的描述正确的是
A. NaHSO4溶液与Ba(OH)2溶液混合后显中性:Ba2++2OH-+2H++SO![]() ===BaSO4↓+2H2O
===BaSO4↓+2H2O
B. 向Fe2(SO4)3溶液中通入足量Na2S溶液:2Fe3++S2-===2Fe2++S↓
C. 强碱溶液中,用次氯酸钠与Fe(OH)2反应是湿法制备高铁酸钠的最主要过程,可表示为:2ClO-+Fe(OH)2===FeO42—+2Cl-+2H+
D. 将少量二氧化碳通入次氯酸钠溶液中:CO2+H2O+2ClO-===CO32—+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①CH3OH(g)+![]() O2(g)===CO2(g)+2H2O(g) ΔH1=-a kJ·mol-1
O2(g)===CO2(g)+2H2O(g) ΔH1=-a kJ·mol-1
②CO(g)+![]() O2(g)===CO2(g) ΔH2=-b kJ·mol-1
O2(g)===CO2(g) ΔH2=-b kJ·mol-1
③H2(g)+![]() O2(g)===H2O(g) ΔH3=-c kJ·mol-1
O2(g)===H2O(g) ΔH3=-c kJ·mol-1
④H2(g)+![]() O2(g)===H2O(l) ΔH4=-d kJ·mol-1 下列叙述正确的是
O2(g)===H2O(l) ΔH4=-d kJ·mol-1 下列叙述正确的是
A. 由上述热化学方程式可知ΔH3<ΔH4
B. H2的燃烧热为d kJ·mol-1
C. CH3OH(g)===CO(g)+2H2(g) ΔH=( a- b-2c)kJ·mol-1
D. 当CO和H2的物质的量之比为1∶2时,其完全燃烧生成CO2和H2O(l)时,放出Q kJ热量,则混合气中CO的物质的量为![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用饱和氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
A.将饱和氯化铁溶液滴入蒸馏水中即可
B.将饱和氯化铁溶液滴入热水中,至溶液呈深黄色
C.将饱和氯化铁溶液滴入沸水中,继续煮沸至溶液呈红褐色
D.将饱和氯化铁溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com