
【题目】回答下列问题。
(1)CS2是一种常用的溶剂,CS2的分子中存在________个σ键。在H—S、H—Cl两种共价键中,键的极性较强的是______,键长较长的是_____。
(2)氢的氧化物与碳的氧化物中,分子极性较小的是________(填分子式)。
(3)醋酸的球棍模型如图1所示。
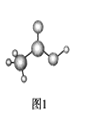
①在醋酸中,碳原子的轨道杂化类型有________;
②Cu的水合醋酸盐晶体局部结构如图2所示,该晶体中含有的化学键是________(填选项字母)。
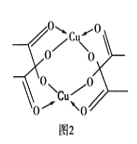
A.极性键 B.非极性键 C.配位键 D.金属键
【答案】2 H—Cl l H—S CO2 sp3、sp2 A、B、C
【解析】
(1)CS2的结构与CO2的相似,均为直线型结构,其结构简式为:S=C=S,因为一个双键由一个σ键和一个Π键组成,所以CS2的分子中存在2个σ键;因为Cl的非金属性比S的强,所以在H—S、H—Cl两种共价键中,键的极性较强的是H—Cl,因而其键长较短,所以H—S的键长较长;
(2)氢的氧化物为H2O,碳的氧化物为CO2,H2O是V形结构,CO2是直线形结构,因此分子极性较小的是CO2;
(3)①在醋酸分子中,甲基上C原子的杂化轨道类型是sp3杂化,羧基上的C原子是sp2杂化;
②根据Cu的水合醋酸盐晶体局部结构可知,该晶体中含有的化学键有碳氧之间的极性键,碳原子与碳原子之间的非极性键以及氧原子与铜原子之间的配位键,答案选ABC。


科目:高中化学 来源: 题型:
【题目】某化学课外小组用图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。

(1)写出A中反应的化学方程式_______________。
(2)观察到A中的现象是_____________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式______________________________。
(4)C中盛放CCl4的作用是________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
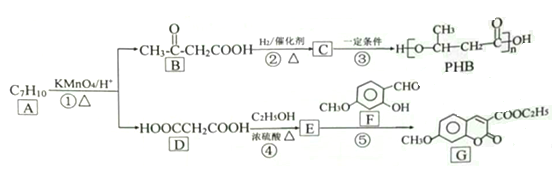
【题目】由化合物A制备一种医药合成中间体G和可降解环保塑料PHB的合成路线如下:
己知: ![]() (-R1、-R2、-R3均为烃基)
(-R1、-R2、-R3均为烃基)
回答下列问题:
(1)A的结构简式___________,G中含氧官能团的名称____________________。
(2)反应①和③的反应类型分别是_____________、________________。
(3)C存在多种同分异构体,其中分别与足量的NaHCO3溶液和Na反应产生气体的物质的量相同的同分异构体的数目为______种。
(4)写出反应③的化学方程式__________________________________
(5)写出满足下列条件的B的同分异构体_________________________
①能发生银镜反应 ②分子中烃基上的氢原子被取代后的一氯代物只有一种
(6)写出用B为起始原料制备高分子化合物![]() 的合成路线(其
的合成路线(其
他试剂任选)。____________________________________________
(7)上述合成路线中最后一步反应的化学方程式为:______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4.铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝:

下列说法中错误的是( )
A. ①②中除加试剂外,还需要进行过滤操作
B. a、b中铝元素的化合价相同
C. ③中需要通入过量的氨气
D. ④进行的操作是加热,而且d一定是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示图象中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,按试题将相应图的字母填入下列空格中,并写出所发生反应的离子方程式.

(1)表示向饱和AlCl3溶液中滴加氨水至过量的是 ______ ,离子方程式:_____ 。
(2)表示向饱和AlCl3溶液中滴加NaOH至过量的是 ______,NaOH过量时的离子方程式:_____。
(3)表示向饱和石灰水中通入CO2至过量的是 _____,CO2少量时的化学方程式:_____。
(4)表示向MgCl2和AlCl3的混合溶液中滴加NaOH溶液至过量的是 ______,Mg2+生成沉淀的离子方程式: ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、Q、W、R的原子序数与其常见化合价关系如图所示。下列说法正确的是
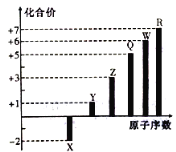
A.X、Y、Z、W、R的简单离子半径大小顺序为R>W>Z>Y>X
B.Q元素形成的可溶性盐的溶液不可能显酸性
C.X、Y、R形成的某种化合物可以用于漂白、消毒
D.Y、Z和W三者最高价氧化物对应的水化物间不能两两相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下左图所示,其中甲池的总反应式为2CH3OH+302+4KOH=2K2CO3+6H20,完成下列问题:

(1)甲池燃料电池的负极反应为___________________。
(2)写出乙池中电解总反应的化学方程式: ___________________。
(3)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生____g沉淀,此时乙池中溶液的体积为400mL,该溶液的pH=____________。
(4)某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH)2 的实验装置(如上右图)。若用于制漂白液,a 为电池的______极,电解质溶液最好用_____。若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用___作电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是__(用离子方程式表示)。向该溶液中滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将__(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为__mol·L-1。(NH3·H2O的电离平衡常数为Kb=2×10-5)
(2)如图1是0.1mol/L电解质溶液的pH随温度变化的图像。
①其中符合0.1mol/LNH4Al(SO4)2溶液的pH随温度变化的曲线是__(填写字母),导致pH随温度变化的原因是__;
②20℃时,0.1mol/L的NH4Al(SO4)2溶液中2c(SO42-)-c(NH4+)-3c(Al3+)=___(填数值)。
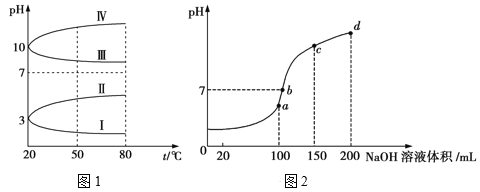
(3)室温时,向100mL0.1mol/L的NH4HSO4溶液中滴加0.1mol/LNaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是__;在b点,溶液中各离子浓度由大到小的排列顺序是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国于2007年11月成功地发射了嫦娥一号探测卫星,确定对月球土壤中14种元素的分布及含量进行探测等,月球的矿产资源极为丰富,仅月面表层![]() 厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石
厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石![]() 、斜长石
、斜长石![]() 和橄榄石
和橄榄石![]() 等,下列说法或分析不正确的是( )
等,下列说法或分析不正确的是( )
A.月球上有游离态铁是因为月球上铁的活动性比地球上铁的活动性弱
B.辉石、斜长石及橄榄石均属于硅酸盐矿
C.橄榄石中铁为![]() 价
价
D.斜长石的氧化物形式可表示为:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com