
����Ŀ������ϩ������Ǻϳ��л������ĵ��壬��ϳɷ���֮һ���£�CH3OC��CH+CH3OH+A![]() CH2=C(CH3)COOCH3������˵����ȷ���ǣ� ��
CH2=C(CH3)COOCH3������˵����ȷ���ǣ� ��
A.��֪�÷�Ӧ��ԭ��������Ϊ100%����AΪCO2
B.CH3OH���ͻ�Ϊͬϵ��
C.CH3C��CH���ϩ���������ƣ�������ʿ��Է����ӳɡ�������Ӧ
D.����NaHCO3��Ӧ��CH2=C(CH3)COOCH3��ͬ���칹����9��
���𰸡�C
��������
A. ��֪�÷�Ӧ��ԭ��������Ϊ100%�������ֻ��CH2=C(CH3)COOCH3�����������غ㶨�ɿ����ж�A��������CO2����A����ȷ��
B. CH3OHΪ�״�������Ϊ�����������������Ĺ����ŵ���Ŀ��ͬ�����Բ���ͬϵ���B����ȷ��
C. ��ϩ���в�����˫�����ܷ����ӳɷ�Ӧ��������Ӧ��CH3C��CHҲ�ܷ����ӳɷ�Ӧ��������Ӧ������CH3C��CH���ϩ���������ƣ���C��ȷ��
D. ����NaHCO3��Ӧ��CH2=C(CH3)COOCH3��ͬ���칹���������ᣬ�����г���COOH�⣬������C4H7����C4H7�����Ƕ�ϩ������ϩ����8�ֽṹ�����п����ǻ������ͼ������������3�ֽṹ�������Ը�ͬ���칹����12�֣���D����ȷ��
����ѡC��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D����Ԫ��ԭ��������������AԪ�����ڲ��������ĵ�������ͬ��BԪ��L���K���������5����CԪ�ص�+3�������Ӻ���ԭ�Ӿ�����ͬ�ĵ�������DԪ�ص�ԭ�Ӻ�����4�����Ӳ㣬K���L�������֮�͵���M����N�������֮�͡�д����
��1��Ԫ�ط��ţ�A_____________B____________C___________D__________________
��2��A��ԭ�ӽṹʾ��ͼ____________��B���ӵĵ���ʽ____________��C�����ӽṹʾ��ͼ________________��Dԭ�ӵĵ���ʽ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��g��+2B��g��![]() C��g��+D��g�� ��H��0��һ���¶��£�2molA��2molB��2L�ܱ������з�Ӧ��10min��ﵽƽ�⣬��ʱ����ѹǿ��Ϊԭ����4/5������������ȷ����
C��g��+D��g�� ��H��0��һ���¶��£�2molA��2molB��2L�ܱ������з�Ӧ��10min��ﵽƽ�⣬��ʱ����ѹǿ��Ϊԭ����4/5������������ȷ����
A. �ӿ�ʼ��ƽ�⣬A�ķ�Ӧ����Ϊ0.08mol��L![]() ��min
��min![]()
B. ���ŷ�Ӧ�Ľ��У����������ܶ���С
C. ���¶��£���Ӧ��ƽ�ⳣ��K=20/3
D. �ﵽƽ��ʱ��B��ת����Ϊ20��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����������У�����ǿ����ʵ��ǣ�����ţ���ͬ��__________������������ʵ���________�����ڷǵ����_____________��
�ٰ��� �ڰ�ˮ ������ �ܴ��� �����ᱵ ���Ȼ��� ���Ȼ��� �������̼ ������ ������
��2�������£�ȡ0.2 mol/L HCl��Һ��0.2mol/L MOH��Һ�������ϣ���û�Ϻ���Һ��pH=5��д��MOH�ĵ��뷽��ʽ��__________________��
��3���ס�����ƿ��ˮ��Ũ�ȷֱ�Ϊ1 molL-1��0.1 molL-1����c(OH��)�� ��c(OH��)��_________10(����ڡ��������ڡ���С�ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X������(��ͨ��)Y��Һ�����ɳ������������Y�����ʵ�����ϵ��ͼ��ʾ���±��з���ͼʾ�������

A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������![]() ����
���� ����
���� �Ⱦ�Ϊ��Ҫ���л�����ԭ�ϡ�����˵����ȷ����
�Ⱦ�Ϊ��Ҫ���л�����ԭ�ϡ�����˵����ȷ����
A. �����ơ��Ż�Ϊͬϵ��B. �����ơ��ŵ�һ�ȴ���ֱ�Ϊ2��5��3��
C. �����ơ�����ֻ����������ˮD. �����ơ��ŵ�����ԭ�Ӳ����ܴ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о����֣���Ԫ�������˵���ϸ�����ʵ��ز����Ԫ�ؿ�Ԥ����״���״��������Ҳ�ᵼ�¼�״���״���˲������������Ԫ��ʱҲҪ�ʿɶ�ֹ���Իش��������⣺
(1)FeҲ��������Ҫ�����Ԫ��֮һ����д��Fe2+�ĺ�������Ų�ʽ��________��
(2)��Alͬһ���ڵ�Na��MgԪ��Ҳ����������Ԫ�أ�Na��Mg��Al��̬ԭ�ӵ�һ�����ܵĴ�С��ϵ��________��
(3)�Ȼ������۵���194�棬���������۵���2054�棬���ǹ�ҵ�ϲ����õ�������Ȼ����ķ�����ȡ�����ʣ�������Ϊ________________________________________��
(4)F��I��ͬһ�����Ԫ�أ�BeF2��H2O����������ԭ�ӹ��ɵĹ��ۻ�������ӣ����߷����е�����ԭ��Be��O���ӻ���ʽ�ֱ�Ϊ________��________��BeF2���ӵ����幹����________��H2O���ӵ����幹����________��
(5)I2����ľ����ṹ��ͼ��ʾ���þ����к���________��I2���ӣ���þ����ľ�������Ϊacm����I2���ܶ���________________g��cm-3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��������Ͽ�֪�����£�FeCl2��O2��Ӧһ������Fe2O3����������FeC13��Cl2����С��ͬѧ��������װ�öԸ÷�Ӧ����̽�����ش��������⣺
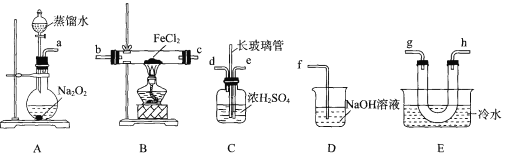
�������ϣ�FeCl2�������ɫ���۵�Ϊ674�棬�е�Ϊ1023�棻FeC13��100������������
(l)װ��A��ʢ������ˮ����������Ϊ____��
(2)�����������ҵ�˳������װ�ú���������˳��Ϊ____(�������ӿڵ�Сд��ĸ)��
(3)װ��C��Ũ���������Ϊ ___���������ܵ�����Ϊ ___ ��
(4)ʵ���������D��������Һ���ʵ��֤���˷�Ӧ��Cl2���� ___��
(5)ʵ������У�B��Ӳ�ʲ������е�����Ϊ ___��װ��E����ˮ������Ϊ ____��
(6)������ʵ���֪�������£�FeCl2��O2��Ӧ�Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӵ�ͭ������������(��Ҫ����Cu2Te)����ȡ���ڵ�һ�ֹ���������ͼ��(��֪TeO2����ˮ��������ǿ���ǿ��) �����й�˵����ȷ����

A. ������������ʱΪʹ��Ԫ�س�����֣�Ӧ�������������
B. �����ˡ��õ��IJ�����������Һ©�����ձ���������
C. ����ԭ��ʱ���������ӷ���ʽΪ2SO32-+Te4++4OH-=Te��+2SO42-+2H2O
D. �жϴ���ϴ���ķ�����ȡ�������һ��ϴ��Һ������BaCl2��Һ��û�а�ɫ��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com