
【题目】已知A(g)+B(g)C(g)+D(s)反应的平衡常数与温度的关系如下:
温度℃ | 700 | 800 | 880 | 1000 | 1200 |
平衡常数 | 1.0 | 10.0 | 12.5 | 16.1 | 17.7 |
回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“>、<、或=”);
(2)800℃时,向一个5L的密闭容器中充入0.4molA和0.7molB,若反应初始2mim内A的平均反应速率为0.01molL﹣1min﹣1 , 则2min时c(A)=molL﹣1 , C的物质的量为mol;若经过一段时间后,反应达到平衡时再向容器中充入0.4molA,则再次达到平衡后A的百分含量与第一次平衡相比(填“增大”、“减小”、或“不变”)
(3)下列选项中能作为判断反应达到平衡的依据有 a.压强不随时间改变
b.v(A):v(b)=1:1
c.单位时间内消耗A和B的物质的量相等
d.C的百分含量保持不变
(4)880℃ 时,反应 C(g)+D(s)A(g)+B(g)的平衡常数的值为 .
(5)某温度时,平衡浓度符合下式:c(A).c(B)=c(C),则该此时的温度为℃.
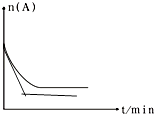
(6)图是1000℃时容器中A的物质的量的变化曲线,请在图中补画出该反应在1200℃时A的物质的量的变化曲线图 . 
【答案】
(1)![]() ;>
;>
(2)0.06;0.1;增大
(3)ad
(4)0.08
(5)700
(6)
【解析】解:(1)由A(g)+B(g)C(g)+D(s),纯固体不能代入K的表达式中,K= ![]() ,由表格数据可知,温度越高,K越大,则正反应为吸热反应,△H>0,所以答案是:
,由表格数据可知,温度越高,K越大,则正反应为吸热反应,△H>0,所以答案是: ![]() ;>;(2)800℃时,K=10.0,初始2mim内A的平均反应速率为0.01molL﹣1min﹣1 , 转化的A为0.02mol/L,则
;>;(2)800℃时,K=10.0,初始2mim内A的平均反应速率为0.01molL﹣1min﹣1 , 转化的A为0.02mol/L,则
A(g)+ | B(g) | C(g)+ D(s) | |
开始 | 0.08 | 0.14 | 0 |
转化 | 0.02 | 0.02 | 0.02 |
2min | 0.06 | 0.12 | 0.02 |
则2min时c(A)=0.06molL﹣1 , C的物质的量为0.02mol/L×5L=0.1mol;此时,Qc= ![]() =2.78<K,平衡正向移动,
=2.78<K,平衡正向移动,
A(g)+ | B(g) | C(g)+ D(s) | |
开始 | 0.08 | 0.14 | 0 |
转化 | X | x | X |
平衡 | 0.08-x | 0.14-x | X |
![]() =10,
=10,
解得x=0.04mol/L,
平衡后A的百分含量为 ![]() ×100%=22.2%,
×100%=22.2%,
反应达到平衡时再向容器中充入0.4molA,平衡正向移动,则
A(g)+ | B(g) | C(g)+ D(s) | |
开始 | 0.04+0.08 | 0.1 | 0.04 |
转化 | X | X | X |
平衡 | 0.12-x | 0.1-x | 0.04+x |
![]() =10.0,
=10.0,
解得x=0.027mol/L,
平衡时A的含量为 ![]() ×100%=39.9%,
×100%=39.9%,
则再次达到平衡后A的百分含量与第一次平衡相比增大,
所以答案是:0.06;0.1;增大;(3)a.该反应为气体体积不等的反应,压强不随时间改变,达到平衡状态,故选; b.v(A):v(b)=1:1始终存在,不能判断达到平衡状态,故不选;c.单位时间内消耗A和B的物质的量相等,只体现正反应速率关系,不能判定平衡,故不选; d.C的百分含量保持不变,可知浓度不变,为平衡状态,故选;所以答案是:ad;(4)880℃时,A(g)+B(g)C(g)+D(s)反应的平衡常数K=12.5,互为相反的两个反应的K互为倒数关系,则880℃时,反应 C(g)+D(s)A(g)+B(g)的平衡常数的值为 ![]() =0.08,所以答案是:0.08;(5)某温度时,平衡浓度符合下式:c(A).c(B)=c(C),可知K=
=0.08,所以答案是:0.08;(5)某温度时,平衡浓度符合下式:c(A).c(B)=c(C),可知K= ![]() =1,则该此时的温度为700℃,所以答案是:700;(6)升高温度,反应速率加快,平衡正向移动,平衡时A的物质的量比原平衡的小,在1200℃时A的物质的量的变化曲线图为
=1,则该此时的温度为700℃,所以答案是:700;(6)升高温度,反应速率加快,平衡正向移动,平衡时A的物质的量比原平衡的小,在1200℃时A的物质的量的变化曲线图为  ,所以答案是:
,所以答案是:  .
.
【考点精析】利用化学平衡的计算对题目进行判断即可得到答案,需要熟知反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列不属于未来化学探索空间的是( )
A. 能源和资源的合理开发
B. 合成新材料,制备新物质
C. 寻找新物种
D. 为治理环境找到快速灵敏的检测手段,并提出防护措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内含量虽然很少,却是维持正常生命活动不可缺少。这可通过下面的哪一实例得到证实
A.缺镁时叶片变黄
B.油菜缺硼时只开花不结果
C.动物血液中钙盐的含量太低会抽搐
D.缺磷会影响DNA的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示.下列判断正确的是( ) 
A.T1<T2 , p1<p2 , a+b>c,正反应为吸热反应
B.T1>T2 , p1<p2 , a+b<c,正反应为吸热反应
C.T1<T2 , p1>p2 , a+b<c,正反应为吸热反应
D.T1>T2 , p1>p2 , a+b>c,正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,1molL﹣1的NH4Cl、CH3COONH4、NH4HSO4三种溶液中,测得c(NH4+)分别为a、b、c(单位为molL﹣1),下列判断正确的是( )
A.a=b=c
B.a>b>c
C.a>c>b
D.c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列问题
(1)单质铝和氢氧化钠溶液反应的化学方程式_________________,本反应中的氧化剂是______
(2)实验室用二氧化锰和浓盐酸制取氯气的离子方程式___________________________________,本反应中的氧化剂和还原剂的物质的量比为____________
(3)二氧化硫和氯气按等物质的量通入足量水中的化学方程式_______________,本反应中若有1mol氧化剂参加反应则转移电子数为_________
(4)硫氰化钾溶液检验三价铁离子的离子方程式:______________,本反应的现象__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。
(1)煤燃烧时会产生大量的SO2,可向煤中加入_____________吸收SO2。检验脱硫后废气中是否含有SO2的简单方法是________________________________________________。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:


①由图1可知SCR技术中的氧化剂是__________________
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图3所示,脱氮效果最佳的c(NO2)/c(NO)=______。
(3)某工厂拟综合处理含NH废水和工业废气(主要含N2、Cl2、NO),设计了如下流程:

“反应2”的离子方程式为________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com