
【题目】乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心。回答下列问题:
(1)乙烷可通过热裂解和氧化裂解制取乙烯。已知下列键能数据:
化学键 | C—C | C=C | C—H | H—H |
键能/ kJ·mol -1 | 347. 7 | 615 | 413. 4 | 436. 0 |
①乙烷直接裂解制乙烯的热化学方程式为_____________________________。
②氧化裂解制乙烯的热化学方程式为C2H6(g) + ![]() O2(g) = C2H4(g) + H2O(g) △H = - 105 kJ·mol-1 . 结合①分析,氧化裂解相对热裂解生产乙烯的优点是:_____________________________________(列举1点)。
O2(g) = C2H4(g) + H2O(g) △H = - 105 kJ·mol-1 . 结合①分析,氧化裂解相对热裂解生产乙烯的优点是:_____________________________________(列举1点)。
(2)利用生物乙醇在某种分子筛催化下可脱水制取乙烯,相应反应如下:
I. C2H5OH(g) ![]() C2H4(g) + H2O(g)
C2H4(g) + H2O(g)
Ⅱ. 2C2H5OH(g) ![]() (C2H5)2O(g) + H2O(g)
(C2H5)2O(g) + H2O(g)
平衡常数[Kp是用平衡分压代替平衡浓度(平衡分压=总压×物质的量分数)]及产品选择性如下图所示:
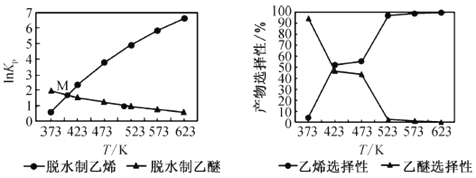
①反应 C2H5OH(g) ![]() C2H4(g) + H2O(g) 的△H______(填“>”或“<”)0。
C2H4(g) + H2O(g) 的△H______(填“>”或“<”)0。
②关于上图中交点M,下列说法正确的是________(填字母)。
a. 一段时间内,反应I、Ⅱ的速率相等
b. 某温度下,反应I、Ⅱ的平衡常数相等
c. 一段时间内,反应I、Ⅱ中乙醇的转化率相等
(3)利用煤制合成气,再由合成气间接制乙烯包含的反应有:
I. CO(g) +2H2(g) ![]() CH3OH(g) △H=a kJ·mol-1
CH3OH(g) △H=a kJ·mol-1
Ⅱ. 2CH3QH(g) ![]() C2H4(g) + 2H2O(g) △H =b kJ·mol-1
C2H4(g) + 2H2O(g) △H =b kJ·mol-1
①反应 2CO(g) + 4H2(g) ![]() C2H4(g) + 2H2O(g) △H = _________kJ·mol-1 (用 a、b表示)。
C2H4(g) + 2H2O(g) △H = _________kJ·mol-1 (用 a、b表示)。
②在容积为1 L的密闭容器中,投入2 mol CO和4 mol H2,10 min后,测得c(CO) = 1. 2 mol·L-1·min-1,则10 min内v(H2)=_____________ mol·L-1·min-1。
【答案】C2H6(g) = C2H4(g) + H2(g) △H = + 123. 5 kJ·mol-1 热裂解是吸热反应需消耗大量的能量,氧化裂解为放热反应,节省能源 > b 2a+b 0. 16
【解析】
(1) ①反应焓变△H=反应物总键能-生成物总键能;
②氧化裂解是放热反应,而热裂解是吸热反应,能量消耗不一样;
(2)①结合升高温度,平衡移动时lnKp的变化分析△H;
②图示体现的是温度对lnKp的影响;
(3) ① 已知:I. CO(g) +2H2(g) ![]() CH3OH(g) △H=a kJ·mol-1,Ⅱ. 2CH3OH(g)
CH3OH(g) △H=a kJ·mol-1,Ⅱ. 2CH3OH(g) ![]() C2H4(g) + 2H2O(g) △H =b kJ·mol-1,根据盖斯定律,I×2+Ⅱ可得反应 2CO(g) + 4H2(g)
C2H4(g) + 2H2O(g) △H =b kJ·mol-1,根据盖斯定律,I×2+Ⅱ可得反应 2CO(g) + 4H2(g) ![]() C2H4(g) + 2H2O(g),由此计算△H;
C2H4(g) + 2H2O(g),由此计算△H;
②根据v=![]() 先计算v(CO),再计算v(H2)。
先计算v(CO),再计算v(H2)。
(1)①C2H6(g)C2H4(g)+H2(g),反应焓变△H=反应物总键能-生成物总键能=413.4kJ/mol×6+347.7kJmol-(616kJ/mol+413.4kJ/mol×4+436.0kJ/mol)=+ 123. 5kJ/mol,则乙烷直接裂解制乙烯的热化学方程式为C2H6(g) = C2H4(g) + H2(g) △H = + 123. 5 kJ·mol-1;
②氧化裂解制乙烯的热化学方程式为C2H6(g) + ![]() O2(g) = C2H4(g) + H2O(g) △H = - 105 kJ·mol-1 ,而乙烷直接裂解制乙烯的热化学方程式为C2H6(g) = C2H4(g) + H2(g) △H = + 123. 5 kJ·mol-1,可见热裂解是吸热反应需消耗大量的能量,氧化裂解为放热反应,节省能源;
O2(g) = C2H4(g) + H2O(g) △H = - 105 kJ·mol-1 ,而乙烷直接裂解制乙烯的热化学方程式为C2H6(g) = C2H4(g) + H2(g) △H = + 123. 5 kJ·mol-1,可见热裂解是吸热反应需消耗大量的能量,氧化裂解为放热反应,节省能源;
(2)①由图示可知升高温度,平衡移动时lnKp的值不断增大,说明温度升高,Kp增大,即平衡正向移动,正方向为吸热反应,故△H>0;
②上图中交点M表示某温度时,反应I、Ⅱ的lnKp的值相等,即平衡常数相等,因反应I、Ⅱ的反应原理不同,无法体现乙醇的转化率是否相等和反应I、Ⅱ的速率是否相等,故答案为b;
(3)①已知:I. CO(g) +2H2(g) ![]() CH3OH(g) △H=a kJ·mol-1,Ⅱ. 2CH3OH(g)
CH3OH(g) △H=a kJ·mol-1,Ⅱ. 2CH3OH(g) ![]() C2H4(g) + 2H2O(g) △H =b kJ·mol-1,根据盖斯定律,I×2+Ⅱ可得反应 2CO(g) + 4H2(g)
C2H4(g) + 2H2O(g) △H =b kJ·mol-1,根据盖斯定律,I×2+Ⅱ可得反应 2CO(g) + 4H2(g) ![]() C2H4(g) + 2H2O(g),则△H=(a kJ·mol-1)×2+(b kJ·mol-1)=(2a+b)kJ·mol-1;
C2H4(g) + 2H2O(g),则△H=(a kJ·mol-1)×2+(b kJ·mol-1)=(2a+b)kJ·mol-1;
②在容积为1 L的密闭容器中,投入2 mol CO和4 mol H2,10 min后,测得c(CO) = 1. 2 mol·L-1·min-1,v(CO)=![]() =
=![]() =0.08 mol·L-1·min-1,则v(H2)= v(CO) ×
=0.08 mol·L-1·min-1,则v(H2)= v(CO) ×![]() =0.08 mol·L-1·min-1×2=0.16 mol·L-1·min-1。
=0.08 mol·L-1·min-1×2=0.16 mol·L-1·min-1。


科目:高中化学 来源: 题型:
【题目】下列离子检验的方法正确的是
A.某溶液中加入KSCN溶液呈红色,说明原溶液不含有Fe2+离子
B.某溶液中通入氯气,然后再加入KSCN溶液呈红色,说明原溶液中一定有Fe2+离子
C.某溶液中加入氢氧化钠溶液生成红褐色沉淀,说明原溶液中一定有Fe3+离子
D.某溶液中加入稀硫酸溶液产生无色气体,说明原溶液中一定有![]() 离子
离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物乙是一种治疗神经类疾病的药物,可由化合物甲经多步反应得到。下列有关甲、乙的说法不正确的是
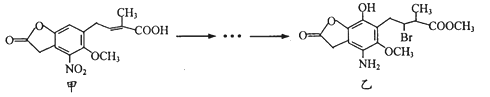
A. 甲的分子式为C14H11NO7
B. 甲和乙所含官能团均为5种
C. 可用NaHCO3溶液鉴别化合物甲和乙
D. 甲能与酸性高锰酸钾溶液反应,乙能与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化氮(NCl3)是一种消毒剂,可利用氯气与氯化铵溶液反应来制备。已知:三氯化氮的相关性质如下:
物理性质 | 化学性质 |
黄色油状液体,熔点为-40℃,沸点为 71℃,不溶于冷水、易溶于有机溶剂,密度为 1.65 gcm-3 | 95℃时爆炸,热水中发生水解 |
某小组同学选择下列装置(或仪器)设计实验制备三氯化氮并探究其性质:
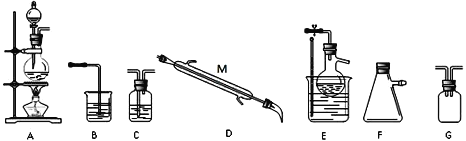
(1)NCl3的电子式为__________________;仪器 M 的名称是______________;
(2)如果气流的方向从左至右,装置连接顺序为A、G、_____________、B。(注明:F仪器使用单孔橡胶塞)
(3)C中试剂是_________________;B装置的作用是________________;
(4)写出E装置中发生反应的化学方程式_______________________________________
(5)当E装置的烧瓶中出现较多油状液体时停止反应。控制水浴加热温度为__________;
(6)已知三氯化氮不具有漂白性,三氯化氮与热水反应的化学方程式为NCl3+4H2O=NH3H2O+3HClO,请设计实验证明该水解反应的产物______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中正确的是
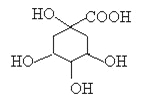
A.奎尼酸的分子式是C7H9O6
B.1mol奎尼酸与足量NaOH溶液反应,最多消耗NaOH物质的量为5mol
C.1 mol奎尼酸与足量钠反应生成56L氢气
D.奎尼酸能发生消去反应,也能与乙醇、乙酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
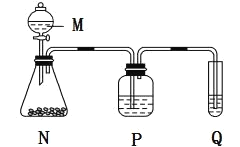
试回答下列问题:
(1)元素E在元素周期表中的位置是______。
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____,Q中观察到的实验现象是_____。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A、C、D的盐 |
b | C、D组成的化合物,且原子数之比为1∶1 |
c | 化学组成为AC2 |
①a含有的化学键有_____。
②b与c反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.已知:Na2SO3(aq)+S(s)![]() Na2S2O3(aq),实验可知该反应较慢。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
Na2S2O3(aq),实验可知该反应较慢。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
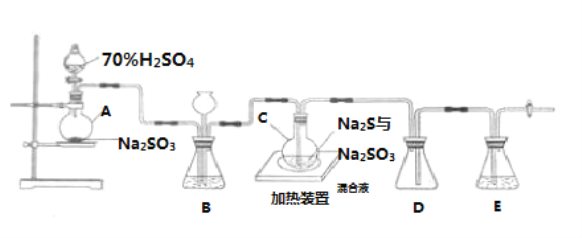
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若_______,则整个装置气密性良好。装置D的作用是______________________________________ 。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___________。
a.蒸馏水 b .饱和Na2SO3溶液
c.饱和NaHSO3溶液 d . 饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是____________。烧瓶C中反应达到终点的现象是____________________。待C中反应完成后应立即关闭分液漏斗的旋塞,原因是_______________________。
(3)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O35H2O,其中可能含有Na2SO3、Na2SO4等杂质,利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:_______________________________________________。供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法不正确的是( )
A. 实验室用H2O2分解制O2,加MnO2做催化剂后,反应速率明显加快
B. 在金属钠与足量水反应中,增加水的量能加快反应速率
C. 2SO2+O2![]() 2SO3反应中,SO2的转化率不能达到100%
2SO3反应中,SO2的转化率不能达到100%
D. 实验室用锌和盐酸反应制取氢气,用锌粉比锌粒反应要快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com