
����Ŀ����ѧ�����ͨѶ����ͨ���ճ����������Ź㷺��Ӧ�á�
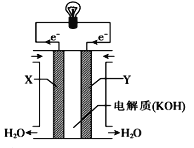
(1)��ͼΪ����ȼ�ϵ�صĹ���ʾ��ͼ���ɴ��ж�X��Ϊ��ص�_____����OH����______(���������)���������ƶ���Y���ĵ缫��Ӧ����ʽΪ________����·��ÿת��0.2mol���ӣ���״������������������������_______ L��
(2)Ϊ����֤Fe3 +��Cu2+������ǿ�������һ��װ�ã�����װ�ü��ܲ����������ܴﵽʵ��Ŀ�ĵ���__________��

(3)Ǧ�����dz����Ļ�ѧ��Դ֮һ�����硢�ŵ���ܷ�Ӧ�ǣ�2PbSO4 + 2H2O![]() Pb + PbO2 + 2H2SO4��Ǧ���طŵ�ʱ������______�������ʻ�ѧʽ�����õ缫����_____������ӡ����٣��������Һ���Ϊ2L����Ӧ������Һ����仯���Բ��ƣ����ŵ���������·��ת��3mol���ӣ�������Ũ����5mol/L�½���________mol/L��
Pb + PbO2 + 2H2SO4��Ǧ���طŵ�ʱ������______�������ʻ�ѧʽ�����õ缫����_____������ӡ����٣��������Һ���Ϊ2L����Ӧ������Һ����仯���Բ��ƣ����ŵ���������·��ת��3mol���ӣ�������Ũ����5mol/L�½���________mol/L��
���𰸡� �� �� O2��2H2O+4e��=4OH�� 1.12L B PbO2 ���� 3.5
��������(1)��������ԭ����ʧ���ӣ��Ǹ���,X��Ϊ��صĸ�����OH�����������ƶ���O2�õ��ӣ�Y���ĵ缫��Ӧ����ʽΪO2��2H2O+4e��=4OH������·��ÿת��0.2mol���ӣ���״������������������������0.2mol��22.4L��mol��1/4 =1.12L��(2)Ϊ����֤Fe3 +��Cu2+������ǿ�������ܲ����������ܴﵽʵ��Ŀ�ĵ���B��A��п��Fe3 +��Ӧ����A����B��Fe3 +��Cu��Ӧ������֤Fe3 +��Cu2+������ǿ������B��ȷ��C������Ũ���ᷴӦ����C����D�����缫��ͬ�������γ�ԭ��أ���D����ѡB��(3)PbO2����������Ǧ���طŵ�ʱ������PbO2�������ʻ�ѧʽ�����ŵ����PbSO4���õ缫�������ӡ������Һ���Ϊ2L����Ӧ������Һ����仯���Բ��ƣ���2PbSO4 + 2H2O![]() Pb + PbO2 + 2H2SO4��ÿת��2mol���ӣ�����2mol���ᣬ�ŵ���������·��ת��3mol���ӣ�����3mol���ᣬ������Ũ����5mol/L�½���
Pb + PbO2 + 2H2SO4��ÿת��2mol���ӣ�����2mol���ᣬ�ŵ���������·��ת��3mol���ӣ�����3mol���ᣬ������Ũ����5mol/L�½���![]() =3.5mol/L��
=3.5mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��ԭ���������ȷ����

A. ѡ����ʵ��Լ�����ͼ1��ʾװ�ÿɷֱ���ȡ����CO2��NO��O2
B. ��ȥ����CO2�л��е�����SO2���ɽ������������ͨ��ʢ����������KMnO4��Һ��Ũ�����ϴ��ƿ
C. ϴ�ӳ���ʱ(��ͼ2)����©���м�����ˮ��û���������裬��ˮ�˾����ظ�����
D. ����Ƶ����Һ©�������������Ȼ�̼���ã��ɽ�����ȡ�����Ȼ�̼��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������������մ����������ʳ�����ƣ�������ϴ�ӣ�����ϴ�����þߵ����۵ȡ��������������ַ������ֳ������õ�ʳ���봿��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���շ���͡��һ�ֵ���Ѫ֬��ҩ���ṹ��ʽ��ͼ��δ��ʾ����ռ乹�ͣ������й����շ���͡��������ȷ���ǣ� �� 
A.�����к���3�ֹ�����
B.�ɷ����ӳɷ�Ӧ��������Ӧ
C.��ˮ��Һ���Ȼ����ǻ����ܵ����H+
D.1mol������������1mol NaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʵ��װ���У�ʵ�鿪ʼһ��ʱ��Կ�����������������ȷ���� ( )

A��ƻ�����ɱ� B��������������С��װߡ�
C��С�Թ�����KNO3�������� D��pH��ֽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�д��ڴ�����H+��SO42����Cl�� �� ����Һ�л����ܴ������ڵ������ǣ�������
A.OH��
B.NO3��
C.Ag+
D.Ba2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ֤��ϡ������ͭ��Ӧ����������ΪNO�������ͼʵ�飨ʵ������л���2Ϊ��״̬��������˵���в���ȷ���ǣ� �� 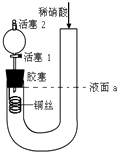
A.��װ������Լ��ȿ��Լӿ�ϡ������ͭ�ķ�Ӧ����
B.�رջ���1������ϡ������Һ��a��
C.ͨ���رջ�������1���Կ��Ʒ�Ӧ�Ľ���
D.��Ӧ��ʼ�����·�����ɫ�������ɣ�������֤��������ΪNO
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com