
【题目】某同学设计实验探究构成原电池的条件,装置如图:

实验一:实验探究电极的构成(甲图)
①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
结论一: _________________________________;
实验二:探究溶液的构成(甲图,A极用锌片,B极用铜片)
①液体采用无水乙醇,发现电流计指针不偏转。
②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生;
结论二: __________________________________________;
实验三:对比实验,探究乙图装置能否构成原电池
将锌、铜两电极分别放入稀硫酸溶液中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转.
结论三: _________________________________________ ;
思考:对该同学的实验,同学乙提出了如下疑问,请你帮助解决。
(1)在甲图装置中,若A为镁片,B为铝片,电解质溶液为NaOH溶液;负极为_______(填“A”或“B”);电流计的指针应向_______偏转(填“右”或“左”)。
(2)一根金属丝两端分别放在图乙的两个烧杯之中,电流计指针_______(填“能”或“不能”)偏转。
【答案】电极必须是两活泼性不同的电极 溶液必须是电解质溶液 必须构成闭合回路 B 右 不能
【解析】
实验一:由①②可知,当两极相同时,不能形成原电池;由③④可知,当两极是两种活泼性不同的金属或一种是金属一种是可导电的非金属时,可以形成原电池;
实验二:①中乙醇是非电解质,溶液中无自由移动离子;②中硫酸是电解质,硫酸溶液中有自由移动离子,能形成原电池;
实验三:要有电流,必须能形成闭合回路。
(1)在甲图装置中,若A为镁片,B为铝片,电解质溶液为NaOH溶液,铝与氢氧化钠溶液发生自发的氧化还原反应,所以铝是负极,镁是正极;根据Al与强碱溶液反应分析;
(2) 一根金属丝两端分别放在图乙的两个烧杯之中,不符合原电池的构成条件,电流计指针不能偏转。
实验一:由①②可知,当两极相同时,不能形成原电池;由③④可知,当两极是两种活泼性不同的金属或一种是金属一种是可导电的非金属时,可以形成原电池;
结论一:电极必须是两活泼性不同的电极;
实验二:①中乙醇是非电解质,溶液中无自由移动离子;②中硫酸是电解质,硫酸溶液中有自由移动离子,能形成原电池;结论二:溶液必须是电解质溶液;
实验三:要有电流,必须能形成闭合回路,结论三:必须构成闭合回路。
(1)在图甲装置中,若A 为镁片,B为铝片,电解质溶液为NaOH溶液,由于铝与氢氧化钠溶液发生自发的氧化还原反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,所以铝是负极,镁是正极,根据上述实验,电流计向负极偏转,即向右偏转;
(2)一根金属丝两端分别放在图乙的两个烧杯之中,不符合原电池的构成条件,没有形成闭合回路,因此电流计指针不能偏转。


科目:高中化学 来源: 题型:
【题目】按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是

A. H2 B. CH3CH2OH(气) C. CO2 D. CO和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5 mol·L-1的盐酸10mL稀释到200mL,从中取出5mL,这5 mL溶液的物质的量浓度为( )
A.0.5mol·L-1B.0.25mol·L-1
C.0.1mol·L-1D.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各组物质中,找出合适的序号填在对应的空格内:
①白磷和红磷 ②NO2和N2O4 ③12C和14C ④![]() 和
和 ![]() ⑤C60和金刚石 ⑥异戊烷和新戊烷
⑤C60和金刚石 ⑥异戊烷和新戊烷 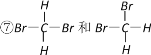
⑴互为同位素的是_____________;⑵互为同分异构体的是__________;
⑶互为同素异形体的是_________;⑷同一种物质的是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,取pH=12的NaOH溶液和氨水各10 mL,分别用蒸馏水冲稀至1 L。关于稀释后的溶液的pH的说法正确的是
A.NaOH溶液的pH小于氨水的pHB.NaOH溶液的pH大于氨水的pH
C.两溶液的pH相等D.无法判别两溶液pH的相对大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A在通常状况下是一种相对分子量为28的气体,A通过加聚反应可以得到F,F常作为食品包装袋的材料。有机物A、B、C、D、E、F有如图所示的关系:
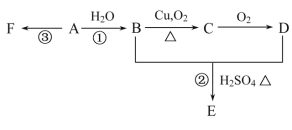
(1)A的分子式为_____,用途为____________________。
(2)写出反应①的化学方程式_____________________,该反应的类型是______。
写出反应②的化学方程式___________________,该反应的类型是_________。
写出反应③的化学方程式____________________________。
(3)写出B生成C的方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将V L气体A(摩尔质量为M g·mol-1)溶于0.1L水中,所得溶液密度为d g·cm-3,则该溶液的物质的量浓度为
A. Vd/(MV+2240)mol/LB. 1000Vd/(MV+2240)mol/L
C. VdM/(MV+2240)mol/LD. VM/22.4(V+0.1)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 ![]() 的分子式均为C8H8,下列说法不正确的是 ( )
的分子式均为C8H8,下列说法不正确的是 ( )
A. 甲、乙、丙的二氯代物数目最少的是丙
B. 甲、乙、丙中只有甲的所有原子可能处于同一平面
C. 甲、乙、丙在空气中燃烧时均产生明亮并带有浓烟的火焰
D. 等量的甲和乙分别与足量的溴水反应,消耗Br2的量:甲>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com