
【题目】化合物 ![]() 的分子式均为C8H8,下列说法不正确的是 ( )
的分子式均为C8H8,下列说法不正确的是 ( )
A. 甲、乙、丙的二氯代物数目最少的是丙
B. 甲、乙、丙中只有甲的所有原子可能处于同一平面
C. 甲、乙、丙在空气中燃烧时均产生明亮并带有浓烟的火焰
D. 等量的甲和乙分别与足量的溴水反应,消耗Br2的量:甲>乙
【答案】D
【解析】本题考查有机物的结构与性质。
A.先判断一氯代物的数目,再分析二氯代物数目;B.分子中含有饱和碳原子,所有原子不可能处于同一平面;C.含碳量与最简式相同的乙炔含碳量相同,在空气中燃烧时均产生明亮并带有浓烟的火焰;D.碳碳双键数目越多,消耗Br2的量越多。
化合物甲的一氯代物有5种,二氯代物有5+3+4+2+0=14种,化合物乙的一氯代物有2种,二氯代物有3+3=6种,化合物丙的一氯代物有1种,二氯代物有3种,A正确;化合物甲含有一个苯环和一个碳碳双键,所有原子可能处于同一平面,化合物乙和化合物丙均含有饱和碳原子,所有原子不可能处于同一平面,B正确;化合物甲、化合物乙和化合物丙的最简式为CH,与乙炔含碳量相同,则在空气中燃烧时均产生明亮并带有浓烟的火焰,C正确;化合物甲含有一个碳碳双键,1mol化合物甲消耗1mol Br2,化合物乙含有三个碳碳双键,1mol化合物乙消耗3mol Br2,D错误。
故选D。


科目:高中化学 来源: 题型:
【题目】某同学设计实验探究构成原电池的条件,装置如图:

实验一:实验探究电极的构成(甲图)
①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
结论一: _________________________________;
实验二:探究溶液的构成(甲图,A极用锌片,B极用铜片)
①液体采用无水乙醇,发现电流计指针不偏转。
②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生;
结论二: __________________________________________;
实验三:对比实验,探究乙图装置能否构成原电池
将锌、铜两电极分别放入稀硫酸溶液中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转.
结论三: _________________________________________ ;
思考:对该同学的实验,同学乙提出了如下疑问,请你帮助解决。
(1)在甲图装置中,若A为镁片,B为铝片,电解质溶液为NaOH溶液;负极为_______(填“A”或“B”);电流计的指针应向_______偏转(填“右”或“左”)。
(2)一根金属丝两端分别放在图乙的两个烧杯之中,电流计指针_______(填“能”或“不能”)偏转。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。关于该化合物的说法不正确的是( )
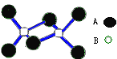
A. 化学式是Al2Cl6
B. 不存在离子键和非极性共价键
C. 在固态时所形成的晶体是分子晶体
D. 是离子化合物,在熔融状态下能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定。回答下列问题:
I.岩脑砂的制备
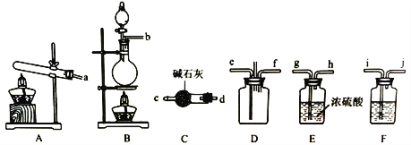
(1)该实验中用浓盐酸与二氧化锰反应制取所需氯气,写出该反应的离子方程式____________
(2)确定上述装置的合理连接顺序:a→____→ef←___(用小写字母和箭头表示,箭头方向与气流方向一致)。
(3)装置F中试剂的作用为___________
(4)装置D处有两个明显的不足之处,其中之一为:导管太细,生成的氯化铵固体可能会堵塞导管,之二为:___________。
II.岩脑砂中元素的测定:准确称取ag岩脑砂,与足量的氧化铜混合加热,利用右图装置测定岩脑砂中氮元素和氯元素的质量之比。充分加热后,G中产生红色固体,H、I装置质量增加,K中收集到无色气体。
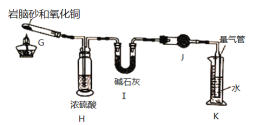
(5)写出G中发生反应的方程式______________________________________________
(6)若没有H装置,会导致测量值_____________(填“偏高”,“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1,Na2O2(s)+CO2(g)===Na2CO3(s)+![]() O2(g) ΔH=-226 kJ·mol-1,根据以上热化学方程式判断,下列说法正确的是( )。
O2(g) ΔH=-226 kJ·mol-1,根据以上热化学方程式判断,下列说法正确的是( )。
A. CO的燃烧热为283 kJ
B. 下图可表示由CO生成CO2的反应过程和能量关系
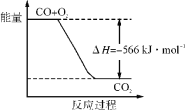
C. 2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,转移电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质结构和化学用语的说法正确的是( )
A. 39 g Na2O2晶体中所含阴、阳离子总数为2NA
B. 1个氮气分子中存在3对共用电子对
C. NaOH和Na2O中所含的化学键类型完全相同
D. AlCl3和MgF2中都含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。 下列说法正确的是 ( )
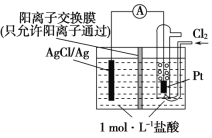
A. 正极反应为AgCl+e-=Ag+Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.02 mol e- 时,交换膜左侧溶液中约减少0.04 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:

已知:AlCl3、FeCl3分别在183 ℃、315 ℃时升华
(1)铝原子的结构示意图为________,实验室配制氯化铝溶液时加入盐酸的目的是________________________。
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为______________________炉气中残余有少量Cl2,请画出吸收Cl2的尾气装置图_____。

(3)700 ℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围________________。
a.低于183 ℃ b.介于183 ℃和315 ℃之间 c.高于315 ℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
m克样品![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)3
Al(OH)3![]() n克Al2O3
n克Al2O3
NaAlO2溶液与过量二氧化碳反应的离子方程式为:______________________。计算该样品中Al的质量分数________(结果用m、n表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2—氯丁烷(![]() )与NaOH乙醇溶液共热发生消去HCl分子的反应
)与NaOH乙醇溶液共热发生消去HCl分子的反应
C. 甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D. 2—丙醇一定条件下发生消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com