
【题目】某化学兴趣小组设计了一系列实验,根据具体实验回答下列问题:
Ⅰ.制取![]()
化学反应方程式为![]() 。
。
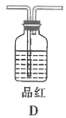
(1)根据实验需要,下列![]() 装置中___________(填序号)最适合制备
装置中___________(填序号)最适合制备![]() 。
。

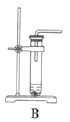
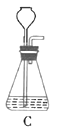

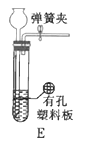
(2)在实验中发现,![]() 气体产生缓慢,但又不存在气密性问题,分析可能的原因:____________、_________________。(任写两条)
气体产生缓慢,但又不存在气密性问题,分析可能的原因:____________、_________________。(任写两条)
Ⅱ.制取![]() 、
、![]() 混合气体并验证(实验装置如图所示)
混合气体并验证(实验装置如图所示)
化学反应方程式为![]() 。
。

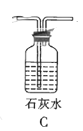
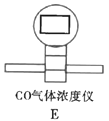
(3)根据实验需要,请从下列![]() 装置中选择最适合的装置并将其序号填在下面的空格中:Ⅰ、Ⅱ处连接的装置分别是________________、________________。上图中装水的洗气瓶的作用是___________。
装置中选择最适合的装置并将其序号填在下面的空格中:Ⅰ、Ⅱ处连接的装置分别是________________、________________。上图中装水的洗气瓶的作用是___________。

Ⅲ.测定样品中![]() 的含量
的含量
(4)某草酸亚铁样品中含有少量硫酸亚铁,设计用滴定法测定该样品中![]() 的含量,滴定反应为
的含量,滴定反应为![]() 。
。
实验方案设计如下:
①将准确称量的ag草酸亚铁样品置于![]() 锥形瓶内,加入适量
锥形瓶内,加入适量![]() 的
的![]() 溶解,加热至70℃左右,立即用浓度为
溶解,加热至70℃左右,立即用浓度为![]() 的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液
的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液![]() 。
。
②向上述滴定混合液中加入适量的![]() 粉和过量的
粉和过量的![]() 的
的![]() 溶液,煮沸(不含
溶液,煮沸(不含![]() ),继续用
),继续用![]() 的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液
的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液![]() 。回答下列问题:
。回答下列问题:
步骤②中检验溶液不含![]() 的操作为取1滴煮沸后的溶液滴入装有___________________溶液的试管中,若_______,则说明溶液不含
的操作为取1滴煮沸后的溶液滴入装有___________________溶液的试管中,若_______,则说明溶液不含![]() 。计算
。计算![]() (
(![]() 的摩尔质量为
的摩尔质量为![]() )的质量分数为__________%。(用含
)的质量分数为__________%。(用含![]() 的式子表示)
的式子表示)
【答案】D 浓硫酸的浓度过低 ![]() 变质 C E 收集一氧化碳,防止污染空气 KSCN溶液 无明显现象或溶液不变红
变质 C E 收集一氧化碳,防止污染空气 KSCN溶液 无明显现象或溶液不变红 ![]()
【解析】
Ⅰ制取![]() :该反应是固液混合不加热型;反应速率过慢,装置气密性没有问题,则是反应物本身的问题;Ⅱ制取
:该反应是固液混合不加热型;反应速率过慢,装置气密性没有问题,则是反应物本身的问题;Ⅱ制取![]() 、
、![]() 混合气体并验证:先通氮气,排除装置内的空气,产生的气体先通过澄清石灰水检验
混合气体并验证:先通氮气,排除装置内的空气,产生的气体先通过澄清石灰水检验![]() ,碱石灰除去CO2并干燥气体,再通过CO浓度仪则可检验,最后的水是收集
,碱石灰除去CO2并干燥气体,再通过CO浓度仪则可检验,最后的水是收集![]() ,防止污染空气;Ⅲ测定样品中
,防止污染空气;Ⅲ测定样品中![]() 的含量:某草酸亚铁样品中含有少量硫酸亚铁,故测定该样品中
的含量:某草酸亚铁样品中含有少量硫酸亚铁,故测定该样品中![]() 的含量,需要根据
的含量,需要根据![]() 的消耗量来计算,
的消耗量来计算,![]() 、
、![]() 均会被高锰酸钾氧化,实验②中无
均会被高锰酸钾氧化,实验②中无![]() ,则实验①是
,则实验①是![]() 与
与![]() 反应,反应②是
反应,反应②是![]() 与
与![]() 反应,再根据高锰酸钾的消耗量与
反应,再根据高锰酸钾的消耗量与![]() 的关系式求解。
的关系式求解。
(1)制取![]() 的方程式:
的方程式: ![]() ,该反应属于固液混合不加热型,最佳反应装置为D;
,该反应属于固液混合不加热型,最佳反应装置为D;
故答案为:D;
(2)在实验中发现,![]() 气体产生缓慢,但又不存在气密性问题,故是反应物本身的问题,可能是浓硫酸的浓度过低或
气体产生缓慢,但又不存在气密性问题,故是反应物本身的问题,可能是浓硫酸的浓度过低或![]() 变质;
变质;
故答案为:浓硫酸的浓度过低;![]() 变质;
变质;
(3)先通氮气,排除装置内的空气,产生的气体先通过澄清石灰水检验![]() ,碱石灰除去CO2并干燥气体,再通过CO浓度仪则可检验,最后的水是收集
,碱石灰除去CO2并干燥气体,再通过CO浓度仪则可检验,最后的水是收集![]() ,防止污染空气;
,防止污染空气;
故答案为:C;E;收集CO,防止污染空气;
(4)检验溶液是否含![]() ,可取1滴煮沸后的溶液滴入KSCN溶液中,观察溶液是否变血红色,此处是不含
,可取1滴煮沸后的溶液滴入KSCN溶液中,观察溶液是否变血红色,此处是不含![]() ,故无明显变化;根据氧化还原反应可知:
,故无明显变化;根据氧化还原反应可知:![]() ,实验②中无
,实验②中无![]() ,则实验①是
,则实验①是![]() 与
与![]() 反应,反应②是
反应,反应②是![]() 与
与![]() 反应,根据实验①来计算:
反应,根据实验①来计算:![]() ,则对应消耗的
,则对应消耗的![]() 为:
为:![]() ,故
,故![]() (
(![]() 的摩尔质量为
的摩尔质量为![]() )的质量分数=
)的质量分数=![]() ;
;
故答案为:KSCN溶液;无明显现象或溶液不变红;![]() 。
。


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是

A. Ⅰ附近溶液pH降低
B. Ⅳ附近很快生成铁锈
C. Ⅲ附近产生黄绿色气体
D. Ⅱ附近很快出现蓝色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋酸钠是一种化学物质,浅黄色或褐色的无定形粉末,不溶于水,常用于锰离子的检验,其有一种制备流程如图:
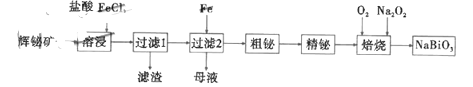
已知:a.辉铋矿(主要成分是![]() ,还含少量
,还含少量![]() 等杂质);
等杂质);
b.水解能力:![]() 。
。
回答下列问题:
(1)制备流程中,溶浸时加入过量的浓盐酸的作用是__________________________。
(2)溶浸时,为了提高浸取速率,可以采取的措施是_____________(填序号)。
a.加入足量的蒸馏水
b.搅拌
c.粉碎矿石
d.升髙温度
(3)过滤2所得“母液”中经过通入气体![]() 后可再循环利用,气体
后可再循环利用,气体![]() 最好是__________(填化学式)。
最好是__________(填化学式)。
(4)写出焙烧时生成铋酸钠的化学方程式:__________________________________,当消耗标准状况下![]() 时,转移电子的数目是________________。
时,转移电子的数目是________________。
(5)铋酸钠(![]() )可用于锰离子(
)可用于锰离子(![]() )的检验,如将铋酸钠固体加入到足量稀硫酸和硫酸锰
)的检验,如将铋酸钠固体加入到足量稀硫酸和硫酸锰![]() 的混合溶液中并加热,可得紫色溶液(
的混合溶液中并加热,可得紫色溶液(![]() 无色),此反应的离子方程式为_________。
无色),此反应的离子方程式为_________。
(6)25℃时,向浓度均为![]() 的
的![]() 、
、![]() 、
、![]() 的混合溶液中滴加
的混合溶液中滴加![]() 溶液(设溶液体积变化不计),当
溶液(设溶液体积变化不计),当![]() 开始沉淀时,所得悬浊液中
开始沉淀时,所得悬浊液中![]() _________。[已知:
_________。[已知:![]()
![]() 、
、![]() 、
、![]() ]
]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是

A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:

(1)b极上的电极反应式为__,甲电池的总反应化学方程式是__。
(2)在粗铜的电解过程中,图中c电极的材料是__(填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为__;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是__,电解一段时间后,电解液中的金属离子有__。
(3)如果要在铁制品上镀镍(二价金属,相对原子质量59),则f电极的材料是__(填“铁制品”或“镍块”,下同),e电极的材料是__。
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )
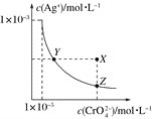
A.t℃时,Ag2CrO4的Ksp为1×10-8
B.饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.t℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t℃时,将0.01 mol·L-1AgNO3溶液滴入20 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液中,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(如图所示)可用于制备各种高性能防腐蚀涂料。W、X、Y、Z是原子序数依次增大的短周期主族元素,且占据三个不同周期,W与Z的质子数之和是X的2倍。下列说法不正确的是
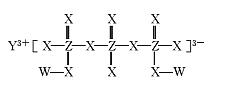
A.原子半径:Y>Z>X
B.X元素的族序数是Y元素的2倍
C.工业上电解熔融Y2X3化合物制备单质Y
D.W与X形成的所有化合物都只含极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1 mol丙酮酸![]() 在镍催化剂作用下加1 mol氢气转化变成乳酸。乳酸的结构简式为_________________________________________。
在镍催化剂作用下加1 mol氢气转化变成乳酸。乳酸的结构简式为_________________________________________。
(2)与乳酸具有相同官能团的乳酸的同分异构体A在酸性条件下,加热失水生成B,由A生成B的化学反应方程式是_________________________________
(3)B的甲酯可以聚合,聚合物的结构简式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2是重要的耐高温材料,可用作陶瓷遮光剂。天然锆英石的主要成分为ZrSiO4,另外还含有铁、铝、铜等金属元素的氧化物杂质,工业上以天然锆英石为原料制备ZrO2的工艺流程如下图所示:
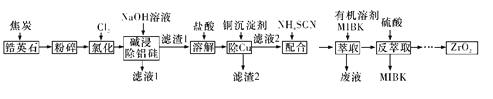
已知:Fe(SCN)3难溶于MIBK; Zr(SCN)4在水中的溶解度不大,易溶于MIBK。
请回答下列问题:
(1)ZrSiO4锆元素的化合价为____________。
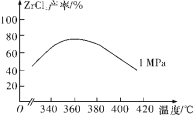
(2)“氯化”主反应为ZrSiO4(s)+2C(s)+4Cl2(g)![]() ZrCl4(g)+SiCl4(g)+2CO2(g) ΔH<0,相同时间内ZrCl4的产率随温度变化如图所示,由图可知“氯化”的最佳温度是________________。“氯化”过程中ZrCl4的产率随温度升高先增大后减小的原因是_________。
ZrCl4(g)+SiCl4(g)+2CO2(g) ΔH<0,相同时间内ZrCl4的产率随温度变化如图所示,由图可知“氯化”的最佳温度是________________。“氯化”过程中ZrCl4的产率随温度升高先增大后减小的原因是_________。
(3)写出Al2O3高温“氯化”过程中转化为AlCl3的化学方程式: ____________。
(4)本流程使用NaCN除铜,若盐酸“溶解”后溶液中的c(Cu2+)=0.01 mol·L-1,当溶液中Cu2+开始沉淀时,c(CN-)=______________。{已知Ksp[Cu(CN)2]=4.00×10-10}
(5)实验室进行“萃取”和“反萃取”的玻璃仪器是________。流程中“萃取”与“反萃取”的目的是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com