
在25 ℃的条件下,将体积都为10 mL,pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,测得稀释后溶液的pH均为5,则稀释时加入水的体积( )
A.a=b=10B.a=b>10 C.a< bD.a>b
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)4.2.2燃料电池试卷(解析版) 题型:选择题
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池的说法中正确的是( )
A.在熔融电解质中O2-由负极移向正极
B.电池的总反应是2C4H10+13O2 8CO2+10H2O
8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+4e-+2H2O 4OH-
4OH-
D.通入丁烷的一极是正极,电极反应为:C4H10-26e-+13O2- 4CO2+5H2O
4CO2+5H2O
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.3盐类水解的原理试卷(解析版) 题型:选择题
下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2O HCOO-+H3O+
HCOO-+H3O+
B.CO2+H2O HC+H+
HC+H+
C.C+H2O HC+OH-
HC+OH-
D.HS-+H2O S2-+H3O+
S2-+H3O+
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.3 酸碱中和滴定(解析版) 题型:选择题
用0.102 6 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为( )
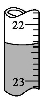
A.22.30 mLB.22.35 mL C.23.65 mL D.23.70 mL
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.3 酸碱中和滴定(解析版) 题型:选择题
酸碱恰好完全中和时( )
A.酸与碱的物质的量一定相等
B.溶液呈现中性
C.酸与碱的物质的量浓度相等
D.酸所能提供的H+与碱所能提供的OH-的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:填空题
下表是几种常见弱酸的电离常数(25 ℃)。
酸 | 电离方程式 | 电离常数K |
CH3COOH | CH3COOH | 1.76×10-5 |
H2CO3 | H2CO3 HC | K1=4.4×10-7 K2=4.7×10-11 |
H2S | H2S HS- | K1=1.3×10-7 K2=7.1×10-15 |
H3PO4 | H3PO4 H2P HP | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
回答下列问题:
(1)当温度升高时,K值 (填“增大”“减小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系? 。
(3)若把CH3COOH、H2CO3、HC、H2S、HS-、H3PO4、H2P、HP都看成是酸,其中酸性最强的是 ,最弱的是 。
(4)多元弱酸是分步电离的,每一步都有相应的电离常数,对于同一种多元弱酸的K1、K2、K3之间存在着一定的规律,此规律是 ,产生此规律的原因是 。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:选择题
甲酸的下列性质中,可以证明它是弱电解质的是( )
A.1 mol·L-1的甲酸溶液的c(H+)为1×10-2 mol·L-1
B.甲酸能与水以任意比互溶
C.10 mL 1 mol·L-1的甲酸溶液恰好与10 mL 1 mol·L-1的NaOH溶液完全反应
D.滴入石蕊溶液显红色
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)1.1中和反应反应热的测定(解析版) 题型:选择题
将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50)。下列叙述正确的是( )

A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学铁及其化合物主要性质(解析版) 题型:选择题
下列图示中能较长时间看到Fe(OH)2白色沉淀的有



A.Ⅰ、Ⅱ、Ⅳ
B.Ⅰ、Ⅱ、III、Ⅳ、Ⅵ
C.Ⅰ、III、Ⅴ
D.Ⅰ、Ⅱ、III、Ⅳ、Ⅴ、Ⅵ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com