
甲酸的下列性质中,可以证明它是弱电解质的是( )
A.1 mol·L-1的甲酸溶液的c(H+)为1×10-2 mol·L-1
B.甲酸能与水以任意比互溶
C.10 mL 1 mol·L-1的甲酸溶液恰好与10 mL 1 mol·L-1的NaOH溶液完全反应
D.滴入石蕊溶液显红色
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.4难溶电解质的溶解平衡(解析版) 题型:选择题
下列说法正确的是( )
A.向饱和食盐水中加入少量的浓盐酸,看不到明显的现象
B.将硫酸铜溶液与碳酸钠溶液混合,得到的沉淀是以Cu(OH)2为主,说明了在相同条件下Cu(OH)2的溶解度比CuCO3的更小
C.在0.01 mol·L-1 NaCl溶液中加入少量的AgNO3溶液,有白色沉淀生成,接着向上述溶液中加入足量的浓氨水,白色沉淀不会溶解
D.CaCO3溶液的导电能力很弱,是因为CaCO3是弱电解质,存在如下电离平衡:CaCO3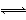 Ca2++ CO32-
Ca2++ CO32-
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2水的电离溶液的酸碱性(解析版) 题型:选择题
下列说法正确的是( )
A.水的电离方程式:H2O H++OH-
H++OH-
B.升高温度,水的电离程度增大
C.在NaOH溶液中没有H+,在HCl溶液中没有OH-
D.纯水中c(H+)=10-7 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.2 pH的计算试卷(解析版) 题型:选择题
在25 ℃的条件下,将体积都为10 mL,pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,测得稀释后溶液的pH均为5,则稀释时加入水的体积( )
A.a=b=10B.a=b>10 C.a< bD.a>b
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:填空题
(1)下列物质:①石墨 ②三氧化硫 ③液态氯化氢 ④氯气 ⑤熔融的硫酸钾 ⑥食盐晶体 ⑦硫酸溶液 ⑧乙醇 ⑨冰醋酸 ⑩NH3·H2O,其中能够导电的是 ,强电解质是 ,弱电解质是 ,非电解质是 。
(2)H2S溶于水的电离方程式为 。
①向H2S溶液中加入CuSO4溶液时,电离平衡向 移动,c(H+) ,c(S2-) 。
②向H2S溶液中加入NaOH固体时,电离平衡向 移动,c(H+) ,c(S2-) 。
③若将H2S溶液加热至沸腾,c(H2S) 。
④若要增大H2S溶液中c(S2-),最好加入 。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)2.3.3化学平衡常数试卷(解析版) 题型:填空题
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)2.3.3化学平衡常数试卷(解析版) 题型:选择题
某温度时,反应SO2(g)+O2(g) SO3(g)的平衡常数K=50,在同一温度下,反应2SO3(g)
SO3(g)的平衡常数K=50,在同一温度下,反应2SO3(g) 2SO2(g)+O2(g)的平衡常数K'应为( )
2SO2(g)+O2(g)的平衡常数K'应为( )
A.2 500B.100C.4×10-4D.2×10-2
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步练(人教选修4)2.3化学平衡状态的建立及标志(解析版) 题型:选择题
在恒温下的密闭容器中,有可逆反应:2NO+O2 2NO2(正反应为放热反应),不能说明已经达到平衡状态的是( )
2NO2(正反应为放热反应),不能说明已经达到平衡状态的是( )
A.正反应生成NO2的速率和逆反应生成O2的速率相等
B.反应容器中压强不随时间的变化而变化
C.混合气体颜色保持不变
D.混合气体的平均相对分子质量不随时间变化而变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com