
(1)下列物质:①石墨 ②三氧化硫 ③液态氯化氢 ④氯气 ⑤熔融的硫酸钾 ⑥食盐晶体 ⑦硫酸溶液 ⑧乙醇 ⑨冰醋酸 ⑩NH3·H2O,其中能够导电的是 ,强电解质是 ,弱电解质是 ,非电解质是 。
(2)H2S溶于水的电离方程式为 。
①向H2S溶液中加入CuSO4溶液时,电离平衡向 移动,c(H+) ,c(S2-) 。
②向H2S溶液中加入NaOH固体时,电离平衡向 移动,c(H+) ,c(S2-) 。
③若将H2S溶液加热至沸腾,c(H2S) 。
④若要增大H2S溶液中c(S2-),最好加入 。
(1)①⑤⑦ ③⑤⑥ ⑨⑩ ②⑧
(2)H2S H++HS-,HS-
H++HS-,HS- H++S2-
H++S2-
①右 增大 减小 ②右 减小 增大
③减小 ④NaOH固体
【解析】
试题分析: (1)有自由移动的离子或自由电子的物质才能导电,①石墨中存在自由移动的电子,⑤熔融的硫酸钾、⑦硫酸溶液中存在自由移动的离子,所以①⑤⑦可以导电。强电解质是指在水溶液中能够完全电离的电解质,③液态氯化氢、⑤熔融的硫酸钾、⑥食盐晶体都是强电解质。⑨冰醋酸、⑩NH3·H2O在水溶液中不能完全电离,属于弱电解质。非电解质是在水溶液中和熔融状态下都不导电的化合物,其中②三氧化硫、⑧乙醇符合,它们属于非电解质。①石墨、④氯气属于单质,既不是电解质也不是非电解质,⑦硫酸溶液是混合物,它不是电解质也不是非电解质。
(2)H2S是二元弱酸,在水溶液中是分两步电离的,其电离方程式应为:H2S H++HS-,HS-
H++HS-,HS- H++S2-
H++S2-
对①,当加入CuSO4时,因发生反应Cu2++S2- CuS↓,使平衡右移,导致c(H+)增大,但c(S2-)减小。
CuS↓,使平衡右移,导致c(H+)增大,但c(S2-)减小。
对②,当加入NaOH时,因发生反应H++OH- H2O,使平衡右移,导致c(H+)减小,但c(S2-)增大。
H2O,使平衡右移,导致c(H+)减小,但c(S2-)增大。
对③,当加热H2S溶液至沸腾时,因H2S挥发,使c(H2S)减小。
对④,增大c(S2-)最好是加入只与H+反应的物质,可见加入强碱如NaOH固体最适宜。
考点:弱电解质的电离


科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)4.2.2燃料电池试卷(解析版) 题型:选择题
质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )
①正极反应为:O2+4H++4e- 2H2O
2H2O
②负极反应为:2H2-4e- 4H+
4H+
③总的化学反应为:2H2+O2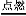 2H2O
2H2O
④氢离子通过电解质向正极移动
A.①②③ B.②③④ C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2水的电离溶液的酸碱性(解析版) 题型:选择题
已知25 ℃时KW=10-14,如果100 ℃时KW=5.5×10-13,这说明( )
A.100 ℃时水的电离程度较小
B.前者c(H+)较后者大
C.水的电离过程是一个吸热过程
D.100 ℃时0.1 mol·L-1 DCl的重水溶液中水的电离程度一定是室温时电离程度的10倍
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.3 酸碱中和滴定(解析版) 题型:选择题
酸碱恰好完全中和时( )
A.酸与碱的物质的量一定相等
B.溶液呈现中性
C.酸与碱的物质的量浓度相等
D.酸所能提供的H+与碱所能提供的OH-的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.2 pH的计算试卷(解析版) 题型:选择题
将pH=8的NaOH溶液与pH=10的NaOH溶液等体积混合后,溶液中的c(H+)最接近于( )
A.1/2(10-8+10-10) mol·L-1
B.(10-8+10-10) mol·L-1
C.(1×10-14+5×10-5) mol·L-1
D.2×10-10 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:选择题
甲酸的下列性质中,可以证明它是弱电解质的是( )
A.1 mol·L-1的甲酸溶液的c(H+)为1×10-2 mol·L-1
B.甲酸能与水以任意比互溶
C.10 mL 1 mol·L-1的甲酸溶液恰好与10 mL 1 mol·L-1的NaOH溶液完全反应
D.滴入石蕊溶液显红色
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)2.3.3化学平衡常数试卷(解析版) 题型:选择题
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.1 | 0.2 | 0 |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X(g)+3Y(g) 2Z(g),其平衡常数为1 600
2Z(g),其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步练(人教选修4)2.3化学平衡状态的建立及标志(解析版) 题型:填空题
下列可以证明H2(g)+I2(g) 2HI(g)已达平衡状态的是 。
2HI(g)已达平衡状态的是 。
①单位时间内生成n mol H2的同时,生成n mol HI
②一个H—H键断裂的同时有两个H—I键断裂
③百分含量w(HI)=w(I2)
④反应速率v(H2)=v(I2)=v(HI)
⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1
⑥温度和体积一定时,生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学钠及其化合物主要性质(解析版) 题型:选择题
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是
A.x=2.24
B.钠的物质的量为0.2 mol
C.反应时,Na、Mg、Al均过量
D.曲线b为Mg与盐酸反应的图像
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com