
已知25 ℃时KW=10-14,如果100 ℃时KW=5.5×10-13,这说明( )
A.100 ℃时水的电离程度较小
B.前者c(H+)较后者大
C.水的电离过程是一个吸热过程
D.100 ℃时0.1 mol·L-1 DCl的重水溶液中水的电离程度一定是室温时电离程度的10倍
C
【解析】
试题分析:由题意知,随水溶液温度的升高,KW也随之增大。即c(H+)·c(OH-)较大。c(H+)·c(OH-)较大,说明H2O H++OH-向右进行的程度大,由此可知水的电离是吸热的。所以A、B两项错误,C项正确;当改用重水作溶剂时,由于重水的电离程度与普通水的电离程度不一定相同(事实上不同),所以室温时重水的离子积c(D+)·c(OD-)不一定等于1×10-14,也不能将普通水在100 ℃时的离子积常数应用于重水溶液,尽管DCl是强酸,在重水溶液中能够完全电离,题目告诉的浓度可以求出溶液中的c(D+),但因不知道两种温度条件下的重水离子积常数,所以无法得出c(OD-),也就是说无法知道两种温度条件下重水分子本身的电离程度,所以D项错误。
H++OH-向右进行的程度大,由此可知水的电离是吸热的。所以A、B两项错误,C项正确;当改用重水作溶剂时,由于重水的电离程度与普通水的电离程度不一定相同(事实上不同),所以室温时重水的离子积c(D+)·c(OD-)不一定等于1×10-14,也不能将普通水在100 ℃时的离子积常数应用于重水溶液,尽管DCl是强酸,在重水溶液中能够完全电离,题目告诉的浓度可以求出溶液中的c(D+),但因不知道两种温度条件下的重水离子积常数,所以无法得出c(OD-),也就是说无法知道两种温度条件下重水分子本身的电离程度,所以D项错误。
考点:水的电离 溶液的酸碱性


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)4.3.1电解原理试卷(解析版) 题型:填空题
如图为持续电解含有一定量CaCl2水溶液(含酚酞)的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入电解液中。
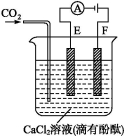
(1)电解时,F极发生 反应,电极反应为 ,E极发生 反应,电极反应为 ,电解总反应为 。
(2)电解池中产生的现象:
① 。
② 。
③ 。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.4难溶电解质的溶解平衡(解析版) 题型:选择题
下列有关AgCl沉淀的溶解平衡的说法中,正确的是( )
A.AgCl沉淀生成和溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl的溶解度减小
D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.3盐类水解的原理试卷(解析版) 题型:选择题
相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温、同体积、同浓度的HCN和HClO溶液的说法中正确的是( )
A.酸的强弱:HCN>HClO
B.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)<c(ClO-)
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.3盐类水解的原理试卷(解析版) 题型:选择题
关于盐类水解的实质,下列叙述正确的是( )
A.盐的电离平衡被破坏
B.水的电离平衡被破坏
C.没有中和反应发生
D.溶液的pH一定变大
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2水的电离溶液的酸碱性(解析版) 题型:选择题
下列说法正确的是( )
A.水的电离方程式:H2O H++OH-
H++OH-
B.升高温度,水的电离程度增大
C.在NaOH溶液中没有H+,在HCl溶液中没有OH-
D.纯水中c(H+)=10-7 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.3 酸碱中和滴定(解析版) 题型:选择题
用0.1 mol·L-1 NaOH溶液滴定0.1 mol·L-1盐酸,如达到滴定终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05 mL),继续加水至50 mL,所得溶液的pH是( )
A.4B.7.2 C.10D.11.3
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:填空题
(1)下列物质:①石墨 ②三氧化硫 ③液态氯化氢 ④氯气 ⑤熔融的硫酸钾 ⑥食盐晶体 ⑦硫酸溶液 ⑧乙醇 ⑨冰醋酸 ⑩NH3·H2O,其中能够导电的是 ,强电解质是 ,弱电解质是 ,非电解质是 。
(2)H2S溶于水的电离方程式为 。
①向H2S溶液中加入CuSO4溶液时,电离平衡向 移动,c(H+) ,c(S2-) 。
②向H2S溶液中加入NaOH固体时,电离平衡向 移动,c(H+) ,c(S2-) 。
③若将H2S溶液加热至沸腾,c(H2S) 。
④若要增大H2S溶液中c(S2-),最好加入 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学镁、铝及其化合物主要性质(解析版) 题型:选择题
海水是重要的资源。可以制备一系列物质

下列说法正确的是
A.步骤②中,应先通CO2,再通NH3
B.步骤③可将MgCl2·6H2O晶体在空气中直接加热脱水
C.步骤④、⑤、⑥反应中,溴元素均被氧化
D.除去粗盐中的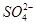 、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com