
【题目】(1)物质的量相等的 CO 和 CO2 中,同温同压下所占的体积比为____,原子个数之比为______;
(2)1.8g水与_______mol硫酸所含的分子数相等,它们所含氧原子数之比是________,其中氢原子数之比是___________。
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为________。
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠________; ②提取溴水中的溴单质______;
③除去水中的Na+、![]() 、Cl-等杂质________; ④除去CuO中的Cu ______;
、Cl-等杂质________; ④除去CuO中的Cu ______;
【答案】1:1 2:3 0.1 1:4 1:1 64g/mol C B/BF D E
【解析】
(1)同温同压下,气体的物质的量之比等于体积之比,原子的物质的量等于分子的物质的量乘以分子中原子的个数;
(2)1.8g水所含分子的数目用公式N=n×NA= ![]() ;
;
(3)利用n=![]() =
=![]() ,从而计算出M;
,从而计算出M;
(4)选择分离物质的方法时,要考虑物质的性质,除去淀粉溶液中的少量碘化钠,选择渗析,淀粉溶液属于胶体,碘化钾溶在溶液里,区分溶液和胶体的方法是渗析;溴水中的溴用有机溶剂萃取后分液;除去自来水中可溶性的离子,可用蒸馏,CuO中的Cu可用加热氧化的方式把铜氧化成氧化铜。
(1)根据阿伏伽德罗定律,在相同的温度和压强下,相同体积的任何气体含有相同数目的分子。物质的量相等的 CO和 CO2,分子的数目也相同,故体积也相同,故体积比为1:1。一个CO分子中含有两个原子,CO2分子中含有三个原子,分子的数目相同,故原子数目比为2:3,
故答案为:1:1;2:3;
(2)1.8g水中水分子的数目=![]() =
=![]() ×NA =0.1 NA个,0.1 NA个硫酸分子的物质的量为0.1mol,由于分子数相同,一个水分子含有一个氧原子,一个硫酸分子含有四个氧原子,故氧原子的数目比为1:4 ,一个水分子有两个氢原子,一个硫酸分子也有两个氢原子,其中氢原子数之比是1:1,
×NA =0.1 NA个,0.1 NA个硫酸分子的物质的量为0.1mol,由于分子数相同,一个水分子含有一个氧原子,一个硫酸分子含有四个氧原子,故氧原子的数目比为1:4 ,一个水分子有两个氢原子,一个硫酸分子也有两个氢原子,其中氢原子数之比是1:1,
故答案为:0.1;1:4;1:1;
(3)3.2g某气体中含有的分子数约为3.01×1022 利用n=![]() =
=![]() ,从而计算出M=
,从而计算出M=![]() =
=![]() =
=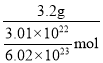 = 64g/mol,
= 64g/mol,
故答案为:64g/mol;
(4)A.过滤是使液固或气固混合物中的流体强制通过多孔性过滤介质,将其中的悬浮固体颗粒加以截留,从而实现混合物的分离操作。
B.萃取是利用化合物在两种互不相溶(或微溶)的溶剂中溶解度的不同,使化合物从一种溶剂内转移到另外一种溶剂中而提取出来的过程,萃取之后要分液。
C.渗析是一种以浓度差为推动力的膜分离操作,利用膜对溶质的选择透过性,实现不同性质溶质的分离,可用于分离溶液和胶体。
D.蒸馏是一种热力学的分离工艺,它利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的单元操作过程,是蒸发和冷凝两种单元操作的联合。①除去淀粉溶液中的少量碘化钠可选择渗析,
②提取溴水中的溴单质,可以选用萃取和分液操作;
③除去水中的Na+、![]() 、Cl-等杂质,选择蒸馏;
、Cl-等杂质,选择蒸馏;
④除去CuO中的Cu,可选择灼热氧化;
故答案为:C; B/BF;D;E。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol·L-1的NaOH溶液230mL:
(1)配制溶液时,一般可以分为以下几个步骤:(完成下列空格)
A.计算 B.称量 C.__ D.冷却 E.__ F.__ G.定容 H.摇匀、装瓶
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、量筒、还有___,使用该仪器前必须进行的一步操作是___。
(3)需称量___g烧碱固体,固体应该放在___中称量。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是__。
A.没有洗涤烧杯和玻璃棒
B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶不干燥,含有少量蒸馏水
D.定容时俯视刻度线
E.未冷却到室温就将溶液转移到容量瓶并定容
(5)若从所配制溶液取出100mL,再将这100mL溶液加水稀释成1L的溶液,则稀释后所得溶液的物质的量浓度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以下为中学化学常见的几种物质①NaOH溶液②铜丝③液氯④盐酸⑤稀硫酸⑥氨水⑦CO2⑧熔融NaCl⑨蔗糖晶体⑩酒精。属于非电解质的是________,属于电解质的是________。
(2)工业上可用浓氨水检查氯气管道是否漏气。若有Cl2漏出,与浓氨水接触会有白烟生成,同时产生一种无毒、无可燃性、不污染大气的气体。有关的化学方程式是________:。该反应中氧化剂和还原剂的物质的量之比为________。
(3)铁酸钠(Na2FeO4)是水处理过程中一种新型的净水型,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+。
①配平制取铁酸钠的化学方程式:____Fe(NO3)3+____NaOH+ ____Cl2——____Na2FeO4 +____NaNO3+____NaCl+____H2O
②用单线桥法标出反应中电子转移的方向和数目____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组学习电化学后,设计了下面的实验装置图,则下列有关该装置图的说法中正确的是 ( )
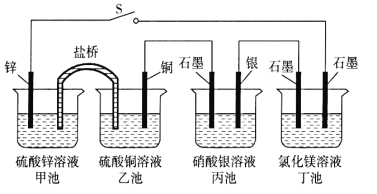
A. 合上电键后,盐桥中的阳离子向甲池移动
B. 合上电键后,丙池为电镀银的电镀池
C. 合上电键后一段时间,丙池中溶液的pH增大
D. 当丁池中生成标准状况下1120 mL Cl2气体时,丁池中理论上最多产生2.9 g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用苯甲醛(C6H5CHO)在NaOH溶液中可以制苯甲醇(C6H5CH2OH)和苯甲酸(C6H5COOH)。实验流程如图:

相关物质的性质如下表所示。回答下列问题:
物质 | 对水的相对密度 | 沸点 | 溶解性 |
苯甲醇 | 1.04 | 205.7 | 微溶于水,易溶于乙醚 |
苯甲酸 | 1.27 | 249 | 微溶于冷水,可溶于热水,易溶于乙醚 |
乙醚 | 0.71 | 34.6 | 与水互不相溶 |
(1)操作①中,需要用到的玻璃仪器除烧杯外,还有____。操作①后,苯甲醇在容器中混合物的_____(填“上”或“下”)层。
(2)乙醚层用10%Na2CO3溶液洗涤的目的是_____。操作②前常需要加入MgSO4,作用是______。操作②的装置如图,指出该装置图中两个错误:______。

(3)操作③是______,操作④是______。
(4)取106.00g苯甲醛反应,若苯甲醛的转化率为80%,乙醚的萃取率为100%,洗涤等过程损失率为10%,则最终可制得苯甲醇___g(结果保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各小题。
(1)等浓度的三种溶液①NH4HCO3、② NH4Cl、③NH4HSO4,则c(NH4+)由大到小排列的顺序为____(填序号)。
(2)常温下,将0.1 mol·L-1的HCN溶液和0.1 mol·L-1的NaCN溶液等体积混合,测得混合液中c(HCN)>c(CN-),(假设混合过程中溶液体积的改变忽略不计)。则该混合液pH____7,c(HCN)+c(CN-)_____0.1 mol·L-1,c(HCN)-c(CN-)_____2c(OH-)(填“>”,“<”或“=”)。
(3)小苏打溶液显碱性而不是显酸性的原因:________,溶液中离子浓度大小顺序:___________。
(4)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
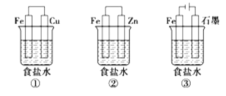
为防止金属Fe被腐蚀,可以采用上述________装置(填装置序号)原理进行防护;装置③中总反应的离子方程式为____________________。检验石墨电极产物气体的方法:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于离子反应又属于氧化还原反应的是 ( )
A.C+O2 ![]() CO2
CO2
B.2 KClO3![]() 2KCl + 3O2↑
2KCl + 3O2↑
C.HCl+NaOH = NaCl+H2O
D.Fe+CuSO4=Cu+FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铜与Fe2O3的混合物共28.8g加入300mL 2.00mol·L-1的稀硫酸中,充分反应后剩余固体的质量为6.40g。请计算:
(1)混合物中铜的物质的量为______mol。
(2)反应后的溶液中最多消耗锌片的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. HOCH2CH(CH3)2与(CH3)3COH属于碳链异构
B. ![]() 的核磁共振氢谱表明其有3种不同化学环境的氢
的核磁共振氢谱表明其有3种不同化学环境的氢
C. 除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量烧碱溶液,通过分液即得乙酸乙酯
D. 用酸性高锰酸钾溶液鉴别苯甲醇、乙醇和苯甲醛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com