
【题目】下列关于有机化合物的说法正确的是( )
A. HOCH2CH(CH3)2与(CH3)3COH属于碳链异构
B. ![]() 的核磁共振氢谱表明其有3种不同化学环境的氢
的核磁共振氢谱表明其有3种不同化学环境的氢
C. 除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量烧碱溶液,通过分液即得乙酸乙酯
D. 用酸性高锰酸钾溶液鉴别苯甲醇、乙醇和苯甲醛
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)物质的量相等的 CO 和 CO2 中,同温同压下所占的体积比为____,原子个数之比为______;
(2)1.8g水与_______mol硫酸所含的分子数相等,它们所含氧原子数之比是________,其中氢原子数之比是___________。
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为________。
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠________; ②提取溴水中的溴单质______;
③除去水中的Na+、![]() 、Cl-等杂质________; ④除去CuO中的Cu ______;
、Cl-等杂质________; ④除去CuO中的Cu ______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年12月8日,凌晨2时23分,我国在西昌卫星发射中心,嫦娥四号探测器搭载长征三号乙运载火箭成功发射,实现了世界首次月球背面软着陆和巡视探测,被认为是中国在工程技术和空间科学方面的双重跨越和创新。
I.肼(N2H4)又称联氨,常温时是一种可燃性的液体,可用作火箭燃料。
(1)已知在25℃、101kPa时,16g N2H4在氧气中完全燃烧生成氮气,放出312kJ的热量,则N2H4完全燃烧的热化学方程式是___________________________________________________。
II.如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
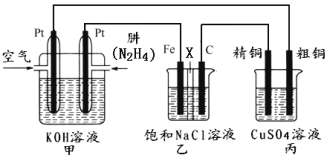
根据要求回答相关问题:
(2)甲装置中正极的电极反应式为:______________________________________。
(3)检验乙装置中石墨电极反应产物的方法是:___________________________。
(4)如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为___________g。
III.对金属制品进行抗腐蚀处理,可延长其使用寿命。该研究性学习小组又以肼(N2H4)─空气燃料电池为电源对铝材表面进行如下处理:
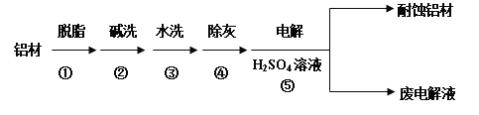
(5)流程⑤中以铝材为阳极,在H2SO4 溶液中电解,最终可在铝材表面形成氧化膜,该电解的阳极电极反应式为__________________________________。
(6)取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,其反应的离子方程式是__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的分子结构如图所示。现有试剂:①Na ②H2/Ni ③Ag(NH3)2OH ④新制Cu(OH)2 ⑤NaOH ⑥酸性KMnO4溶液。能与该化合物中两个或两个以上官能团都发生反应的试剂有( )

A.①②⑤⑥ B.①②④⑥ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列图中表示其产生H2的总体积(V)与时间(t)的关系正确的是( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol/L氨水分别滴定20.0mL 0.1mol/L的盐酸和醋酸,曲线如图所示,下列叙述中不正确的是
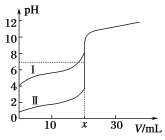
A. x=20
B. Ⅰ曲线表示的是滴定醋酸的曲线
C. 滴定过程中![]() 的值逐渐减小
的值逐渐减小
D. 当Ⅰ曲线和Ⅱ曲线pH均为7时,某一溶液中的c(Cl-)大于另一溶液中的c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应能量变化、化学反应速率和化学反应限度,在实际工业生产和生活中有着重要的意义。回答下列问题:
(1)科学家提出可利用FeO吸收和利用CO2,其原理为:
已知:C(s)+2H2O(g)====CO2(g)+2H2(g) △H=+113.4kJ·mol-1
3FeO(s)+H2O(g)====Fe3 O4(s)+H2(g) △H=+18.7kJ·mol-1
则反应6FeO(s)+CO2(g)====2Fe3O4(s)+C(s)的△H=_______。
(2)肼的制备方法是用次氯酸钠氧化过量的氨。
已知ClO-水解的方程式为:ClO-+H2O![]() HClO+OH-。常温下,该水解反应的平衡常数为Kh=1.0×10-6mol·L-1,则1.0mol·L-1NaClO溶液的pH=______。
HClO+OH-。常温下,该水解反应的平衡常数为Kh=1.0×10-6mol·L-1,则1.0mol·L-1NaClO溶液的pH=______。
(3)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g) ![]() HCN(g)+3H2 (g) △H>0
HCN(g)+3H2 (g) △H>0
①其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如下图所示。X代表的是______(填“温度”或“压强”)。
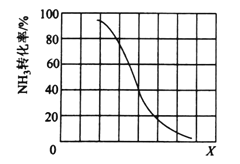
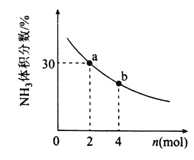
②其他条件一定,向2L密闭容器中加入nmolCH4和2molNH3,平衡时NH3体积分数随n变化的关系如下图所示。若反应从开始到a点所用时间为10min,该时间段内用CH4的浓度变化表示的反应速率为______;该温度下,b点的平衡常数为________
(4)纳米氧化亚铜Cu2O是一种用途广泛的光电材料,电化学法可用铜棒和石墨作电极,电解Cu(NO3)2稀溶液制备。电解过程中无气体产生,则铜棒作______极,阴极生成Cu2O的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg和SiO2在高温下反应生成MgO和Mg2Si。下列说法正确的是
A. 物质的熔点:Mg>MgOB. 氧元素不存在同素异形体
C. Mg的还原性强于SiD. 该反应是置换反应,镁元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生反应:2HI(g)![]() H2(g)+I2(g)△H>0,0~15s内c(HI)由0.lmol/L降到0.07mol/L,则下列说法正确的是
H2(g)+I2(g)△H>0,0~15s内c(HI)由0.lmol/L降到0.07mol/L,则下列说法正确的是
A. 当HI、H2、I2浓度之比为2:1:1时,说明该反应达平衡
B. c(HI)由0.07mol/L降到0.05mol/L所需的反应时间小于10s
C. 升高温度正反应速率加快,逆反应速率减慢
D. 0~15s内用I2表示的平均反应速率为:v(I2)=0.001mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com