
【题目】某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
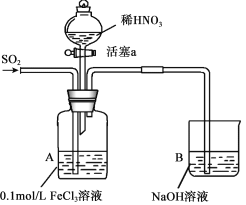
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a。 | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中注入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学用语和简单文字叙述):________。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2 ![]() Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因________。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因________。
(3)实验II中发生反应的离子方程式是__________________。
(4)实验III中,浅绿色溶液变为黄色的原因是__________________(用离子方程式表示)。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的化学方程式是______________。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。请从微粒变化的角度解释________。
【答案】Fe3++3H2O![]() Fe(OH)3+3H+,加入盐酸,增大c(H+),平衡左移,抑制Fe3+水解; Fe3+和SO2生成红棕色的Fe(SO2)63+反应速率较快:Fe3++6SO2
Fe(OH)3+3H+,加入盐酸,增大c(H+),平衡左移,抑制Fe3+水解; Fe3+和SO2生成红棕色的Fe(SO2)63+反应速率较快:Fe3++6SO2![]() Fe(SO2)63+。而反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+反应缓慢,但是反应限度较大,使溶液中c(Fe3+)降低,平衡逆向移动,红棕色逐渐褪去,最终得到浅绿色溶液; Ba2++ SO42-= BaSO4↓; 3Fe2++4H++ NO3-= 3Fe3++NO↑+2H2O; 2NO+ O2= 2NO2; 实验II中溶液中检出Fe2+和SO42-,说明Fe3+氧化SO2生成SO42-,氧化性Fe3+>SO42-;实验III中溶液变黄色、IV中检出Fe3+和NO生成,说明酸性条件下NO3-氧化Fe2+,氧化性NO3->Fe3+;所以,在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。
Fe(SO2)63+。而反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+反应缓慢,但是反应限度较大,使溶液中c(Fe3+)降低,平衡逆向移动,红棕色逐渐褪去,最终得到浅绿色溶液; Ba2++ SO42-= BaSO4↓; 3Fe2++4H++ NO3-= 3Fe3++NO↑+2H2O; 2NO+ O2= 2NO2; 实验II中溶液中检出Fe2+和SO42-,说明Fe3+氧化SO2生成SO42-,氧化性Fe3+>SO42-;实验III中溶液变黄色、IV中检出Fe3+和NO生成,说明酸性条件下NO3-氧化Fe2+,氧化性NO3->Fe3+;所以,在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。
【解析】
通过“氧化剂氧化性大于氧化产物的氧化性”原理设计实验。
(1)溶液中存在水解平衡:Fe3++3H2O![]() Fe(OH)3+3H+,加入盐酸,增大c(H+),平衡左移,抑制Fe3+水解;
Fe(OH)3+3H+,加入盐酸,增大c(H+),平衡左移,抑制Fe3+水解;
(2)Fe3+和SO2生成红棕色的Fe(SO2)63+反应速率较快:Fe3++6SO2![]() Fe(SO2)63+。而反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+反应缓慢,但是反应限度较大,使溶液中c(Fe3+)降低,平衡逆向移动,红棕色逐渐褪去,最终得到浅绿色溶液;
Fe(SO2)63+。而反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+反应缓慢,但是反应限度较大,使溶液中c(Fe3+)降低,平衡逆向移动,红棕色逐渐褪去,最终得到浅绿色溶液;
(3)加入KSCN溶液后溶液不变色,说明铁离子完全转化为亚铁离子,再加入BaCl2溶液产生白色沉淀,氧化生成硫酸根与钡离子结合为硫酸钡,反应离子方程式为:Ba2++SO42-=BaSO4↓;
(4)硝酸具有强氧化性,将溶液中亚铁离子氧化为铁离子,浅绿色溶液变为黄色,反应离子方程式为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
(5)反应生成的NO与氧气反应生成二氧化氮,二氧化氮为红棕色,发生反应的方程式是:2NO+O2=2NO2;
(6)验II中溶液中检出Fe2+和SO42-,说明Fe3+氧化SO2生成SO42-,氧化性Fe3+>SO42-;实验III中溶液变黄色、IV中检出Fe3+和NO生成,说明酸性条件下NO3-氧化Fe2+,氧化性NO3->Fe3+;所以,在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】由丙烯经下列反应制得F、G两种高分子化合物,它们都是常用的塑料。

(1)F的结构简式为________。
(2)在一定条件下,两分子E能脱去两分子形成一种六元环状化合物,该化合物的结构简式为_______。
(3)①B→C 化学方程式为______。
②C与含有NaOH的Cu(OH)2悬浊液反应的化学方程式为______。
③E→G化学方程式为______。
(4)手性分子X为E的一种同分异构体,lmolX与足量金属钠反应产生lmol氢气,lmolX与足量银氨溶液反应能生成2molAg,则X的结构简式为_______。
(5)用G代替F制成一次性塑料餐盒的优点是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐具有极强的氧化性,可作水处理剂。低温下,在Na2FeO4溶液中加入KOH浓溶液可析出K2FeO4。完成下列填空:
(1)写出上述得到K2FeO4的化学方程式_____。
(2)Na2FeO4和稀H2SO4发生如下反应:Na2FeO4+H2SO4→Fe2(SO4)3+O2↑+Na2SO4+H2O。配平上述化学方程式_____。若反应中产生3.36L(标准状况)的氧气,则转移电子数为_____。
(3)实验室配制Fe2(SO4)3溶液时,需加入少量稀硫酸,结合离子方程式用化学平衡移动原理解释其原因______。
(4)在Fe2(SO4)3溶液中滴加NaHSO3溶液,n(SO42-)增大,则还原产物是____。写出检验上述反应中Fe2(SO4)3是否消耗完全的方法______。
(5)已知HSO3-在水中既能水解也能电离。NaHSO3溶液呈酸性,溶液中c(H2SO3)_____c(SO32-)(选填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180.5 kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH3=-116.5 kJ·mol-1
(1)CO的燃烧热为______________。
(2)若1 mol N2(g)、1 mol O2(g)分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g)分子中化学键断裂时需吸收的能量为________。
Ⅱ.利用水煤气合成二甲醚的总反应为:
3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ·mol-1
(3)它可以分为两步,反应分别如下:
①2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH1=-205.1 kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=________。
(4)已知CH3OCH3(g)的燃烧热为1455 kJ·mol-1,写出表示其燃烧热的热化学方程式:_________________________________。若二甲醚燃烧生成的CO2恰好能被100 mL 0.2 mol·L-1 NaOH溶液吸收生成Na2CO3,则燃烧过程中放出的热量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在2L刚性密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误的是( )

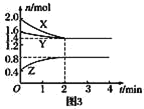
A.容器中发生的反应可表示为3X(g)+Y(g)![]() 2Z(g)
2Z(g)
B.保持其他条件不变,升高温度,X的转化率减小
C.反应进行的前4min内,用X表示的反应速率v(X)=0.075mol·L-1·min-1
D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-半径,Y的氧化物是形成酸雨的主要物质之一。请回答:
(1)Q元素在周期表中的位置___。
(2)将这五种元素原子半径从大到小排列,排在第三的元素原子是___(填元素符号)。
(3)元素的非金属性Z___Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有___ (填序号)
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)若使A按下列途径完全转化为F,F的化学式为___。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图分别表示生物体内的生物大分子的部分结构模式图,据图回答下列问题:

(1)图甲中的三种物质的基本单位都是___________,其中属于动物细胞储能物质的是___________。这三种物质中,在功能上与另外两种截然不同的是______________________。
(2)图乙化合物是肺炎双球菌遗传物质的一部分,其基本单位是__________,可用图中字母_______表示,各基本单位之间是通过___________(填①、②或③)连接起来的。
(3)图丙所示化合物的名称是___________,是由___________种氨基酸经___________过程形成的,脱去水中的氢元素来自___________,连接氨基酸之间的化学键是___________(填化学键结构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | NH3·H2O | H2CO3 | H2SO3 |
电离平衡常数 | 1.7×10-5 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.3×10-2 K2=6.3×10-8 |
请回答下列问题:
(1)H2CO3的第二级电离平衡常数的表达式K2=______。
(2)相同温度下,等pH的CH3COONa溶液、Na2CO3溶液和Na2SO3溶液,三种溶液的物质的量浓度c(CH3COONa)、c(Na2CO3)、c(Na2SO3)由大到小排序为____。
(3) 用足量Na2CO3溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为____。
(4)25℃时,向0.1 molL-1的氨水中缓缓少量CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是______。
A. B.
B.
C.  D.
D.
(5)能证明醋酸是弱酸的实验事实是______(填写序号)。
① 相同条件下,浓度均为0.1 molL-1的盐酸和醋酸,醋酸的导电能力更弱
② 25℃时,一定浓度的CH3COOH、CH3COONa混合溶液的pH等于7
③ CH3COOH溶液能与NaHCO3反应生成CO2
④ 0.1molL-1 CH3COOH溶液可使紫色石蕊试液变红
(6)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示。

① a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是______。
② a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)_____c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,H2SO3 的电离常数Ka1=1.23![]() 10-2,Ka2=5.6
10-2,Ka2=5.6![]() 10-8,HClO的电离常数Ka=2.98
10-8,HClO的电离常数Ka=2.98![]() 10-8,下列说法错误的是
10-8,下列说法错误的是
A. 常温下,相同浓度的H2SO3 比HClO酸性强
B. 常温下,将NaHSO3溶液滴入到NaClO溶液中发生反应:HSO3-+ClO-=SO32-+HClO
C. 常温下,NaHSO3溶液中HSO3-的电离程度大于其水解程度,NaHSO3溶液呈酸性
D. 将pH=5的HClO溶液加水稀释到pH=6时,溶液中部分离子浓度会升高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com