
����Ŀ����ͼ��ʾ������I�̶��������������������ƶ���M��N���������о�������Ӧ��A(g)+2B(g)![]() xC(g)��H=��192kJmol��1����M��N�ж�ͨ��1mol A��2mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ����( )
xC(g)��H=��192kJmol��1����M��N�ж�ͨ��1mol A��2mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ����( )

A. ��x=3���ﵽƽ���A�����������ϵΪ����(M)����(N)
B. ��x��3���ﵽƽ���B��ת���ʹ�ϵΪ����(M)����(N)
C. ��x��3��C��ƽ��Ũ�ȹ�ϵΪ��c(M)��c(N)
D. x����Ϊ��ֵ����ʼʱ��N�����г�������ֵ��C��ƽ���N������A��Ũ�Ⱦ����
���𰸡�D
��������M�����Ǻ��º����½�����ƽ�⣬N�����Ǻ��º�ѹ�½�����ƽ�⣬
A����x=3�����ڷ�Ӧǰ������������䣬N����������ƽ������º����½�����ƽ���Ч�����Դﵽƽ���A�����������ϵΪ���գ�M��=�գ�N������A����B����x��3�����ڷ�Ӧ�������������N����������ƽ���൱�ں��º����½�����ƽ���������������ѹǿ��С��ƽ�������ƶ���B��ת�����������Դﵽƽ���B��ת���ʹ�ϵΪ������M��������N������B����C����x��3�����ڷ�Ӧ�����������С��N����������ƽ���൱�ں��º����½�����ƽ����С���������ѹǿ����ƽ�������ƶ���C��ƽ��Ũ����������C��ƽ��Ũ�ȹ�ϵΪ��c��M����c��N������C����D�����º�ѹ�£�x����Ϊ��ֵ����ʼʱ��N�����г�������ֵ��C��һ�ߵ���A��B�����ʵ���֮�ȶ���1��2��Ϊ��Чƽ�⣬��Ӧ���Ũ����ͬ����ƽ���N������A��Ũ�Ⱦ���ȣ���D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����ǰѲ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܣ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ��(��H)����֪���»�ѧ���ļ��ܣ�
��ѧ�� | H��H | Cl��Cl | H��Cl |
����1 mol��ѧ��ʱ�ų������� | 436kJ/mol | 243kJ/mol | 431kJ/mol |
�������Ȼ�ѧ����ʽ����ȷ����
A.![]() H2(g)��
H2(g)��![]() Cl2(g)=HCl(g) ��H=��91.5kJ/mol
Cl2(g)=HCl(g) ��H=��91.5kJ/mol
B.H2(g)+Cl2(g)=2HCl(g) ��H=��183kJ/mol
C.2HCl(g)=H2(g)+Cl2(g) ��H=��183kJ/mol
D.![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g) ��H=��91.5kJ/mol
Cl2(g)=HCl(g) ��H=��91.5kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͭ�Ͻ���Cu����������Ϊ80%��90%��������Fe�ȡ�ͨ���ü�ӵ������ⶨ����Cu�ĺ������������£�
��ȡa g��Ʒ������ϡH2SO4��H2O2��Һʹ���ܽ⣬��г�ȥ������H2O2����ȴ����ˣ���Һ������250 mL����ƿ�У�
��ȡ50.00 mL��Һ����ƿ�У�����NH4F��Һ��������ҺpHΪ3��4����ַ�Ӧ�������KI��Һ�����ɰ�ɫ��������Һ���ػ�ɫ��
��������ƿ�м���c mol��L1 Na2S2O3��Һ�ζ�������ƿ����ҺΪdz��ɫʱ����������������Һ����������dz��ɫ���ټ���KSCN��Һ������������յ㣻
����ƽ�вⶨ���Σ�����Na2S2O3��Һ�����ƽ��Ϊv mL������ͭ������������
��֪������F��Fe3+�����ȶ���FeF63����ɫ����
����I2��ˮ���ܽ��С���ӷ���
����I2+I I3���ػ�ɫ����
����I2+2Na2S2O3== 2NaI+Na2S4O6����ɫ����
(1)����Cu�ܽ�����ӷ���ʽ��__________________________��
(2)����Cu2+��I��Ӧ����CuI��ɫ������I2��
�ټ���NH4F��Һ��Ŀ����__________________________��
��Cu2+��I��Ӧ�����ӷ���ʽ��_________________________��
�ۼ������KI��Һ��������________________________________��
(3)����ʱ��CuSCN���ܽ�ȱ�CuIС��CuI��������������I2��I3��ʹ�ⶨ�����ȷ�����У��ڵζ����յ�ǰ����KSCN��Һ��ԭ����_��
(4)��Ʒ��Cu����������Ϊ______(�г�����ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�д��������µ�ƽ�⣺Br2��H2O![]() HBr��HBrO�����д�ʩ������ʹ��Һ��ɫ��dz����
HBr��HBrO�����д�ʩ������ʹ��Һ��ɫ��dz����
A. ͨ����ϩ����B. ͨ��SO2����C. ����NaF����D. ����NaI����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������,��20mL0.05molL-1��ijϡ��H2B��Һ�е���0.1molL-1��ˮ����Һ����ˮ�����������Ũ������백ˮ����仯��ͼ�����з�����ȷ����
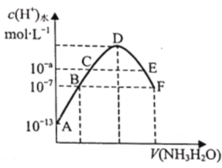
A.NaHB��Һ��һ������H2B����
B.A��B��C������Һ��pH��С��D��E��F������Һ��pH������
C.E��Һ������Ũ�ȴ�С��ϵΪc(NH4+)>c(B2-)>c(H+)>c��OH-)
D.B����ҺpH=7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������[(NH4)2Fe(SO4)2���Ƿ�����ѧ�е���Ҫ�Լ����ڲ�ͬ�¶��¼��ȷֽ����ò��ﲻͬ�������ͼʵ��װ�ã��г�װ����ȥ������500��ʱ������������A�е�������������ֽ���ȫ��ȷ���ֽ���������������������������ʡ�ˮ���ľ���ɷ֣���֪ÿ��װ���е�ҩƷ��������
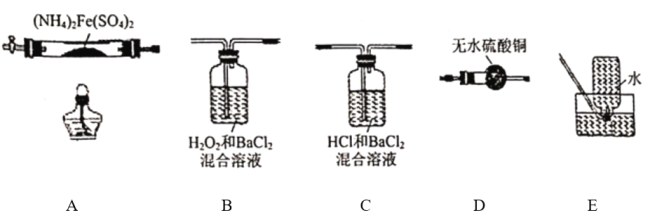
��1����������װ����ɸ�ʵ�飬���װ�õ���ȷ����˳��Ϊ_______________(��װ���������ĸ������˳��ÿ��װ�ö�Ҫʹ�ã�������Aǰ��Ҫͨ��һ��ʱ��N2Ŀ����_______________��
��2�����۲쵽B���а�ɫ�������ɣ�C��������������װ��C������Ϊ_______________,D�а�ɫ��Ϊ��ɫ��д��B�з�����Ӧ�����ӷ���ʽ_______________װ��B��װ��C�ܷ�_______________���� ���ܡ�����ԭ����_______________����ܡ�����˿գ���
��3��A�й�����ȫ�ֽ���Ϊ����ɫ��ĩ��ijͬѧ���ʵ����֤����������ΪFe2O3��������FeO���������ɱ������ݣ��Լ�����������Ʒ��ѡ����
ʵ�鲽�� | Ԥ������ | ���� |
_______________ | _______________ | �̱��������ΪFe2O3 |
��4�������������500��ʱ��������������ȫ�ֽ⣬��E���ռ���������ֻ��N2,A�й��������Fe2O3������Ϊ80g,B�г������ʵ���Ϊ2rnol,������N2������Ϊ_______________g��
��5��ij����(Cr2O72-����ˮ�������������Һ�ζ���������Ӧ����Ԫ�غ�Ԫ����ȫת��Ϊ�����������и�Ԫ�ػ��ϼ�Ϊ+3),�ó����������õ�amolFeOFemCrnO3�������Ǵ��������е�ʵ����ģ���������������淋����ʵ���Ϊ_______________mol(��a�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯����ָһ�������£�1mol�����ͻ��������ʱ�ų��������������ǻ���ϩ��![]() ����������ϩ��
����������ϩ��![]() ���ͱ����⻯�����ݡ�����˵����ȷ����
���ͱ����⻯�����ݡ�����˵����ȷ����
������ |
|
|
|
�⻯�� | -119��7 | -232��7 | -208��4 |
A.���⻯�����ݿ��Ʋ⣬������ϩ��![]() �ķ�Ӧ�����
�ķ�Ӧ�����
B.����ϩ��������ϩ�ͱ�����ͬ�Ĺ�����
C.���ֻ������л�����ϩ���ȶ�����ǿ
D.���������£�1mol![]() ת��Ϊ
ת��Ϊ![]() ʱ�ų�����
ʱ�ų�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���������ˮ�еμ�NaOH��Һ����Һ��ˮ���������![]() �ĸ�������NaOH��Һ���֮��Ĺ�ϵ��ͼ��ʾ������˵����ȷ��
�ĸ�������NaOH��Һ���֮��Ĺ�ϵ��ͼ��ʾ������˵����ȷ��
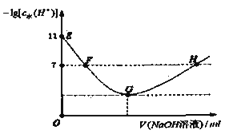
A.��pH��ֽ�ⶨE���Ӧ����Һ��![]()
B.F��H���Ӧ����Һ������![]()
C.��ˮϡ��H���Ӧ����Һ����Һ��pH����
D.G���Ӧ����Һ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����������˵����ȷ����
A.1L 1mol��L-1��NaOH��Һ�к���NA����ԭ��
B.���³�ѹ�£�14gCO��N2�����������������Ϊ7NA
C.NA��һ����̼���Ӻ�0.5 mol�����������Ϊ7��4
D.��״������11.2L����������ԭ����ΪNA��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com