
【题目】下列实验不能达到预期目的的是( )
序号 | 实验内容 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较Cl2、Br2的非金属性强弱 |
B | Cl2、S分别与Fe反应 | 比较Cl2、S的氧化性强弱 |
C | 测定相同浓度的Na2CO3、Na2SO4两溶液的pH | 比较碳酸、硫酸的稳定性强弱 |
D | 测定相同浓度的盐酸、醋酸两溶液的导电性 | 比较盐酸、醋酸的酸性强弱 |
A.A
B.B
C.C
D.D
 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】图为北京奥运会的奖牌﹣﹣“金镶玉”牌,使用了昂贵的玉石材料,其化学成分多为含水钙镁硅酸盐,如Ca2Mg5Si8O22(OH)2等.下列说法正确的是( )
A.Ca2Mg5Si8O22(OH)2可用氧化物的形式表示为2CaO5MgO8SiO2H2O
B.从分类的角度看,Ca2Mg5Si8O22(OH)2为氧化物
C.玉石材料性质稳定,耐强酸和强碱的腐蚀
D.Ca2Mg5Si8O22(OH)2易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变 化如图(Ⅰ)所示.保持其他条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示.下列结论正确的是( ) 
A.t2时,保持其它条件和物质状态不变,增加压强,化学平衡向逆反应方向移动
B.T℃时,若密闭容器中各物质起始浓度为:0.4 mol/L X、0.4 mol/L Y、0.2 mol/L Z.保持其他条件不变,达到平衡时z的浓度为0.4 mol/L
C.图(Ⅱ)中T1>T2 , 则正反应是吸热反应
D.其他条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,冰醋酸加水稀释过程中溶液的导电能力有如图所示曲线,请回答. 
①a、b、c三点的氢离子浓度由小到大的顺序为 .
②a、b、c三点中,醋酸的电离程度最大的一点是 .
③测得某醋酸溶液中氢离子浓度为0.004molL﹣1 , 则醋酸的电离度为 , 该温度下醋酸的电离平衡常数K=
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应 A(g)+3B(g)2C(g)+2D(g),在不同情况下,测得有下列四个反应速率,其反应速率最快的是( )
A.v(A)=0.15molL﹣1s﹣1
B.v(B)=0.6molL﹣1s﹣1
C.v(C)=0.5molL﹣1s﹣1
D.v(D)=0.4molL﹣1s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应中的能量变化有重要意义.请根据学过的知识回答下列问题:
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示: 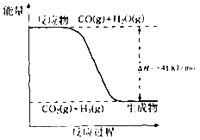
①反应的热化学方程式为 .
②已知:C(s)+H2O (g)═CO(g)+H2(g)△H=+131kJmoL﹣1
则C(s)+CO2(g)═2CO(g)△H= .
(2)化学反应可视为旧键断裂和新键形成的过程.:已知N≡N键的键能是948.9kJmol﹣1 , H﹣H键的键能是436.0kJmol﹣1;N﹣H键的键能是391.55kJ/mol..则 ![]() N2(g)+
N2(g)+ ![]() H2(g)═NH3(g)△H= .
H2(g)═NH3(g)△H= .
(3)在25℃、101Pa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是
A. 肯定只有SO2和NOB. 肯定没有Cl2、O2和NO
C. 可能有Cl2和O2D. 肯定只有NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应Cu(s)+2Ag+(aq)Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计
A.指针偏转方向如图所示,有关叙述正确的是( ) 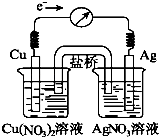
B.KNO3盐桥中的K+移向Cu(NO3)2溶液
C.当电流计指针指向0时,该反应达平衡,平衡常数K=0
D.若向硝酸银溶液中加入NaCl固体,随着NaCl量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转
E.向硝酸铜溶液中加入NaOH固体,随着NaOH量的增加,电流计指针向右偏转幅度减小→指针指向0→向左偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com